对于可逆反应CO+H2O(g)⇌CO2+H2,回答下列问题:
(1)830 K时,若起始时c(CO)=2 mol•L﹣1,c(H2O)=3 mol•L﹣1,平衡时CO的转化率为60%,水蒸气的转化率为_____ ;平衡常数K的值为_____ 。
(2)830 K时,若只将起始时c(H2O)改为6 mol•L﹣1,则水蒸气的转化率为_____ 。
(3)若830 K时,某时刻混合体系中各气体的浓度为c(CO2)=0.4 mol•L﹣1、c(CO)=0.6 mol•L﹣1、c(H2O)=3 mol•L﹣1,c(H2)=2 mol•L﹣1请判定该体系中反应进行的方向:_____ (填“正向进行”“逆向进行”或“达到平衡”)。
(1)830 K时,若起始时c(CO)=2 mol•L﹣1,c(H2O)=3 mol•L﹣1,平衡时CO的转化率为60%,水蒸气的转化率为
(2)830 K时,若只将起始时c(H2O)改为6 mol•L﹣1,则水蒸气的转化率为
(3)若830 K时,某时刻混合体系中各气体的浓度为c(CO2)=0.4 mol•L﹣1、c(CO)=0.6 mol•L﹣1、c(H2O)=3 mol•L﹣1,c(H2)=2 mol•L﹣1请判定该体系中反应进行的方向:
更新时间:2019/12/31 18:42:46
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石(TiO2)转化为TiCl4,再进一步还原得到钛。TiO2转化为TiCl4有直接氯化法和碳氯化法
(ⅰ)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ΔH1=172kJ·mol-1
(ⅱ)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) ΔH2=-51kJ·mol-1
在1.0×105pa,将TiO2、C、Cl2以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。

反应C(s)+CO2(g)=2CO(g)的平衡常数 Kp(1400℃)=___________ Pa。
(ⅰ)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ΔH1=172kJ·mol-1
(ⅱ)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) ΔH2=-51kJ·mol-1
在1.0×105pa,将TiO2、C、Cl2以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。

反应C(s)+CO2(g)=2CO(g)的平衡常数 Kp(1400℃)=
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将 和
和 充入密闭容器中发生反应
充入密闭容器中发生反应 ,压强为
,压强为 和
和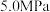 下
下 的平衡转化率随温度的变化关系如图所示。
的平衡转化率随温度的变化关系如图所示。
b点对应的平衡常数
___________  (
( 为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。

 和
和 充入密闭容器中发生反应
充入密闭容器中发生反应 ,压强为
,压强为 和
和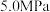 下
下 的平衡转化率随温度的变化关系如图所示。
的平衡转化率随温度的变化关系如图所示。b点对应的平衡常数

 (
( 为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】在一定条件下,将2 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。
(1)x=_______ ,2min内A的平均反应速率v(A)=_______ 。
(2)B的转化率为_______ ,该温度下反应的平衡常数的值为_______ (结果保留三位有效数字)。
(3)其他条件不变,若再向容器中加入0.2 mol B和0.2 mol C,此时v(正)_______ v(逆)(填“>”“=”或“<”)。
 xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。(1)x=
(2)B的转化率为
(3)其他条件不变,若再向容器中加入0.2 mol B和0.2 mol C,此时v(正)
您最近半年使用:0次
【推荐1】已知 热分解反应为
热分解反应为 。在
。在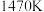 、
、 反应条件下,将
反应条件下,将 的混合气进行上述反应。平衡时混合气中
的混合气进行上述反应。平衡时混合气中 与
与 的分压相等,
的分压相等, 平衡转化率为
平衡转化率为___________ ,平衡常数
_________  。
。
 热分解反应为
热分解反应为 。在
。在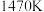 、
、 反应条件下,将
反应条件下,将 的混合气进行上述反应。平衡时混合气中
的混合气进行上述反应。平衡时混合气中 与
与 的分压相等,
的分压相等, 平衡转化率为
平衡转化率为
 。
。
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某温度下,在一个体积为2L的固定不变的密闭容器中充入2molSO2和1molO2,发生2SO2(g)+O2(g) 2SO3(g)反应。5min后反应达到化学平衡状态,平衡时测得容器中混合气体为2.4mol。求:
2SO3(g)反应。5min后反应达到化学平衡状态,平衡时测得容器中混合气体为2.4mol。求:
(1)以SO3的浓度变化表示该反应的化学反应速率为________
(2)该反应中SO2的平衡转化率为________
(3)该反应的平衡常数K值为________
 2SO3(g)反应。5min后反应达到化学平衡状态,平衡时测得容器中混合气体为2.4mol。求:
2SO3(g)反应。5min后反应达到化学平衡状态,平衡时测得容器中混合气体为2.4mol。求:(1)以SO3的浓度变化表示该反应的化学反应速率为
(2)该反应中SO2的平衡转化率为
(3)该反应的平衡常数K值为
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】反应 I2(g)+H2(g) 2HI(g)在密闭容器中达到平衡时,测得:c(I2)=0.11mmol•L-1,c(H2)=0.11mmol•L-1,c(HI)=0.77mmol•L-1。(1mmol•L-1=10-3mol•L-1)
2HI(g)在密闭容器中达到平衡时,测得:c(I2)=0.11mmol•L-1,c(H2)=0.11mmol•L-1,c(HI)=0.77mmol•L-1。(1mmol•L-1=10-3mol•L-1)
(1)该温度下,该反应的化学平衡常数 K=___________ 。
(2)相同温度下,按以下初始浓度进行实验:
① 反应向__________ 方向(填“正反应”或者“逆反应”)进行,结合计算说明理由:___________ 。
②该反应达到平衡时,容器中c(HI)=___________ mmol•L-1,I2 的转化率是___________ 。
 2HI(g)在密闭容器中达到平衡时,测得:c(I2)=0.11mmol•L-1,c(H2)=0.11mmol•L-1,c(HI)=0.77mmol•L-1。(1mmol•L-1=10-3mol•L-1)
2HI(g)在密闭容器中达到平衡时,测得:c(I2)=0.11mmol•L-1,c(H2)=0.11mmol•L-1,c(HI)=0.77mmol•L-1。(1mmol•L-1=10-3mol•L-1)(1)该温度下,该反应的化学平衡常数 K=
(2)相同温度下,按以下初始浓度进行实验:
| 物质 | 初始浓度 |
| c(I2)/mmol•L-1 | 1.00 |
| c(H2)/mmol•L-1 | 1.00 |
| c(HI)/mmol•L-1 | 1.00 |
②该反应达到平衡时,容器中c(HI)=
您最近半年使用:0次



