将 和
和 充入密闭容器中发生反应
充入密闭容器中发生反应 ,压强为
,压强为 和
和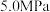 下
下 的平衡转化率随温度的变化关系如图所示。
的平衡转化率随温度的变化关系如图所示。
b点对应的平衡常数
___________  (
( 为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。

 和
和 充入密闭容器中发生反应
充入密闭容器中发生反应 ,压强为
,压强为 和
和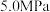 下
下 的平衡转化率随温度的变化关系如图所示。
的平衡转化率随温度的变化关系如图所示。b点对应的平衡常数

 (
( 为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
2023高三·全国·专题练习 查看更多[1]
(已下线)考向3 Kc、Kp、转化率及相关计算
更新时间:2023-03-10 01:34:25
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】在气体总压强分别为p1和p2时,反应2SO3(g)  2SO2(g)+O2(g)在不同温度下达到平衡,测得SO3(g)及SO2(g)的物质的量分数如图所示:
2SO2(g)+O2(g)在不同温度下达到平衡,测得SO3(g)及SO2(g)的物质的量分数如图所示:
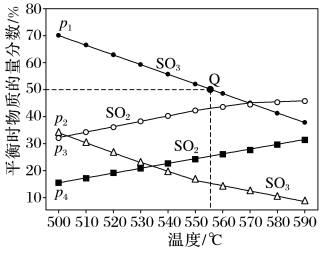
(1)压强:p1___________ (填“>”或“<”)p2
(2)若p1=0.81 MPa,起始时充入一定量的SO3(g)发生反应,计算Q点对应温度下该反应的平衡常数Kp=___________ MPa(用平衡分压代替平衡浓度计算。分压=总压×物质的量分数)
 2SO2(g)+O2(g)在不同温度下达到平衡,测得SO3(g)及SO2(g)的物质的量分数如图所示:
2SO2(g)+O2(g)在不同温度下达到平衡,测得SO3(g)及SO2(g)的物质的量分数如图所示:
(1)压强:p1
(2)若p1=0.81 MPa,起始时充入一定量的SO3(g)发生反应,计算Q点对应温度下该反应的平衡常数Kp=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】在2L带气压计的恒容密闭容器中通入2 molX(g)和1molY(g),发生反应:2X(g)+Y(g) 2Z(g) ΔH<0。若达到平衡时气体总物质的量变为原来的0.85倍,请回答下列问题。
2Z(g) ΔH<0。若达到平衡时气体总物质的量变为原来的0.85倍,请回答下列问题。
(1)若反应经历5min达到平衡,则Y的平均反应速率为__ 。
(2)相同条件下进行反应,在t1时刻,只改变下列某一种条件,其曲线图象如图甲。
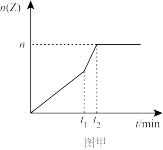
若n=0.9mol,t1时刻改变的条件是__ (填选项编号,A.升温 B.降温 C.加压 D.减压 E.加催化剂),t2__ 5min(填“>”“<”或“=”,下同)。
(3)若其他条件不变,原容器为恒压容器,达到平衡后Z的物质的量__ 0.9mol。
(4)若将物质的量均为3mol的物质X、Y混合于5L容器中发生反应,在反应过程中Z的物质的量分数随温度变化如图乙。
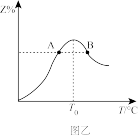
①A、B两点Z物质正反应速率的大小关系是__ ;(速率用A、B表示)
②温度T<T0时,Z%逐渐增大的原因是___ 。
 2Z(g) ΔH<0。若达到平衡时气体总物质的量变为原来的0.85倍,请回答下列问题。
2Z(g) ΔH<0。若达到平衡时气体总物质的量变为原来的0.85倍,请回答下列问题。(1)若反应经历5min达到平衡,则Y的平均反应速率为
(2)相同条件下进行反应,在t1时刻,只改变下列某一种条件,其曲线图象如图甲。

若n=0.9mol,t1时刻改变的条件是
(3)若其他条件不变,原容器为恒压容器,达到平衡后Z的物质的量
(4)若将物质的量均为3mol的物质X、Y混合于5L容器中发生反应,在反应过程中Z的物质的量分数随温度变化如图乙。

①A、B两点Z物质正反应速率的大小关系是
②温度T<T0时,Z%逐渐增大的原因是
您最近一年使用:0次
【推荐3】回答下列问题:
消除含氮、硫等化合物对大气的污染,对建设美丽家乡、打造宜居环境具有重要意义。
(1)容积均恒定为1 L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2 mol的NO2,发生反应:2NO2(g) ⇌N2O4 ΔH<0,甲中NO2的相关量随时间变化如图所示。
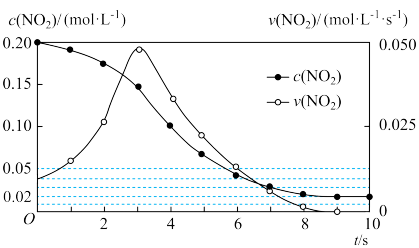
① 0~3 s内,甲容器中NO2的反应速率增大的原因是___________ 。
② 甲达到平衡时,温度若为T ℃,此温度下的平衡常数K=___________ 。(不用注明单位)
③ 平衡时,p甲___________ p乙(填“>”、“<”或“=”,下同),原因是:___________ 。
④平衡时,K甲___________ K乙
(2)汽车尾气中CO与H2O(g)在一定条件下可以发生反应:CO(g)+ H2O(g)⇌CO2(g)+H2(g) ΔH2<0.820℃ 时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0.
平衡时,甲容器中CO的转化率是___________ (填“>”、“=”、“<”或“无法判断”);丙容器中n(CO)为___________ mol。
消除含氮、硫等化合物对大气的污染,对建设美丽家乡、打造宜居环境具有重要意义。
(1)容积均恒定为1 L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2 mol的NO2,发生反应:2NO2(g) ⇌N2O4 ΔH<0,甲中NO2的相关量随时间变化如图所示。

① 0~3 s内,甲容器中NO2的反应速率增大的原因是
② 甲达到平衡时,温度若为T ℃,此温度下的平衡常数K=
③ 平衡时,p甲
④平衡时,K甲
(2)汽车尾气中CO与H2O(g)在一定条件下可以发生反应:CO(g)+ H2O(g)⇌CO2(g)+H2(g) ΔH2<0.820℃ 时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0.
| 起始物质的量 | 甲 | 乙 | 丙 |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】设在容积可变的密闭容器中充入10 mol N2(g)和10 mol H2(g),反应在一定条件下达到平衡时,NH3的体积分数为0.25。计算[(1)、(2)的计算都需按格式写计算过程,否则答案对也不给分]
(1)该条件下反应N2(g)+3H2(g) 2NH3(g) 的平衡常数
2NH3(g) 的平衡常数________ 。(设该条件下,每1mol气体所占的体积为VL)
(2)上述反应的平衡时,再充入10 mol的N2,根据计算,平衡应向什么方向移动________
(3)某温度下将所得的氨气配成0.1 mol•L-1的溶液,所得溶液的pOH_____ ;将该溶液冲稀100倍;计算此时氨水的电离度为________ (已知该温度下Kb(NH3·H2O) =1.0×10-5)
(1)该条件下反应N2(g)+3H2(g)
 2NH3(g) 的平衡常数
2NH3(g) 的平衡常数(2)上述反应的平衡时,再充入10 mol的N2,根据计算,平衡应向什么方向移动
(3)某温度下将所得的氨气配成0.1 mol•L-1的溶液,所得溶液的pOH
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】已知合成氨反应N2(g)+3H2(g)⇌2NH3(g) ΔH=-92kJ·mol-1。

科研小组模拟不同条件下的合成氨反应,向刚性容器中充入10.0molN2和20.0molH2,不同温度下平衡混合物中氨的体积分数与总压强(p)的关系如图2所示,在T2、50MPa时,平衡常数Kp=___________ MPa-2(列出表达式,分压=总压×物质的量分数)。

科研小组模拟不同条件下的合成氨反应,向刚性容器中充入10.0molN2和20.0molH2,不同温度下平衡混合物中氨的体积分数与总压强(p)的关系如图2所示,在T2、50MPa时,平衡常数Kp=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】t ℃时,将2mol A 和 6 mol B 充入容积固定为 2 L 的密闭容器中发生反应: A(g)+2B(g)  2C(g)。 反应 2 min 时测得 C 的浓度为 0.4 mol·L- 1 ,4 min 末反应达到平衡, B 的转化率为 50%。试计算:
2C(g)。 反应 2 min 时测得 C 的浓度为 0.4 mol·L- 1 ,4 min 末反应达到平衡, B 的转化率为 50%。试计算:
(1)第 2 min 到第 4 min 内 A 的平均反应速率为_______
(2)t ℃时该反应的平衡常数为_______
(3)若从反应开始到建立平衡时放出热量 353.88 kJ,则该反应的 ΔH=_______ 。(写出三个题 完整计算过程,无计算过程不给分)
 2C(g)。 反应 2 min 时测得 C 的浓度为 0.4 mol·L- 1 ,4 min 末反应达到平衡, B 的转化率为 50%。试计算:
2C(g)。 反应 2 min 时测得 C 的浓度为 0.4 mol·L- 1 ,4 min 末反应达到平衡, B 的转化率为 50%。试计算:(1)第 2 min 到第 4 min 内 A 的平均反应速率为
(2)t ℃时该反应的平衡常数为
(3)若从反应开始到建立平衡时放出热量 353.88 kJ,则该反应的 ΔH=
您最近一年使用:0次



