以C、CO、CO2、CH4等含1个碳原子的物质为原料,可以合成一些化工原料和燃料。
(1)碳原子的核外电子排布式是___ ,其最外层有___ 种运动状态不同的电子。
(2)上述物质中属于非极性分子的是___ 。
(3)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质。
①用合成气制备二甲醚时,还产生了一种常温为液态的氧化物,写出制备二甲醚的化学方程式____ 。
②仅用合成气为原料不可能合成的物质是___ (填字母序号)。
a.甲醇 b.乙二醇 c.乙二酸 d.尿素
工业上可用CO2生产燃料甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)+Q(Q>0)。在2L的密闭容器中,发生上述反应:测得n(CO2)和n(CH3OH)随时间变化如图所示。
CH3OH(g)+H2O(g)+Q(Q>0)。在2L的密闭容器中,发生上述反应:测得n(CO2)和n(CH3OH)随时间变化如图所示。
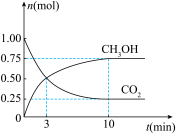
(4)该反应的化学平衡常数的表达式K=___ ,如果平衡常数K减小,平衡___ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(5)从反应开始到平衡,H2的平均反应速率v(H2)=___ 。
(6)为了提高CH3OH的产量,理论上可以采取的合理措施有___ 、___ (任写2条措施)。
(7)常温常压下,16g液态甲醇完全燃烧,当恢复到原状态时,放出369.2kJ的热量,写出该反应的热化学方程式___ 。
(1)碳原子的核外电子排布式是
(2)上述物质中属于非极性分子的是
(3)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质。
①用合成气制备二甲醚时,还产生了一种常温为液态的氧化物,写出制备二甲醚的化学方程式
②仅用合成气为原料不可能合成的物质是
a.甲醇 b.乙二醇 c.乙二酸 d.尿素
工业上可用CO2生产燃料甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)+Q(Q>0)。在2L的密闭容器中,发生上述反应:测得n(CO2)和n(CH3OH)随时间变化如图所示。
CH3OH(g)+H2O(g)+Q(Q>0)。在2L的密闭容器中,发生上述反应:测得n(CO2)和n(CH3OH)随时间变化如图所示。
(4)该反应的化学平衡常数的表达式K=
(5)从反应开始到平衡,H2的平均反应速率v(H2)=
(6)为了提高CH3OH的产量,理论上可以采取的合理措施有
(7)常温常压下,16g液态甲醇完全燃烧,当恢复到原状态时,放出369.2kJ的热量,写出该反应的热化学方程式
2020·上海静安·一模 查看更多[2]
更新时间:2020-01-04 14:20:17
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】过氧化物是一类非常重要的化合物,从人们制得第一种过氧化物距今已有200多年的历史了,在众多的过氧化物中过氧化氢迄今为止仍然得到广泛的应用。
(1)与H2O2具有相同的电子总数的双原子分子有_______ (写两种);
(2)若从海水中提取碘,需将碘化物变成单质碘。写出在酸性条件下H2O2氧化I-离子的离子方程式_______ ;
(3)Na2O2、K2O2、CaO2和BaO2都能与酸作用生成H2O2,目前实验室制取H2O2可通过上述某种过氧化物与适量的稀H2SO4作用并过滤后获得,其中最适合的过氧化物是_______ (填化学式);
(4)纯H2O2可用作火箭燃料的氧化剂,已知0.4mol液态肼(N2H4)与足量的液态H2O2反应,生成N2(g)和H2O(g),放出256.6kJ的热量,则该反应的热化学方程式是_______ 。
(1)与H2O2具有相同的电子总数的双原子分子有
(2)若从海水中提取碘,需将碘化物变成单质碘。写出在酸性条件下H2O2氧化I-离子的离子方程式
(3)Na2O2、K2O2、CaO2和BaO2都能与酸作用生成H2O2,目前实验室制取H2O2可通过上述某种过氧化物与适量的稀H2SO4作用并过滤后获得,其中最适合的过氧化物是
(4)纯H2O2可用作火箭燃料的氧化剂,已知0.4mol液态肼(N2H4)与足量的液态H2O2反应,生成N2(g)和H2O(g),放出256.6kJ的热量,则该反应的热化学方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】近几年全国各地都遭遇“十面霾伏”。其中机动车尾气和燃煤产生的烟气对空气质量恶化贡献较大。
⑴ 汽车尾气净化的主要原理为:2NO(g) + 2CO(g) 2CO2(g)+ N2(g) △H<0
2CO2(g)+ N2(g) △H<0
若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是_________ (填代号)。

(2)一定条件下氮氧化物和碳氧化物可以反应,已知2.24L(折算为标准状况)N2O和CO的混合气体在点燃条件恰好完全反应,放出bkJ热量。生成的3种产物均为大气组成气体,并测得反应后气体的密度是反应前气体密度的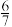 倍。请写出该反应的热化学方程式
倍。请写出该反应的热化学方程式_____________ 。
(3)电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。


① NO2、O2和熔融NaNO3可制作燃料电池,其原理见上方右图。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为________________________________ 。
② 电解NO制备NH4NO3原理如上方左图所示。石墨III为_______ 极 ,石墨IV的电极反应式为___________ 。为使电解产物完全转化为NH4NO3,需要补充的物质X的化学式为______ 。
⑴ 汽车尾气净化的主要原理为:2NO(g) + 2CO(g)
 2CO2(g)+ N2(g) △H<0
2CO2(g)+ N2(g) △H<0若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是

(2)一定条件下氮氧化物和碳氧化物可以反应,已知2.24L(折算为标准状况)N2O和CO的混合气体在点燃条件恰好完全反应,放出bkJ热量。生成的3种产物均为大气组成气体,并测得反应后气体的密度是反应前气体密度的
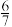 倍。请写出该反应的热化学方程式
倍。请写出该反应的热化学方程式(3)电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。


① NO2、O2和熔融NaNO3可制作燃料电池,其原理见上方右图。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为
② 电解NO制备NH4NO3原理如上方左图所示。石墨III为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】向某密闭容器中加入0.3mol A、0.1mol C和一定量的气体B三种气体,在一定条件下发生反应,各物质浓度随时间变化如图所示。下面右图为t2时刻后改变容器中条件,平衡体系中速率随时间变化的情况且t2-t5四个阶段都各改变一种条件,所用条件均不同。t3-t4阶段为使用催化剂。

(1)若t1=15s,则t0-t1阶段以C浓度变化表示的反应速率为v(C)=_______ mol/(L∙s);
(2)若t2-t3阶段,C的体积分数变小,此阶段v正_______ v逆(填“大于”、“小于”或“等于”)
(3)B的起始物质的量为_______ mol;
(4)t1时刻,平衡常数K=_______ ;
(5)t5-t6阶段容器内A的物质的量共减小0.03mol,而此过程中容器与外界的热交换总量为a kJ,写出该反应的热化学方程式_______ ;
(6)若t2时刻后图象变化如-图,则改变条件为_______


a.恒温恒压下,按照2:1比例充入任意量的B和C
b.恒温恒压下,加入0.24mol A、0.06mol B和0.14mol C
c.恒温恒压下,加入0.12mol A、0.1mol B和0.22mol C
d.恒温恒压下,加入0.14mol B和0.30mol C

(1)若t1=15s,则t0-t1阶段以C浓度变化表示的反应速率为v(C)=
(2)若t2-t3阶段,C的体积分数变小,此阶段v正
(3)B的起始物质的量为
(4)t1时刻,平衡常数K=
(5)t5-t6阶段容器内A的物质的量共减小0.03mol,而此过程中容器与外界的热交换总量为a kJ,写出该反应的热化学方程式
(6)若t2时刻后图象变化如-图,则改变条件为


a.恒温恒压下,按照2:1比例充入任意量的B和C
b.恒温恒压下,加入0.24mol A、0.06mol B和0.14mol C
c.恒温恒压下,加入0.12mol A、0.1mol B和0.22mol C
d.恒温恒压下,加入0.14mol B和0.30mol C
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】减少 排放并实现
排放并实现 的有效转化是科研的热点。以下几种为常见的
的有效转化是科研的热点。以下几种为常见的 利用方法,回答下列问题:
利用方法,回答下列问题:
利用 干重整反应不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。该反应一般认为通过如下步骤来实现:
干重整反应不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。该反应一般认为通过如下步骤来实现:
反应iii:主反应
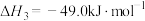
反应iv:副反应
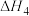
反应iii、iv的平衡常数的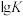 随
随 的变化曲线如图所示:
的变化曲线如图所示:

由图可知,代表反应iii的曲线是___________ (填“ ”或“
”或“ ”),原因是
”),原因是___________ ;升高温度,反应iv的平衡常数
___________ (填“增大”“减小”或“不变”)。
 排放并实现
排放并实现 的有效转化是科研的热点。以下几种为常见的
的有效转化是科研的热点。以下几种为常见的 利用方法,回答下列问题:
利用方法,回答下列问题:利用
 干重整反应不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。该反应一般认为通过如下步骤来实现:
干重整反应不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。该反应一般认为通过如下步骤来实现:反应iii:主反应

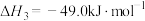
反应iv:副反应

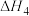
反应iii、iv的平衡常数的
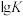 随
随 的变化曲线如图所示:
的变化曲线如图所示:
由图可知,代表反应iii的曲线是
 ”或“
”或“ ”),原因是
”),原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
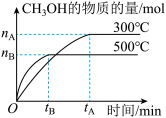
【推荐2】一定条件下,在体积为3L的密闭容器中发生反应CO(g)+2H2(g) CH3OH(g),CH3OH的物质的量与时间变化图象如图:
CH3OH(g),CH3OH的物质的量与时间变化图象如图:
(1)该反应的平衡常数表达式K=__ ;
(2)降低温度,K值将__ (填“增大”、“减小”或“不变”)。
(3)若起始时加入1molCO和2molH2,则达平衡时,CO和H2的转化率之比为__ 。
(4)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是__ (用nB,tB表示)。
(5)判断该可逆反应达到化学平衡状态的标志是__ (填字母,下同)。
a.CO的浓度不再变化
b.混合气体的密度不再改变
c.混合气体的平均摩尔质量不再改变
d.v生成(CH3OH)=v消耗(CO)
(6)300℃时,将容器的容积压缩到原来的 ,在其他条件不变的情况下,对平衡体系产生的影响是
,在其他条件不变的情况下,对平衡体系产生的影响是__ 。
a.CH3OH的物质的量增加
b.正反应速率加快,逆反应速率减慢
c.c(CO)和c(H2)均减小
d.重新平衡时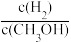 减小
减小
 CH3OH(g),CH3OH的物质的量与时间变化图象如图:
CH3OH(g),CH3OH的物质的量与时间变化图象如图:
(1)该反应的平衡常数表达式K=
(2)降低温度,K值将
(3)若起始时加入1molCO和2molH2,则达平衡时,CO和H2的转化率之比为
(4)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是
(5)判断该可逆反应达到化学平衡状态的标志是
a.CO的浓度不再变化
b.混合气体的密度不再改变
c.混合气体的平均摩尔质量不再改变
d.v生成(CH3OH)=v消耗(CO)
(6)300℃时,将容器的容积压缩到原来的
 ,在其他条件不变的情况下,对平衡体系产生的影响是
,在其他条件不变的情况下,对平衡体系产生的影响是a.CH3OH的物质的量增加
b.正反应速率加快,逆反应速率减慢
c.c(CO)和c(H2)均减小
d.重新平衡时
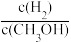 减小
减小
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
(1)表中b_____ c(填“<”、“=”、“>”).
(2)20s时,N2O4的浓度为_____ mol/L,0~20s内N2O4的平均反应速率为_________ .
(3)该反应在80℃时该反应的平衡常数K值为_______ (保留2位小数).
| 时间(s) c(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.20 | a | 0.10 | c | d | e |
| c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)表中b
(2)20s时,N2O4的浓度为
(3)该反应在80℃时该反应的平衡常数K值为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)Ti基态原子的价电子排布式为_________ 。
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。电负性:C___ Ti(填“>”或“<“,下同);第一电离能:N____ O,原因是_________ 。
(3)月球岩石——玄武岩的主要成分为钛酸亚铁(FeTiO3)。FeTiO3与80%的硫酸反应可生成TiOSO4。SO42-的空间构型为___ 形,其中硫原子的杂化方式为_______ ,写出与SO42-互为等电子体的一种分子的化学式:________ 。
(4)Ti的氧化物和CaO相互作用能形成钛酸盐CaTiO3,CaTiO3的晶体结构如图1,Ti位于立方体的体心。该晶体中,Ca2+的配位数为__ 。
(5)Fe能形成多种氧化物,其中FeO晶胞结构如图2。FeO晶胞边长为428pm则FeO晶体的密度为____ g/cm3(阿伏伽德罗常数的值用NA表示,1pm=10-12m,写出计算式即可)。
(1)Ti基态原子的价电子排布式为
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。电负性:C
(3)月球岩石——玄武岩的主要成分为钛酸亚铁(FeTiO3)。FeTiO3与80%的硫酸反应可生成TiOSO4。SO42-的空间构型为
(4)Ti的氧化物和CaO相互作用能形成钛酸盐CaTiO3,CaTiO3的晶体结构如图1,Ti位于立方体的体心。该晶体中,Ca2+的配位数为
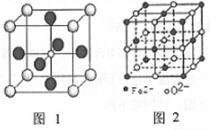
(5)Fe能形成多种氧化物,其中FeO晶胞结构如图2。FeO晶胞边长为428pm则FeO晶体的密度为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】CoP、FeS2、NiS2等物质对电化学氢析出反应有良好的催化活性和稳定性。请回答下列问题:
(1)基态Co原子价层电子的电子排布图(轨道表达式)为________________ ,基态P原子的电子占据最高能级的电子云轮廓图为_______ 。
(2)PH3的沸点_____ (填“高于”或“低于”)NH3,原因是______________ 。
(3)下图为白磷(P4)的晶胞示意图,晶胞的边长为a nm,设阿伏加 德罗常数的数值为NA,其晶体密度的计算表达式为______ g·cm-3。

(1)基态Co原子价层电子的电子排布图(轨道表达式)为
(2)PH3的沸点
(3)下图为白磷(P4)的晶胞示意图,晶胞的边长为a nm,设阿伏加 德罗常数的数值为NA,其晶体密度的计算表达式为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。元素W比元素X序数小5。
(1)X与Y所形成化合物晶体的晶胞如下图所示。
①在1个晶胞中,X离子的数目为_____________ 。
②该化合物的化学式为_______________ 。
③写出元素W的价电子排布式______________ 。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是__________ 。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是_____________ 。
(4)Y与Z可形成YZ42-,YZ42-的空间构型为__________ (用文字描述)。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,该配合物的1个配体中含有σ键的数目为_______ 。
(1)X与Y所形成化合物晶体的晶胞如下图所示。
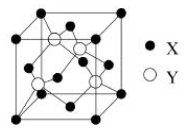
①在1个晶胞中,X离子的数目为
②该化合物的化学式为
③写出元素W的价电子排布式
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是
(4)Y与Z可形成YZ42-,YZ42-的空间构型为
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,该配合物的1个配体中含有σ键的数目为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】按要求填空:
(1)原子序数为24的元素原子中有___________ 个电子层,___________ 个能级,_________ 个未成对电子,位于元素周期表的___________ 区。
(2)在下列物质中:①N2、②H2O、③NaOH、④MgCl2、⑤C2H4、⑥Na2O2(用序号填空)
其中只含有非极性键的是___________ ;只含有极性键的是___________ ;只含有离子键的是___________ ;既含有非极性键又含有极性键的是___________ ;含有非极性键的离子化合物是___________ 。
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的___________ 键更稳定(填“σ”或“π”)。
(1)原子序数为24的元素原子中有
(2)在下列物质中:①N2、②H2O、③NaOH、④MgCl2、⑤C2H4、⑥Na2O2(用序号填空)
其中只含有非极性键的是
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】(1)下面列出了几组物质,请将正确的序号填写在空格上。
同位素__________ ,同系物__________ ,同素异形体__________ ,同分异构体__________ 。
①金刚石与“足球烯” ;②
;② 与
与 ; ③氧气
; ③氧气 与臭氧
与臭氧 ;④
;④  和
和 ;⑤
;⑤ 和CH3CH2CH2CH2CH3;⑥
和CH3CH2CH2CH2CH3;⑥ 和CH3CH2CH2CH2CH3
和CH3CH2CH2CH2CH3
请用下列几种物质的序号填空:
①Ar ②CO2 ③Na2O2 ④KOH ⑤MgBr2 ⑥NH4Cl ⑦H2SO4
只存在共价键的是__________ ,只存在离子键的是______________ ,既存在离子键又存在极性共价键的是____________ ,既存在离子键又存在非极性共价键的是___________ 。
(3)已知一定条件下,金刚石转化为石墨释放出能量,则等质量的金刚石比石墨具有的能量____ (填“高”、“低”),故金刚石比石墨稳定性_____ (填“强”、“弱”),等质量的金刚石和石墨充分燃烧均生成二氧化碳,______ 放出热量多
同位素
①金刚石与“足球烯”
 ;②
;② 与
与 ; ③氧气
; ③氧气 与臭氧
与臭氧 ;④
;④  和
和 ;⑤
;⑤ 和CH3CH2CH2CH2CH3;⑥
和CH3CH2CH2CH2CH3;⑥ 和CH3CH2CH2CH2CH3
和CH3CH2CH2CH2CH3请用下列几种物质的序号填空:
①Ar ②CO2 ③Na2O2 ④KOH ⑤MgBr2 ⑥NH4Cl ⑦H2SO4
只存在共价键的是
(3)已知一定条件下,金刚石转化为石墨释放出能量,则等质量的金刚石比石墨具有的能量
您最近一年使用:0次
【推荐3】用丙酮为原料来合成化合物B的路线如图(其中部分产物未列出):_______ 。
(2)中间产物A可经还原直接得到对应相同碳骨架的烷烃,请写出得到的该烷烃的分子式_______ ,用系统命名法命名该烷烃:_______ 。
(3)写出化合物B与氢氧化钠的水溶液共热的化学方程式:_______ 。
(4)丙酮可发生自身羟醛缩合,研究表明该反应机理为,碱性条件下丙酮失去1个 形成阴离子,再和另一分子丙酮发生加成反应。请解释丙酮具有一定的酸性(
形成阴离子,再和另一分子丙酮发生加成反应。请解释丙酮具有一定的酸性(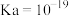 )的理由
)的理由_______ 。
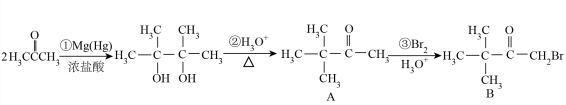
(2)中间产物A可经还原直接得到对应相同碳骨架的烷烃,请写出得到的该烷烃的分子式
(3)写出化合物B与氢氧化钠的水溶液共热的化学方程式:
(4)丙酮可发生自身羟醛缩合,研究表明该反应机理为,碱性条件下丙酮失去1个
 形成阴离子,再和另一分子丙酮发生加成反应。请解释丙酮具有一定的酸性(
形成阴离子,再和另一分子丙酮发生加成反应。请解释丙酮具有一定的酸性(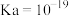 )的理由
)的理由
您最近一年使用:0次



