钛铁矿是铁和钛的氧化物矿物,成分可表示为FeTiO3 (Ti为+4价)。钛白粉(TiO2)涂料、塑料、油墨、造纸行业具有广泛的用途,制备流程如图:
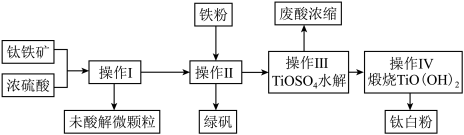
(1)钛铁矿与硫酸反应时可表示为FeTiO3+H2SO4→TiOSO4+X+H2O,其中X的化学式为______ ,该反应为______ (填“氧化还原反应”或“非氧化还原反应”)。
(2)某钛铁矿中FeTiO3的含量为76%,该钛铁矿与硫酸反应时Ti转化率为92%,操作I到操作IV的过程中Ti的转化率为96%,则1t该钛铁矿可生产钛白粉______ t (所有计算结果保留两位有效数字),能否计算绿矾的产量______ ?(若能则计算数值,否则说明理由)。
(3)操作I的名称是______ ,操作II包括搅拌、结晶、______ ,操作II中加入铁粉的目的是______ (用离子方程式表示)。
(4)写出操作III中TiOSO4水解的化学方程式:______ 。
(5)该生产过程中产生的尾气SO2、SO3的处理方法是______ 。

(1)钛铁矿与硫酸反应时可表示为FeTiO3+H2SO4→TiOSO4+X+H2O,其中X的化学式为
(2)某钛铁矿中FeTiO3的含量为76%,该钛铁矿与硫酸反应时Ti转化率为92%,操作I到操作IV的过程中Ti的转化率为96%,则1t该钛铁矿可生产钛白粉
(3)操作I的名称是
(4)写出操作III中TiOSO4水解的化学方程式:
(5)该生产过程中产生的尾气SO2、SO3的处理方法是
更新时间:2020-01-09 16:08:18
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】三硫代碳酸钠(Na2CS3)又名全硫碳酸钠,常温下是一种玫瑰红色针状物质。在农业上常用作杀菌剂、杀虫剂。某小组欲测定三硫代碳酸钠样品的纯度,实验如下:
【实验一】配制Na2CS3溶液
取10.00g Na2CS3固体样品配制成250mL溶液
(1)上述溶液配制过程中不可能用到的仪器是______ (填字母)。

【实验二】测定Na2CS3样品纯度
实验装置如下图所示,取上述Na2CS3溶液100mL于圆底烧瓶中,滴加足量2.0mol/L稀H2SO4,充分反应,关闭活塞。待反应结束后打开止水夹k,通入一段时间N2。

已知:①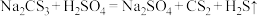 。
。
②CS2是不溶于水、比水重、易挥发(沸点为46℃)的无色液体;CS2与CO2某些性质相似,与NaOH溶液反应生成Na2CS3和H2O。
实验小组设计如下两种实验方案测定Na2CS3样品纯度
方案1:通过测定B中产生沉淀的质量,计算样品纯度
(2)B中发生反应的离子方程式_______ 。
(3)将B中产生的沉淀过滤、洗涤、干燥、称重得2.40g固体。样品的纯度为________ 。
方案2:通过装置C的增重,计算样品纯度
(4)反应结束后,通入的N2最好是60℃左右的热N2,其目的是______ 。
(5)该方案测得的Na2CS3样品纯度____ (填“偏高”或“偏低”),分析原因,写出你对装置的改进建议_____ 。
【实验一】配制Na2CS3溶液
取10.00g Na2CS3固体样品配制成250mL溶液
(1)上述溶液配制过程中不可能用到的仪器是

【实验二】测定Na2CS3样品纯度
实验装置如下图所示,取上述Na2CS3溶液100mL于圆底烧瓶中,滴加足量2.0mol/L稀H2SO4,充分反应,关闭活塞。待反应结束后打开止水夹k,通入一段时间N2。

已知:①
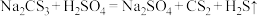 。
。②CS2是不溶于水、比水重、易挥发(沸点为46℃)的无色液体;CS2与CO2某些性质相似,与NaOH溶液反应生成Na2CS3和H2O。
实验小组设计如下两种实验方案测定Na2CS3样品纯度
方案1:通过测定B中产生沉淀的质量,计算样品纯度
(2)B中发生反应的离子方程式
(3)将B中产生的沉淀过滤、洗涤、干燥、称重得2.40g固体。样品的纯度为
方案2:通过装置C的增重,计算样品纯度
(4)反应结束后,通入的N2最好是60℃左右的热N2,其目的是
(5)该方案测得的Na2CS3样品纯度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】 与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以
与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以 分别与
分别与 溶液和
溶液和 溶液反应为原理,制备
溶液反应为原理,制备 和
和 ,并探究
,并探究 和
和 的部分性质。回答下列问题:
的部分性质。回答下列问题:
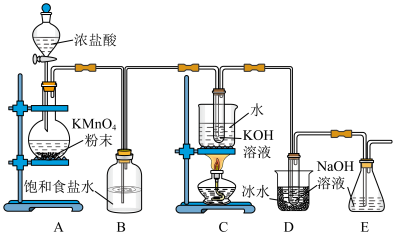
(1)盛放浓盐酸的仪器名称是___________ 。
(2)A装置中发生反应的离子方程式为___________ 。
(3)C装置中采用的加热方式的名称为___________ 。
(4)取少量 、
、 装置中生成的
装置中生成的 和
和 溶液(两溶液均调至碱性)。分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液,1号试管溶液颜色不变,2号试管溶液颜色变为棕色,经检验有
溶液(两溶液均调至碱性)。分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液,1号试管溶液颜色不变,2号试管溶液颜色变为棕色,经检验有 生成,由此可推知,在碱性条件下,
生成,由此可推知,在碱性条件下, 的氧化能力
的氧化能力___________ (填“>”或“<”) 的氧化能力。
的氧化能力。
(5)该兴趣小组在 条件下,将一定量的
条件下,将一定量的 通入
通入 溶液中,
溶液中, 恰好反应完全,得到的产物中含有
恰好反应完全,得到的产物中含有 、
、 和
和 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为___________ mol。
 与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以
与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以 分别与
分别与 溶液和
溶液和 溶液反应为原理,制备
溶液反应为原理,制备 和
和 ,并探究
,并探究 和
和 的部分性质。回答下列问题:
的部分性质。回答下列问题:
(1)盛放浓盐酸的仪器名称是
(2)A装置中发生反应的离子方程式为
(3)C装置中采用的加热方式的名称为
(4)取少量
 、
、 装置中生成的
装置中生成的 和
和 溶液(两溶液均调至碱性)。分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液,1号试管溶液颜色不变,2号试管溶液颜色变为棕色,经检验有
溶液(两溶液均调至碱性)。分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液,1号试管溶液颜色不变,2号试管溶液颜色变为棕色,经检验有 生成,由此可推知,在碱性条件下,
生成,由此可推知,在碱性条件下, 的氧化能力
的氧化能力 的氧化能力。
的氧化能力。(5)该兴趣小组在
 条件下,将一定量的
条件下,将一定量的 通入
通入 溶液中,
溶液中, 恰好反应完全,得到的产物中含有
恰好反应完全,得到的产物中含有 、
、 和
和 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】醋酸铟是一种化工产品,以ITO靶材废料(主要由 、
、 组成)为原料制备醋酸铟的流程如下:
组成)为原料制备醋酸铟的流程如下:
(1)已知 和
和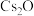 可反应生成偏铟酸铯(CsInO2),也可以与
可反应生成偏铟酸铯(CsInO2),也可以与 反应生成
反应生成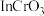 ,据此判断
,据此判断 属于
属于___________ (填“酸性氧化物”“碱性氧化物”或“两性氧化物”)。写出 与
与 反应的离子方程式:
反应的离子方程式:___________ 。
(2)酸浸时,铟的浸出率在不同温度和硫酸浓度下的数值如下表,锡的浸出率小于20%。
由上表信息可得出规律:其他条件不变时,铟的浸出率随温度升高而___________ (填“增大”“减小”或“不变”,下同),温度越高,硫酸浓度对铟的浸出率影响___________ 。
(3)酸溶时无气泡产生,则酸溶时发生反应的化学方程式为___________ 。
(4)现有一份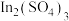 和
和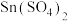 的混合溶液,向其中逐渐加入锌粉,测得析出固体的质量随加入锌粉的物质的量的关系如图所示。图中ab段反应的离子方程式为
的混合溶液,向其中逐渐加入锌粉,测得析出固体的质量随加入锌粉的物质的量的关系如图所示。图中ab段反应的离子方程式为___________ ,该混合溶液中,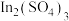 和
和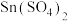 的物质的量浓度之比为
的物质的量浓度之比为___________ 。
 、
、 组成)为原料制备醋酸铟的流程如下:
组成)为原料制备醋酸铟的流程如下: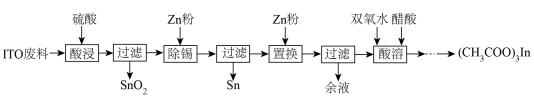
(1)已知
 和
和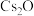 可反应生成偏铟酸铯(CsInO2),也可以与
可反应生成偏铟酸铯(CsInO2),也可以与 反应生成
反应生成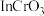 ,据此判断
,据此判断 属于
属于 与
与 反应的离子方程式:
反应的离子方程式:(2)酸浸时,铟的浸出率在不同温度和硫酸浓度下的数值如下表,锡的浸出率小于20%。
| 温度 | 30℃ | 50℃ | 70℃ | 90℃ |
 的 的 溶液 溶液 | 56% | 72% | 83% | 91% |
 的 的 溶液 溶液 | 68% | 81% | 89% | 94% |
(3)酸溶时无气泡产生,则酸溶时发生反应的化学方程式为
(4)现有一份
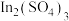 和
和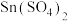 的混合溶液,向其中逐渐加入锌粉,测得析出固体的质量随加入锌粉的物质的量的关系如图所示。图中ab段反应的离子方程式为
的混合溶液,向其中逐渐加入锌粉,测得析出固体的质量随加入锌粉的物质的量的关系如图所示。图中ab段反应的离子方程式为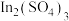 和
和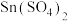 的物质的量浓度之比为
的物质的量浓度之比为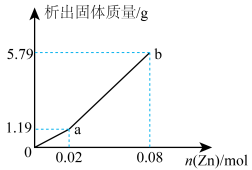
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。制备高铁酸钠的反应原理为:
)是一种新型绿色消毒剂,主要用于饮用水处理。制备高铁酸钠的反应原理为: 。某化学兴趣小组用废铁屑(主要成分为Fe,杂质有Al、C)制备高铁酸钠的主要流程如下。
。某化学兴趣小组用废铁屑(主要成分为Fe,杂质有Al、C)制备高铁酸钠的主要流程如下。___________ , 中铁的化合价为
中铁的化合价为___________ 。
(2)“碱浸”过程中发生的离子反应方程式为___________ 。
(3)“酸浸”时适当升温的目的是___________ 。
(4)“滤渣”的主要成分为___________ 。
(5)“操作I”中通入空气的目的是___________ 。
(6)常温下,加入NaOH溶液调节溶液
___________ 时,溶液中 mol/L(已知:常温下,
mol/L(已知:常温下, 的溶度积常数为
的溶度积常数为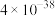 )。
)。
 )是一种新型绿色消毒剂,主要用于饮用水处理。制备高铁酸钠的反应原理为:
)是一种新型绿色消毒剂,主要用于饮用水处理。制备高铁酸钠的反应原理为: 。某化学兴趣小组用废铁屑(主要成分为Fe,杂质有Al、C)制备高铁酸钠的主要流程如下。
。某化学兴趣小组用废铁屑(主要成分为Fe,杂质有Al、C)制备高铁酸钠的主要流程如下。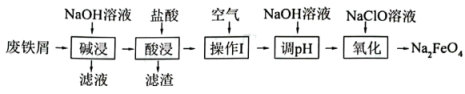
 中铁的化合价为
中铁的化合价为(2)“碱浸”过程中发生的离子反应方程式为
(3)“酸浸”时适当升温的目的是
(4)“滤渣”的主要成分为
(5)“操作I”中通入空气的目的是
(6)常温下,加入NaOH溶液调节溶液

 mol/L(已知:常温下,
mol/L(已知:常温下, 的溶度积常数为
的溶度积常数为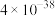 )。
)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】高纯碳酸锰(MnCO3)广泛应用于电子工业,是制造高性能磁性材料的主要原料。工业上以软锰矿(主要成分是MnO2、含有少量的Fe3O4、Al2O3、SiO2)为主要原料制备高纯碳酸锰的工艺流程如图所示:
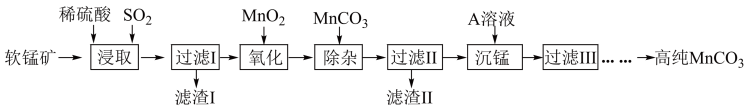
已知:①Ksp(MnCO3)=2.2×10-11。
②碳酸锰难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解。
(1)为了加快浸取速率,可以采取的措施是_______ (写两条即可),浸取过程中MnO2发生反应的离子方程式为_______ 。
(2)滤渣Ⅱ的主要成分是_______ 。
(3)沉锰过程中,A溶液可以选用NH4HCO3溶液或(NH4)2CO3溶液。
①若是选用NH4HCO3溶液,则反应的离子方程式为:_______ 。
②若是选用(NH4)2CO3溶液。取过滤Ⅱ的滤液100mL,其中c(Mn2+)=2.0mol/L,加入等体积的(NH4)2CO3溶液。如果使“沉锰”后的溶液中c(Mn2+)=1.0×10-10mol/L,则加入的c((NH4)2CO3)=_______ mol/L。
(4)为了得到高纯碳酸锰,在过滤Ⅲ操作后,最好选择用乙醇洗去表面的杂质。选择用乙醇洗涤的原因是_______ 。
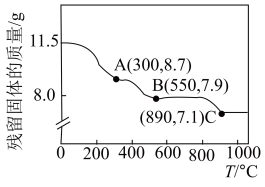
(5)在空气中加热所得MnCO3固体(不含其他杂质),随着温度的升高,残留固体的质量如图所示。则B点的成分为_______ (填化学式)。

已知:①Ksp(MnCO3)=2.2×10-11。
②碳酸锰难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解。
(1)为了加快浸取速率,可以采取的措施是
(2)滤渣Ⅱ的主要成分是
(3)沉锰过程中,A溶液可以选用NH4HCO3溶液或(NH4)2CO3溶液。
①若是选用NH4HCO3溶液,则反应的离子方程式为:
②若是选用(NH4)2CO3溶液。取过滤Ⅱ的滤液100mL,其中c(Mn2+)=2.0mol/L,加入等体积的(NH4)2CO3溶液。如果使“沉锰”后的溶液中c(Mn2+)=1.0×10-10mol/L,则加入的c((NH4)2CO3)=
(4)为了得到高纯碳酸锰,在过滤Ⅲ操作后,最好选择用乙醇洗去表面的杂质。选择用乙醇洗涤的原因是
(5)在空气中加热所得MnCO3固体(不含其他杂质),随着温度的升高,残留固体的质量如图所示。则B点的成分为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学小组制备SO2 ( Na2SO3+H2SO4= Na2SO4+SO2 ↑+H2O),并验证SO2的部分性质,装置如图 (部分夹持装置省略)所示。

几回答下列问题:
(1)仪器a的名称为___________ 。
(2)体现SO2氧化性的实验现象是___________ ;证明SO2具有漂白性的现象是___________ 。
(3)C中反应的离子方程式为___________ 。
(4)实验观察到E装置试剂瓶内有白色沉淀生成,反应的离子方程式为___________ ;b中的试剂为___________ ;反应结束后通入N2的目的是___________ 。

几回答下列问题:
(1)仪器a的名称为
(2)体现SO2氧化性的实验现象是
(3)C中反应的离子方程式为
(4)实验观察到E装置试剂瓶内有白色沉淀生成,反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是___ 。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是______________ 。
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
(3)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:

回答下列问题:
①操作Ⅰ的名称是____ ,操作Ⅱ的名称是____ 。②写出在空气中煅烧FeCO3的化学方程式________________ 。
(4)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定。
a.称取2.850 g绿矾(FeSO4·7H2O)产品,溶解,在250 mL容量瓶中定容;
b.量取25.00 mL待测溶液放入锥形瓶中;
c.用硫酸酸化的0.01000 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00 mL。
①达到滴定终点时的现象____ 。
②某同学设计的下列滴定方式,最合理的是____ 。(夹持部分略去)(填字母序号)

③计算上述样品中FeSO4·7H2O的质量分数为____ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
(3)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:

回答下列问题:
①操作Ⅰ的名称是
(4)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定。
a.称取2.850 g绿矾(FeSO4·7H2O)产品,溶解,在250 mL容量瓶中定容;
b.量取25.00 mL待测溶液放入锥形瓶中;
c.用硫酸酸化的0.01000 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00 mL。
①达到滴定终点时的现象
②某同学设计的下列滴定方式,最合理的是

③计算上述样品中FeSO4·7H2O的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某酸性废腐蚀液含有大量 、
、 、
、 ,任意排放会造成环境污染及资源的浪费。以废腐蚀液为原料,回收铜并将铁的化合物全部转化为
,任意排放会造成环境污染及资源的浪费。以废腐蚀液为原料,回收铜并将铁的化合物全部转化为 溶液。测得某酸性废腐蚀液中含
溶液。测得某酸性废腐蚀液中含 、
、 、
、 、HCl。取该酸性废腐蚀液200mL,按如下流程在实验室进行实验:
、HCl。取该酸性废腐蚀液200mL,按如下流程在实验室进行实验:

(1)腐蚀液中加入过量Fe粉,发生反应的离子方程式除 外,还有(任写一个):
外,还有(任写一个):_______ 。
(2)由滤渣得到铜,除杂所需试剂是_______ 。
(3)写出 溶液中通入
溶液中通入 ,发生反应的离子方程式:
,发生反应的离子方程式:_______ 。
(4)实验室用固体 与浓HCl反应制备
与浓HCl反应制备 的化学方程式为:
的化学方程式为: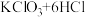 (浓)
(浓)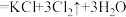 ,上述反应产生0.3 mol
,上述反应产生0.3 mol  ,则转移的电子数为
,则转移的电子数为_______ (设NA表示阿伏加德罗常数的值)。
 、
、 、
、 ,任意排放会造成环境污染及资源的浪费。以废腐蚀液为原料,回收铜并将铁的化合物全部转化为
,任意排放会造成环境污染及资源的浪费。以废腐蚀液为原料,回收铜并将铁的化合物全部转化为 溶液。测得某酸性废腐蚀液中含
溶液。测得某酸性废腐蚀液中含 、
、 、
、 、HCl。取该酸性废腐蚀液200mL,按如下流程在实验室进行实验:
、HCl。取该酸性废腐蚀液200mL,按如下流程在实验室进行实验:
(1)腐蚀液中加入过量Fe粉,发生反应的离子方程式除
 外,还有(任写一个):
外,还有(任写一个):(2)由滤渣得到铜,除杂所需试剂是
(3)写出
 溶液中通入
溶液中通入 ,发生反应的离子方程式:
,发生反应的离子方程式:(4)实验室用固体
 与浓HCl反应制备
与浓HCl反应制备 的化学方程式为:
的化学方程式为: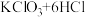 (浓)
(浓)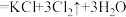 ,上述反应产生0.3 mol
,上述反应产生0.3 mol  ,则转移的电子数为
,则转移的电子数为
您最近一年使用:0次
【推荐3】铬铁矿的主要成分可表示为FeO•Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:
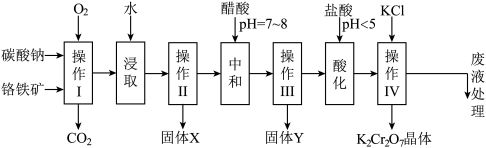
已知:
①4FeO•Cr2O3+8Na2CO3+7O2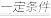 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3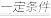 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
根据题意回答下列问题:
(1)操作I在常温下该反应速度极慢,下列措施中能使反应速率增大的是______ .
A.升高温度 B.通入过量的空气 C.将原料粉碎 D.增加纯碱的用量
(2)固体X中主要含有______ (填写化学式);
(3)酸化步骤用盐酸调节溶液pH<5,并煮沸其目的是______ .(离子方程式表示)
(4)操作 iv有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、______ 、______ 、洗涤、干燥.
(5)表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.
该反应在溶液中能发生的理由是______ .(文字说明)
(6)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量______ (填写试剂)、溶解、过滤、再______ (填写试剂)、…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为______ (用含m、n的代数式表示).

已知:
①4FeO•Cr2O3+8Na2CO3+7O2
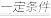 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;②Na2CO3+Al2O3
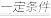 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;根据题意回答下列问题:
(1)操作I在常温下该反应速度极慢,下列措施中能使反应速率增大的是
A.升高温度 B.通入过量的空气 C.将原料粉碎 D.增加纯碱的用量
(2)固体X中主要含有
(3)酸化步骤用盐酸调节溶液pH<5,并煮沸其目的是
(4)操作 iv有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、
(5)表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.
该反应在溶液中能发生的理由是
| 物质 | 溶解度/(g/100g水) | ||||
| 0°C | 40°C | 80°C | |||
| KCl | 28 | 40.1 | 51.3 | ||
| NaCl | 35.7 | 36.4 | 38 | ||
| K2Cr2O7 | 4.7 | 26.3 | 73 | ||
| Na2Cr2O7 | 163 | 215 | 376 | ||
(6)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铜是人类最早使用的金属,在生产生活中应用及其广泛。工业上以黄铜矿 (主要成分FeCuS2)为原料制取金属铜,其主要工艺流程如图所示。

已知:反应II的离子方程式:Cu2++CuS+4Cl-=2[CuCl2]-+S
回答下列问题:
(1)FeCuS2中S的化合价____ 。
(2)反应I在隔绝空气、高温煅烧条件下进行,写出化学方程式____ 。
(3)为了反应I充分进行,工业上可采取的措施是____ 。
(4)反应III的离子方程式为____ 。
(5)向反应III后的溶液中加入稀硫酸的目的是____ 。
(6)该流程中,可循环利用的物质除CuCl2外,还有___ (填化学式)。
(7)反应IV中,处理尾气SO2的方法,合理的是_____
A.高空排放
B.用BaCl2溶液吸收制备BaSO3
C.用氨水吸收后,再经氧化,制备(NH4)2SO4
D.用纯碱溶液吸收可生成Na2SO3(H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11;H2SO3:Ka1=1.2×102,Ka2=5.6×108)
(8)CuCl悬浊液中加入Na2S,发生的反应为2CuCl(s)+S2-(aq) Cu2S(s)+2Cl-(aq)
Cu2S(s)+2Cl-(aq)
该反应的平衡常数K=___ [已知Ksp(CuCl)=a,Ksp(Cu2S)=b]

已知:反应II的离子方程式:Cu2++CuS+4Cl-=2[CuCl2]-+S
回答下列问题:
(1)FeCuS2中S的化合价
(2)反应I在隔绝空气、高温煅烧条件下进行,写出化学方程式
(3)为了反应I充分进行,工业上可采取的措施是
(4)反应III的离子方程式为
(5)向反应III后的溶液中加入稀硫酸的目的是
(6)该流程中,可循环利用的物质除CuCl2外,还有
(7)反应IV中,处理尾气SO2的方法,合理的是
A.高空排放
B.用BaCl2溶液吸收制备BaSO3
C.用氨水吸收后,再经氧化,制备(NH4)2SO4
D.用纯碱溶液吸收可生成Na2SO3(H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11;H2SO3:Ka1=1.2×102,Ka2=5.6×108)
(8)CuCl悬浊液中加入Na2S,发生的反应为2CuCl(s)+S2-(aq)
 Cu2S(s)+2Cl-(aq)
Cu2S(s)+2Cl-(aq)该反应的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】NiSO4·nH2O易溶于水,难溶于乙醇,其水溶液显酸性。由一种废料(主要成分是铁镍合金,还含有铜、镁等金属氧化物及SiO2)为原科制取NiSO4·nH2O步骤如图:

(1)“酸溶”步骤中加入H2O2的目的是_______ 。
(2)为了不引入杂质离子,试剂X可以选择_______ 。“除铜” 步骤反应的离子方程式是_______ 。
(3)向“除铜”后的滤液中加入NaF溶液、使Mg2+转化为MgF2沉淀除去,若溶液的pH值偏低,将会导致MgF2沉淀不完全,其原因是_______ 。若“除铜”后的滤液中c(Mg2+)=1.0×10-3mol·L-1,当除镁率达到99%时,溶液中c(F-)=_______ mol/L。[已知Ksp(MgF2)=4.0×10-11)]
(4)其他的离子杂质可以通过“萃取”和“反萃取”的步骤除去,“萃取”的原理为Ni2++2RH NiR2 +2H+,“反萃取”时需加入的试剂Y为
NiR2 +2H+,“反萃取”时需加入的试剂Y为_______ ,分离有机相和水相的操作的名称为_______ 。
(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH。该反应的化学方程式为_______ 。
(6)采用热重分析法测定NiSO4·nH2O样品所含结晶水数,将样品在900°C下进行煅烧,失重率随时间变化如图,A点时失掉2个结晶水,n的值为_______ ,C 点产物的化学式为_______ 。


(1)“酸溶”步骤中加入H2O2的目的是
(2)为了不引入杂质离子,试剂X可以选择
(3)向“除铜”后的滤液中加入NaF溶液、使Mg2+转化为MgF2沉淀除去,若溶液的pH值偏低,将会导致MgF2沉淀不完全,其原因是
(4)其他的离子杂质可以通过“萃取”和“反萃取”的步骤除去,“萃取”的原理为Ni2++2RH
 NiR2 +2H+,“反萃取”时需加入的试剂Y为
NiR2 +2H+,“反萃取”时需加入的试剂Y为(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH。该反应的化学方程式为
(6)采用热重分析法测定NiSO4·nH2O样品所含结晶水数,将样品在900°C下进行煅烧,失重率随时间变化如图,A点时失掉2个结晶水,n的值为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】焦亚硫酸钠(Na2S2O5)是生产、生活中重要的物质,受热易分解,实验室制备Na2S2O5的实验流程如下:
H2SO4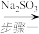 SO2
SO2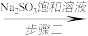 Na2S2O5溶液
Na2S2O5溶液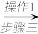 Na2S2O5晶体
Na2S2O5晶体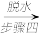 Na2S2O5
Na2S2O5
(1)步骤一中一般用70%的H2SO4,H2SO4浓度过小或过大均不利于SO2的逸出,原因是_______ 。
(2)步骤二的实验装置如图:

①三颈烧瓶中发生反应的化学方程式为_________ 。
②处理尾气,选用的最合理的装置(夹持装置已略去)为_______ (填标号)。

(3)“操作1”包括的操作有低温蒸发、结晶、____ 、洗涤。洗涤时先用饱和SO2水溶液,再用无水乙醇,用饱和SO2水溶液、无水乙醇洗涤产品的共同优点是____ ,用无水乙醇洗涤的另外一个优点是_____ 。
(4)“步骤四”脱水需在N2的气氛中低温烘干,原因是______ 。
(5)用酸性KMnO4溶液______ (填“能”或“不能”)鉴别出产品Na2S2O5中含有Na2SO4。
(6)产品纯度检验:取1.0 g Na2S2O5产品溶于水配成100 mL溶液,取上述配好的溶液25.00 mL,用0.1 mol·L-1的碘标准液滴定至终点,消耗24.00 mL碘标准液,该样品中Na2S2O5的纯度为_____ 。(其他杂质不参与反应)
H2SO4
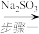 SO2
SO2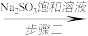 Na2S2O5溶液
Na2S2O5溶液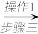 Na2S2O5晶体
Na2S2O5晶体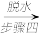 Na2S2O5
Na2S2O5(1)步骤一中一般用70%的H2SO4,H2SO4浓度过小或过大均不利于SO2的逸出,原因是
(2)步骤二的实验装置如图:

①三颈烧瓶中发生反应的化学方程式为
②处理尾气,选用的最合理的装置(夹持装置已略去)为

(3)“操作1”包括的操作有低温蒸发、结晶、
(4)“步骤四”脱水需在N2的气氛中低温烘干,原因是
(5)用酸性KMnO4溶液
(6)产品纯度检验:取1.0 g Na2S2O5产品溶于水配成100 mL溶液,取上述配好的溶液25.00 mL,用0.1 mol·L-1的碘标准液滴定至终点,消耗24.00 mL碘标准液,该样品中Na2S2O5的纯度为
您最近一年使用:0次



