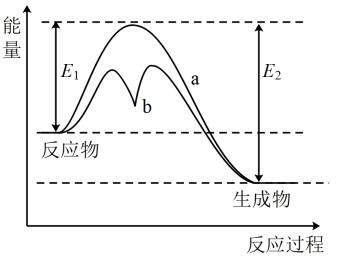
常压下羰基化法精炼镍的原理为:Ni(s) + 4CO(g) Ni(CO)4(g),下列判断正确的是
Ni(CO)4(g),下列判断正确的是
 Ni(CO)4(g),下列判断正确的是
Ni(CO)4(g),下列判断正确的是| A.增加Ni的用量,可加快该反应速率 |
| B.该反应达到平衡时,4v生成[Ni(CO)4]=v生成(CO) |
| C.减压,平衡逆向移动,反应的平衡常数减小 |
| D.选择合适的催化剂可提高CO转化率 |
19-20高二上·河北唐山·期末 查看更多[8]
更新时间:2020-01-20 21:53:52
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列事实,不能用勒夏特列原理解释的是
A.合成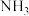 反应,为提高 反应,为提高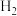 的转化率,理论上应采取相对较高压强的措施 的转化率,理论上应采取相对较高压强的措施 |
B.低温比高温有利于合成 |
C.对于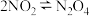 ,达平衡后增大压强可使气体颜色变深 ,达平衡后增大压强可使气体颜色变深 |
D.溴水中有平衡: ,加入NaOH溶液后,溶液颜色变浅 ,加入NaOH溶液后,溶液颜色变浅 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在合成氨工业中,原料气循环使用主要是为了
| A.增大反应速率 | B.提高 N2和 H2的利用率 |
| C.降低氨的沸点 | D.提高平衡混合物中氨的含量 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知:2NO(g)+O2(g)  2NO2(g),其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图),下列说法
2NO2(g),其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图),下列说法不正确 的是

 2NO2(g),其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图),下列说法
2NO2(g),其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图),下列说法
| A.p1<p2 |
| B.该反应的△H<0 |
| C.A、B两点的平衡常数:K(A)=K(B) |
| D.其它条件不变,通入一定量的NO,可使A点到B点 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法不正确的是
| A.平衡移动,平衡常数不一定改变;平衡常数改变,平衡一定移动 |
| B.化学平衡正向移动,正反应速率不一定增大 |
| C.对达到平衡的一个放热的可逆反应,若降低温度正反应速率减小,逆反应速率增大 |
| D.参加反应物质的性质是决定化学反应速率的主要因素 |
您最近半年使用:0次

 ,10min后达到平衡状态。下列说法
,10min后达到平衡状态。下列说法