21. Ⅰ.随着氮氧化物对环境及人类活动影响的日趋严重,如何消除大气污染物中的氮氧化物成为人们关注的主要问题之一,利用 NH
3的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:4NH
3(g)+6NO(g)

5N
2(g)+6H
2O(l) -Q
(1)一定温度下,在恒容密闭容器中按照 n(NH
3)︰n(NO) =2︰3 充入反应物,发生上述反应。下列不能判断该反应达到平衡状态的是
___________。
A.c(NH
3)︰c(NO) =2︰3
B.n(NH
3)︰n(N
2) 不变
C.容器内压强不变
D.容器内混合气体的密度不变
E.1molN—H 键断裂的同时,生成 1molO—H 键
(2)某研究小组将 2molNH
3、3molNO 和一定量的O
2充入 2L 密闭容器中,在 Ag
2O 催化剂表面发生上述反应,NO 的转化率随温度变化的情况如图所示。
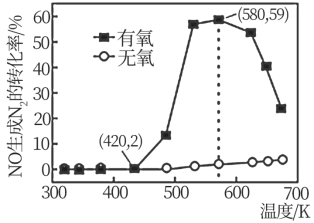
①在 5min 内,温度从 420K 升高到 580K,此时段内NO 的平均反应速率

(NO)=
___________;
②在有氧条件下,温度 580K 之后 NO 生成 N
2的转化率降低的原因可能是
___________。
Ⅱ. 用尿素[(NH
2)
2CO]水溶液吸收氮氧化物也是一种可行的方法。NO 和 NO
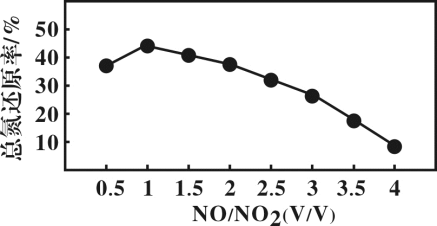
2不同配比混合气通入尿素溶液中,总氮还原率与配比关系如下图。
(1)用尿素[(NH
2)
2CO]水溶液吸收体积比为 1∶1的NO 和 NO
2混合气,可将 N 元素转变为对环境无害的气体。写出该反应的化学方程式
___________。
(2)随着 NO 和 NO
2配比的提高,总氮还原率降低的主要原因是
___________。