H2CO3 Ka1=4.3×10-7 Ka2=5.61×10-11 HClO Ka=2.95×10-8 ,下列实验不能达到目的的是
| 选项 | 目的 | 实验 |
| A | 制取较高浓度的次氯酸溶液 | 将Cl2通入碳酸钠溶液中 |
| B | 加快氧气的生成速率 | 在过氧化氢溶液中加入少量MnO2 |
| C | 除去乙酸乙酯中的少量乙酸 | 加入饱和碳酸钠溶液洗涤、分液 |
| D | 制备少量二氧化硫气体 | 向饱和亚硫酸钠溶液中滴加浓硫酸 |
| A.A | B.B | C.C | D.D |
19-20高三上·福建莆田·期末 查看更多[2]
更新时间:2020/01/23 21:01:17
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列关于Cu和浓硫酸制备SO2反应的实验原理或操作能达到实验目的的是


| A.用装置甲制取并收集SO2 |
| B.用装置乙验证二氧化硫的漂白性 |
| C.用装置丙过滤出稀释后混合物中的不溶物 |
D.用装置丁测定反应后溶液中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知反应:2NaIO3+5SO2+4H2O=I2+3H2SO4+2NaHSO4,利用下列装置从含NaIO3的废液中得到I2的苯溶液并回收NaHSO4。其中装置正确且能达到相应实验目的的是( )
A.制取SO2 |
B.还原IO3- |
C.放出I2的苯溶液 |
D.从水溶液中提取NaHSO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
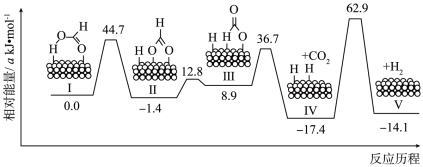
【推荐1】控制光沉积构建光催化材料,人工模拟光合作用,可实现 、
、 与有机物的转化,转化过程的反应机理如图所示。下列说法中正确的是
与有机物的转化,转化过程的反应机理如图所示。下列说法中正确的是
 、
、 与有机物的转化,转化过程的反应机理如图所示。下列说法中正确的是
与有机物的转化,转化过程的反应机理如图所示。下列说法中正确的是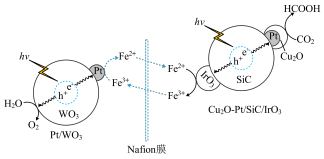
A.转化过程中的电子转移只发生在 与 与 之间 之间 |
B.转化过程中 在催化剂表面发生还原反应 在催化剂表面发生还原反应 |
C. 转化的反应为 转化的反应为 |
D.该转化过程应用了 的还原性与 的还原性与 的氧化性 的氧化性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关说法正确的是
| A.化学平衡发生移动,平衡常数必发生变化 |
| B.加入催化剂,单位体积内反应物分子中活化分子百分数不变 |
| C.人们把能够发生有效碰撞的分子叫活化分子,把活化分子具有的能量叫活化能 |
| D.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,若将含0.5 molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
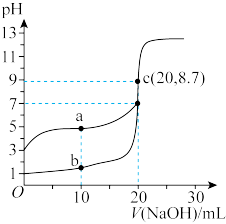
【推荐1】25℃时,用HCl气体调节0.1 mol/L氨水的pH,溶液中微粒浓度的对数值(1gc)、反应物的物质的量之比x与pH的关系如下图。若忽略通入气体后溶液体积的变化,[x= ] 正确的是
] 正确的是

 ] 正确的是
] 正确的是
| A.水的电离程度:P1>P2>P3 |
B.P2所示溶液中:c(Cl-)=c( )+c(NH3·H2O) )+c(NH3·H2O) |
C.P3所示溶液中:c( )>c(Cl-)>c(OH-)>c(H+) )>c(Cl-)>c(OH-)>c(H+) |
D.25℃时, 的水解常数为10-9.25 的水解常数为10-9.25 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】亚磷酸(H3PO3)是一种二元弱酸,常温下,向一定浓度的NaOH溶液中逐滴滴加H3PO3溶液,含磷各微粒的分布分数X(平衡时某微粒的浓度占各微粒浓度之和的分数)与pOH[pOH=-lgc(OH-)]的关系如图所示。下列说法正确的是
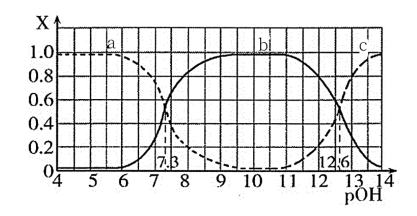

| A.反应主要产物为Na2HPO3和NaH2PO3两种酸式盐 |
B.曲线b代表X(HPO ) ) |
C.H2PO 的电离平衡常数Ka=1×10-6.7mol·L-1 的电离平衡常数Ka=1×10-6.7mol·L-1 |
D.NaH2PO3溶液:c(Na+)>c(HPO )>c(H2PO )>c(H2PO )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】实验室制备的乙酸乙酯样品中混有乙酸和乙醇,某兴趣小组设计如下方案分离与提纯该样品。
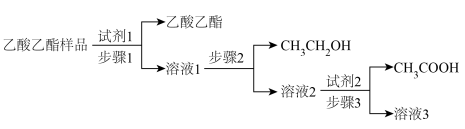
| A.步骤1中,试剂1为NaOH溶液 |
| B.步骤1中涉及分液操作,乙酸乙酯从分液漏斗上口倒出 |
| C.步骤2中可采用蒸馏操作 |
| D.步骤3中,试剂2宜选用硫酸等难挥发性酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列装置或操作能达到实验目的的是
| A | B | C | D |
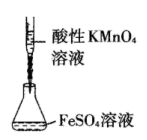 | 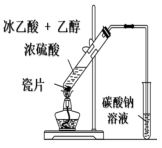 | 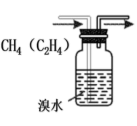 | 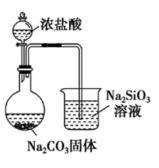 |
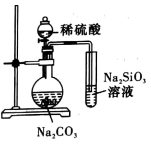
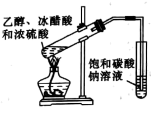
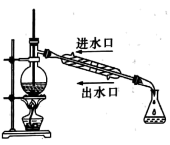
| 用酸性KMnO4溶液滴定FeSO4溶液 | 制取乙酸乙酯 | 除去CH4中的C2H4 | 证明酸性: HCl>H2CO3>H2SiO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


 溶液,再加几滴
溶液,再加几滴 溶液
溶液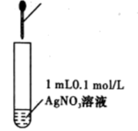
 的非金属性强弱
的非金属性强弱

