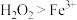下列有关说法中正确的是
| A.Ksp(AB2)<Ksp(CD),说明AB2 的溶解度小于CD 的溶解度 |
| B.在ZnS的沉淀溶解平衡体系中加入蒸馏水,ZnS的Ksp增大 |
| C.AgCl 分别在同浓度的CaCl2溶液和NaCl 溶液中溶解度不同 |
| D.在CaCO3的沉淀溶解平衡体系中加入稀盐酸,沉淀溶解平衡不移动 |
更新时间:2020-02-17 19:50:13
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法不正确的是
| A.pH 相等的NaOH和Na2CO3溶液c(NaOH)>c(Na2CO3) |
| B.稀释 0.1mol/L 醋酸溶液,其电离程度增大,pH 也增大 |
| C.AlBr3 溶液蒸干灼烧后得到的固体是 Al2O3 |
| D.分别用等体积的蒸馏水和稀硫酸洗涤 BaSO4 沉淀,用水洗涤造成 BaSO4 的损失量大于用稀硫酸洗涤时的损失量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关描述不正确的是
| A.用杂化轨道理论解释CH4的正四面体空间构型 |
B.用周期律与周期表解释反应2C+SiO2 2CO↑+Si 2CO↑+Si |
| C.用平衡移动原理解释钟乳石的形成过程 |
| D.用洪特规则解释Fe2+与Fe3+稳定性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列图示实验正确的是
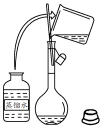 | 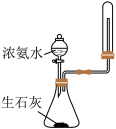 |
| A.洗涤烧杯并将洗涤液转入容量瓶 | B.实验室快速制备 |
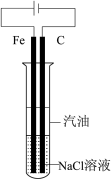 | 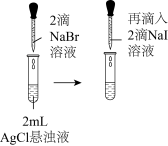 |
C.制备并观察 的颜色 的颜色 | D.证明溶解度: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列对实验现象解释的方程式中,正确的是
A.向醋酸中加入小苏打溶液,产生无色气体: |
B.向 溶液中加入足量的 溶液中加入足量的 溶液,得到白色沉淀: 溶液,得到白色沉淀: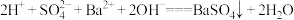 |
C.向 悬浊液中滴入 悬浊液中滴入 溶液,生成黑色沉淀: 溶液,生成黑色沉淀: |
D.向铬酸钾溶液中滴入少量浓硫酸,溶液变橙色: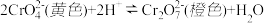 |
您最近一年使用:0次

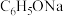 溶液中通入
溶液中通入

 和
和 溶液
溶液
 溶液中滴加
溶液中滴加 溶液
溶液