常温下,Ksp(MnS)=2.5×10-13,Ksp(FeS)=6.3×10-18。FeS和MnS在水中的沉淀溶解平衡曲线如图所示(X2+表示Fe2+或Mn2+),下列说法错误的是( )
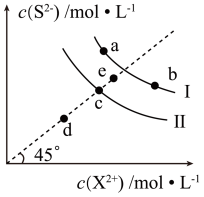

| A.曲线I表示MnS的沉淀溶解平衡曲线 |
| B.升高温度,曲线Ⅱ上的c点可沿虚线平移至d点 |
C.常温下,反应MnS(s)+Fe2+(aq) FeS(s)+Mn2+(aq)的平衡常数K≈4×104 FeS(s)+Mn2+(aq)的平衡常数K≈4×104 |
| D.向b点溶液中加入少量Na2S固体,溶液组成由b点沿工线向a点方向移动 |
19-20高三上·湖南益阳·期末 查看更多[8]
湖南省益阳市2019-2020学年高三上学期期末考试化学试题湖南省衡阳市一中2020届高三1月份期末联考理综化学试题(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编宁夏六盘山高级中学2020届高三下学期第五次模拟测试理综化学试题(已下线)第21讲 难溶电解质的溶解平衡-2021年高考化学一轮复习名师精讲练(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)江西省南昌市八一中学、洪都中学、南师附中、十七中四校2021-2022学年高二上学期期末联考化学考试试题云南省大理市下关第一中学2023-2024学年高二下学期开学化学试题
更新时间:2020-02-22 13:39:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】有关AgCl沉淀的溶解平衡的说法正确的是
| A.AgCl沉淀的生成和溶解仍在不断进行,但速率相等 |
| B.AgCl不溶于水,溶液中没有Cl-和Ag+ |
| C.升高温度,AgCl的溶解度不变,Ksp不变 |
| D.向AgCl饱和溶液中加入NaCl固体,AgCl的Ksp变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合后溶液显中性 |
| B.pH=11的氨水稀释100倍后,溶液的pH=9 |
| C.常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同 |
| D.常温下,已知醋酸电离平衡常数为Ka,醋酸根水解平衡常数为Kh,水的离子积为Kw,则有:Ka·Kh=Kw |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对饱和AgCl溶液(有AgCl固体存在)进行下列操作后,c(Ag+)和Ksp(AgCl)均保持不变的是
| A.加少量水稀释 | B.加热 |
| C.加入少量盐酸 | D.加入少量AgNO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关实验操作、现象、解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 等体积 的HX和HY两种酸分别与足量的铁反应,排水法收集气体 的HX和HY两种酸分别与足量的铁反应,排水法收集气体 | HX放出的氢气多 | HX酸性比HY弱 |
| B | 先向 溶液中滴几滴 溶液中滴几滴 溶液,再加入几滴 溶液,再加入几滴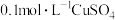 溶液 溶液 | 开始有白色沉淀生成;后又有黑色沉淀生成 |  |
| C | Al箔插入稀 中 中 | 无现象 | Al箔表面被 氧化,形成致密的氧化膜 氧化,形成致密的氧化膜 |
| D | 向紫色石蕊试液中持续长时间通入氯气 | 溶液先变红,最后变为无色 | 氯气有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列装置图或曲线图与对应的叙述相符的是
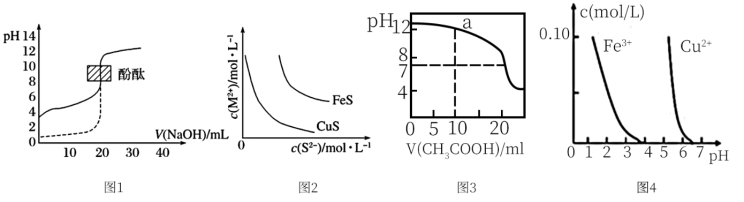

| A.如图1所示,用0.1mol/LNaOH溶液分别滴定相同物质的量浓度、相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线 |
| B.某温度下FeS、CuS的沉淀溶解平衡曲线如图2所示,首先沉淀的离子为Fe2+ |
| C.如图3所示,用0.1mol/LCH3COOH溶液滴定20mL0.1mol/LNaOH溶液的滴定曲线,当pH=7时:c(Na+)=(CH3COO-)>c(OH-)=c(H+) |
| D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在5.5左右 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
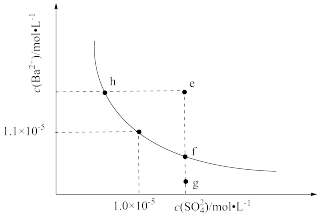
【推荐1】某温度下, 的溶解平衡曲线如下图所示,下列说法错误的是
的溶解平衡曲线如下图所示,下列说法错误的是
 的溶解平衡曲线如下图所示,下列说法错误的是
的溶解平衡曲线如下图所示,下列说法错误的是
A.该温度下 的溶度积 的溶度积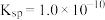 |
| B.升高温度可使f点移动到h点沉淀析出 |
C.加入 固体可使g点移动到f点 固体可使g点移动到f点 |
D.该温度下e点析出 沉淀 沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】①已知t℃时 的
的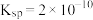 ;②在t℃时
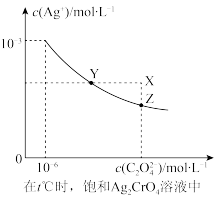
;②在t℃时 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
 的
的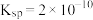 ;②在t℃时
;②在t℃时 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.在t℃时, 的 的 为 为 |
B.在饱和 溶液中加入 溶液中加入 可使溶液由Y点到X点 可使溶液由Y点到X点 |
C.在t℃时,以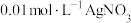 溶液滴定 溶液滴定 和 和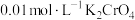 的混合溶液, 的混合溶液, 先沉淀 先沉淀 |
D.在t℃时,反应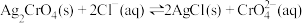 的平衡常数 的平衡常数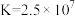 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化学反应原理是研究化学的重要工具,下列相关说法正确的是
A.CH4(g)+Cl2(g)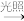 CH3Cl(g)+HCl(g)能自发进行,则该反应 CH3Cl(g)+HCl(g)能自发进行,则该反应 H>0 H>0 |
| B.向碳酸钠溶液中通入少量的氯气:Na2CO3+H2O+2Cl2=2HClO+2NaCl+CO2 |
| C.室温下,稀释0.1 mol/L的HClO溶液,溶液中c(ClO-)减小 |
| D.向硫酸钡悬浊液中加入足量饱和碳酸钠溶液,振荡过滤洗涤,向沉淀中加入盐酸溶液有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某实验小组按下图所示进行实验:

下列说法错误的是

下列说法错误的是
A.①③溶液中均有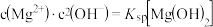 |
| B.③溶液又变红的原因:沉淀溶解平衡正向移动 |
C.①溶液中 等于③溶液中 等于③溶液中 |
D.③溶液中存在: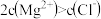 |
您最近一年使用:0次
【推荐3】室温下,通过下列实验探究沉淀的生成、转化与溶解。
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 向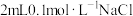 溶液中滴加2滴 溶液中滴加2滴 溶液,产生白色沉淀 溶液,产生白色沉淀 |
| 2 | 向实验1的试管中滴加4滴 溶液,沉淀变为黄色 溶液,沉淀变为黄色 |
| 3 | 向实验2的试管中滴加8滴 溶液,沉淀变为黑色 溶液,沉淀变为黑色 |
| 4 | 向少量 固体中滴加适量 固体中滴加适量 氨水,固体溶解,得到无色澄清溶液 氨水,固体溶解,得到无色澄清溶液 |
A.实验 1 所得上层清液中有 c(Na+)>c(Cl-)>c(NO ) ) |
| B.实验 2 说明 Ksp(AgI)>Ksp (AgCl) |
| C.实验 3 所用的 Na2S 溶液中存在 c(OH-)=c(H+)+c(HS-)+c( H2S) |
| D.实验 4 中反应的离子方程式为 Ag++2NH3=[Ag(NH3)2]+ |
您最近一年使用:0次

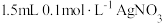 溶液和
溶液和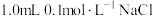 溶液混合,得到浊液a,过滤得到滤液b和白色沉淀c。已知:
溶液混合,得到浊液a,过滤得到滤液b和白色沉淀c。已知: ,
, 。下列分析错误的是
。下列分析错误的是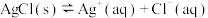

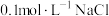 溶液,会出现白色沉淀
溶液,会出现白色沉淀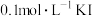 溶液,沉淀变为黄色
溶液,沉淀变为黄色 和
和 增大
增大 在水溶液中存在平衡:
在水溶液中存在平衡: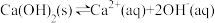 ,升温,溶液碱性增强
,升温,溶液碱性增强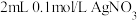 溶液的试管中滴加
溶液的试管中滴加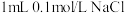 溶液,再向其中滴加4-5滴
溶液,再向其中滴加4-5滴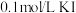 溶液,先观察到白色沉淀,后又产生黄色沉淀,说明
溶液,先观察到白色沉淀,后又产生黄色沉淀,说明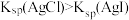
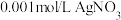 溶液滴入
溶液滴入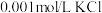 和
和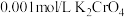 混合溶液中,先产生
混合溶液中,先产生 ,
,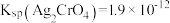 ]
]

