甲醇广泛用作燃料电池的燃料,可用天然气来合成,已知:
①2CH4(g)+O2(g)===2CO(g)+4H2(g) ΔH=-71 kJ/mol
②CO(g)+2H2(g)===CH3OH(l) ΔH=-90.5 kJ/mol
③CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ/mol
下列不 能得出的结论是( )
①2CH4(g)+O2(g)===2CO(g)+4H2(g) ΔH=-71 kJ/mol
②CO(g)+2H2(g)===CH3OH(l) ΔH=-90.5 kJ/mol
③CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ/mol
下列
| A.反应②不需要加热就能进行 |
| B.CO(g)+2H2(g)===CH3OH(g) ΔH>-90.5 kJ/mol |
| C.甲醇的燃烧热ΔH=-764 kJ/mol |
| D.若CO的燃烧热ΔH=-283.0 kJ/mol,则H2的燃烧热ΔH=-285.8 kJ/mol |
更新时间:2020-02-26 20:05:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】计算机模拟单个 处理
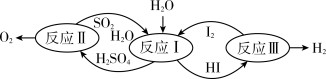
处理 废气在催化剂表面发生反应的反应历程如下,下列说法错误的是
废气在催化剂表面发生反应的反应历程如下,下列说法错误的是

 处理
处理 废气在催化剂表面发生反应的反应历程如下,下列说法错误的是
废气在催化剂表面发生反应的反应历程如下,下列说法错误的是
| A.反应Ⅰ为反应决速步骤 |
B.反应的热化学方程式为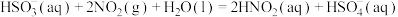 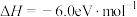 |
C.反应Ⅰ的离子方程式为 |
D.反应中消耗 可处理含 可处理含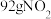 的废气 的废气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在298K、 下,将
下,将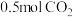 通入
通入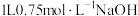 溶液中充分反应,生成碳酸钠和碳酸氢钠的物质的量之比为1∶1,且测得反应放出x kJ的热量。已知在该条件下,
溶液中充分反应,生成碳酸钠和碳酸氢钠的物质的量之比为1∶1,且测得反应放出x kJ的热量。已知在该条件下, 通入
通入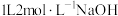 溶液中充分反应放出y kJ的热量,则
溶液中充分反应放出y kJ的热量,则 与NaOH溶液反应生成
与NaOH溶液反应生成 的热化学方程式正确的是
的热化学方程式正确的是
 下,将
下,将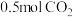 通入
通入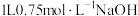 溶液中充分反应,生成碳酸钠和碳酸氢钠的物质的量之比为1∶1,且测得反应放出x kJ的热量。已知在该条件下,
溶液中充分反应,生成碳酸钠和碳酸氢钠的物质的量之比为1∶1,且测得反应放出x kJ的热量。已知在该条件下, 通入
通入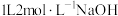 溶液中充分反应放出y kJ的热量,则
溶液中充分反应放出y kJ的热量,则 与NaOH溶液反应生成
与NaOH溶液反应生成 的热化学方程式正确的是
的热化学方程式正确的是A.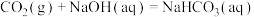 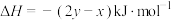 |
B.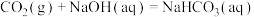 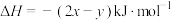 |
C.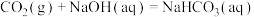  |
D.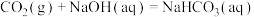 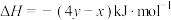 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】甲烷双重整制备合成气(CO和H2)包括了水蒸气重整(反应I)和二氧化碳重整(反应Ⅱ)两个反应。在p=3.2×106Pa下,向密闭容器中按n(CH4):n(H2O):n(CO2)=5:4:2通入混合气,发生反应:(Ea表示反应中基元反应的最大活化能)
反应I:CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=206.2kJ·mol-1 Ea1=240.1kJ·mol-1
反应Ⅱ:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=247.0kJ·mol-1 Ea2=577.6kJ·mol-1
副反应:CH4(g)=C(s)+2H2(g)
重整体系中,各气体的平衡体积分数随温度的变化如图所示。下列说法正确的是

反应I:CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=206.2kJ·mol-1 Ea1=240.1kJ·mol-1
反应Ⅱ:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=247.0kJ·mol-1 Ea2=577.6kJ·mol-1
副反应:CH4(g)=C(s)+2H2(g)
重整体系中,各气体的平衡体积分数随温度的变化如图所示。下列说法正确的是

| A.曲线X表示CH4的平衡体积分数随温度的变化 |
| B.适当增加水蒸气或CO2的用量均可减少碳的生成 |
| C.在相同条件下,反应I的速率小于反应II的速率 |
| D.CO(g)+H2O(g)=CO2(g)+H2(g) △H=40.8kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定条件下31g白磷完全转化为红磷放出7.3kJ的热量。下列叙述错误的是
| A.该转化属于化学变化 |
| B.31g白磷的总能量比31g红磷的总能量高 |
| C.红磷比白磷稳定 |
| D.等质量的白磷和红磷完全燃烧释放的热量相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知热化学方程式:H2O(g)=H2(g) + 1/2O2(g) △H = +241.8kJ/mol
H2(g)+ 1/2O2(g) = H2O(1) △H = -285.8kJ/mol
当1g水蒸气变为液态水时,其热量变化是 ( )
H2(g)+ 1/2O2(g) = H2O(1) △H = -285.8kJ/mol
当1g水蒸气变为液态水时,其热量变化是 ( )
| A.吸收44kJ | B.放出 44kJ |
| C.放出2.44kJ | D.吸收2.44kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知NO2与N2O4可相互转化:2NO2(g) N2O4(g)
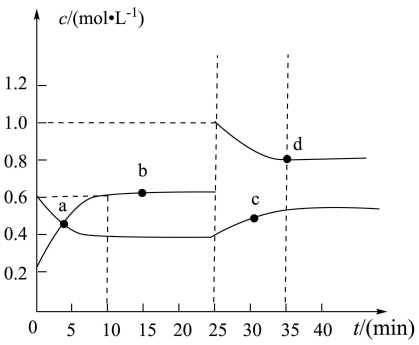
N2O4(g)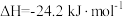 ,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析合理的是
,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析合理的是
 N2O4(g)
N2O4(g)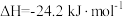 ,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析合理的是
,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图所示。下列推理分析合理的是
| A.25min时,正反应速率减小 |
| B.反应进行到10min时,体系吸收的热量为9.68kJ |
C.a、b、c、d四点中 正与 正与 逆均相等 逆均相等 |
D.10min时, 的生成速率为 的生成速率为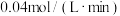 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法中正确的是
| A.在相同条件下,将等量的硫蒸气和硫固体分别完全燃烧,前者放出热量多 |
| B.吸热反应必须在加热条件下才能发生,而放热反应则无须加热 |
| C.在稀溶液中:H+(a)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,若将含0.5molH2SO4的稀硫酸和含0.5molBa(OH)2的稀溶液混合,放出的热量为57.3kJ |
| D.N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.4kJ/mol,则在密闭容器中充入0.5molN2、1.5molH2,充分反应后放出46.2kJ的热量 |
您最近一年使用:0次

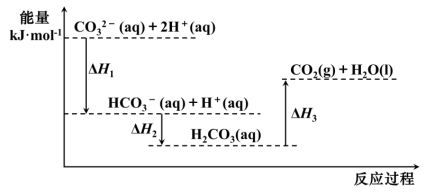
 (aq)+H+(aq)=CO2(g)+H2O(l)为吸热反应
(aq)+H+(aq)=CO2(g)+H2O(l)为吸热反应 (aq)+2H+(aq)=CO2(g)+H2O(l) ΔH=ΔH1+ΔH2+ΔH3
(aq)+2H+(aq)=CO2(g)+H2O(l) ΔH=ΔH1+ΔH2+ΔH3