钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。完成下列计算:
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠___ g。
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度________ (忽略溶液体积变化)。
②计算并确定该钠-钾合金的化学式________ 。
(3)氢氧化钠溶液处理铝土矿井过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2→2Al(OH)3↓ +Na2CO3+H2O。已知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)3和15 mol Na2CO3,若通入溶液的二氧化碳为112L(标准状况下),计算生成的Al(OH)3和Na2CO3的物质的量之比________ 。
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失。
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠。通过计算,分析和比较上表3组数据,给出结论________ 。
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度
②计算并确定该钠-钾合金的化学式
(3)氢氧化钠溶液处理铝土矿井过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2→2Al(OH)3↓ +Na2CO3+H2O。已知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)3和15 mol Na2CO3,若通入溶液的二氧化碳为112L(标准状况下),计算生成的Al(OH)3和Na2CO3的物质的量之比
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失。
| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠。通过计算,分析和比较上表3组数据,给出结论
2012·上海·高考真题 查看更多[2]
更新时间:2020-03-20 22:19:22
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某校研究性学习小组测定Fe—Al合金、Fe—Zn合金和Fe—Cu合金中铁的质量分数,实验室只提供一瓶未标明质量分数的稀硫酸和必要的仪器。他们取其中一种合金的粉末5.6g与足量该硫酸充分反应,经测定,产生了气体ag。请讨论(数据保留两位有效数字为计算结果进行分析讨论):
(1)当粉末为Fe—Al合金时,a的取值范围为___ 。
(2)当粉末为Fe—Zn合金时,a的取值范围为__ 。
(3)当a的取值范围为__ 时,可得出该粉末一定为Fe—Cu合金的结论。
(1)当粉末为Fe—Al合金时,a的取值范围为
(2)当粉末为Fe—Zn合金时,a的取值范围为
(3)当a的取值范围为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取W g NaHCO3固体加热使其完全分解,将生成的CO2通入足量澄清石灰水中全部吸收,生成5.0 g CaCO3沉淀。试计算:
(1)CaCO3的物质的量为_______ mol。
(2)NaHCO3固体的质量w=_______ 。
(1)CaCO3的物质的量为
(2)NaHCO3固体的质量w=
您最近一年使用:0次
【推荐1】请回答下列问题:
(1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为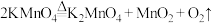 ,氧化产物是
,氧化产物是___________ (填化学式)。
(2)查阅资料可知,铜和浓 共热,发生反应
共热,发生反应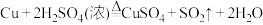 ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为___________ ,其中 在反应中表现的性质为
在反应中表现的性质为___________ 。
(3)已知反应
① ;
;
②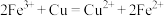 ;
;
③ ;
;
④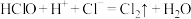 。
。
微粒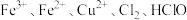 氧化性由强到弱的顺序为
氧化性由强到弱的顺序为___________
(4)请配平下列反应方程式:___________
___________ ___________
___________ (浓)=___________
(浓)=___________ ___________
___________ ___________
___________ ___________
___________
若反应中发生氧化反应的 物质的量为
物质的量为 ,则反应中转移的电子数为
,则反应中转移的电子数为___________ 。
(1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为
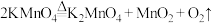 ,氧化产物是
,氧化产物是(2)查阅资料可知,铜和浓
 共热,发生反应
共热,发生反应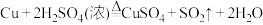 ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为 在反应中表现的性质为
在反应中表现的性质为(3)已知反应
①
 ;
;②
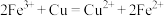 ;
;③
 ;
;④
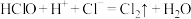 。
。微粒
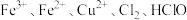 氧化性由强到弱的顺序为
氧化性由强到弱的顺序为(4)请配平下列反应方程式:
___________
 ___________
___________ (浓)=___________
(浓)=___________ ___________
___________ ___________
___________ ___________
___________
若反应中发生氧化反应的
 物质的量为
物质的量为 ,则反应中转移的电子数为
,则反应中转移的电子数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】饮用水质量是关系人类健康的重要问题。
(1)Cl2是最早用于饮用水消毒的物质,写出Cl2溶于水发生反应的离子方程式:___ 。
(2)ClO2是一种高效、低毒的消毒剂,逐渐取代Cl2成为生产自来水的消毒剂,工业上用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应中氧化剂与还原剂物质的量之比为____ 。
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,比Cl2、ClO2氧化性更强,是无二次污染的绿色水处理剂。工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾。由以上信息可知,相同条件下,高铁酸钠溶解度比高铁酸钾溶解度__ (填“大”或“小”)。高铁酸钾溶于水放出氧气,能杀菌消毒,生成能吸附水中悬浮物的氢氧化铁胶体。用一个离子方程式表示高铁酸钾处理水的过程____ 。干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应的还原剂是___ ,每生成1molNa2FeO4转移__ mol电子。
(1)Cl2是最早用于饮用水消毒的物质,写出Cl2溶于水发生反应的离子方程式:
(2)ClO2是一种高效、低毒的消毒剂,逐渐取代Cl2成为生产自来水的消毒剂,工业上用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应中氧化剂与还原剂物质的量之比为
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,比Cl2、ClO2氧化性更强,是无二次污染的绿色水处理剂。工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾。由以上信息可知,相同条件下,高铁酸钠溶解度比高铁酸钾溶解度
您最近一年使用:0次
【推荐3】分类法是进行化学研究的重要方法。不同的标准可以把物质和反应分为不同的类别。回答下列问题:
(1)现有九种物质:①铜;②小苏打;③硫酸铁;④二氧化碳;⑤葡萄糖;⑥熔融氯化钠;⑦氢氧化铁胶体;⑧浓硫酸;⑨液氨;上述物质中,属于能导电的纯净物是___________ (填序号);属于非电解质的是___________ (填序号);③在水中的电离方程式为___________ 。
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是___________ (填标号)。

A. B.HCl C.
B.HCl C. (乙醇) D.NaCl E.Hg
(乙醇) D.NaCl E.Hg
(3)氧化还原反应是一类重要化学反应,在生产生活中有重要应用。
①工业上,用 溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式
溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式___________ 。
②完善下面的化学方程式,并配平___________ 。

③利用盐酸酸化淀粉的KI溶液检验食盐中的碘元素( )。写出发生反应的离子方程式
)。写出发生反应的离子方程式___________ 。
(4)在20.00ml 溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
(1)现有九种物质:①铜;②小苏打;③硫酸铁;④二氧化碳;⑤葡萄糖;⑥熔融氯化钠;⑦氢氧化铁胶体;⑧浓硫酸;⑨液氨;上述物质中,属于能导电的纯净物是
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是

A.
 B.HCl C.
B.HCl C. (乙醇) D.NaCl E.Hg
(乙醇) D.NaCl E.Hg(3)氧化还原反应是一类重要化学反应,在生产生活中有重要应用。
①工业上,用
 溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式
溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式②完善下面的化学方程式,并配平

③利用盐酸酸化淀粉的KI溶液检验食盐中的碘元素(
 )。写出发生反应的离子方程式
)。写出发生反应的离子方程式(4)在20.00ml
 溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________A. | B. | C. | D.V |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】取一定物质的量浓度的NaOH溶液100mL,然后向其通入一定量的CO2气体,得到溶液A,向A中逐滴缓慢加入0.1 mol•L-1的HCl溶液,产生的CO2气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示,通过计算回答:
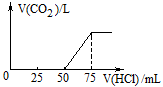
(1)A溶液中的溶质为_________ (化学式),其物质的量之比是_______ 。
(2)通入CO2气体体积__________________ (标准状况)。
(3)NaOH溶液的物质的量浓度______________________ 。
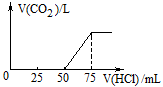
(1)A溶液中的溶质为
(2)通入CO2气体体积
(3)NaOH溶液的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】天然碱是一种重要的矿物质,盛产于我国的青海湖地区。某天然碱样品的成分可以看成是碳酸钠、碳酸氢钠和水按物质的量之比1:1:2形成的结晶水合物。请回答下列问题:
(1)这种天然碱中碳酸钠、碳酸氢钠和水三者的质量比为___________ 。
(2)45.2 g此天然碱与100 mL密度为1.1 g/cm3的中等浓度盐酸恰好完全反应,产生a mol CO2,则a=_______ ,盐酸中溶质的质量分数ω(HCl)=_______ %。
(3)用一个化学方程式表示该天然碱与盐酸的反应:
___________________________ 。
(1)这种天然碱中碳酸钠、碳酸氢钠和水三者的质量比为
(2)45.2 g此天然碱与100 mL密度为1.1 g/cm3的中等浓度盐酸恰好完全反应,产生a mol CO2,则a=
(3)用一个化学方程式表示该天然碱与盐酸的反应:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有白色沉淀生成,在所得的悬浊液中逐滴加入1mol•L﹣1HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示.试回答:
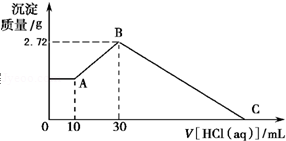
(1)从0开始到A点沉淀物的化学式为____________ ;B点沉淀物的化学式为_________ .
(2)原混合物中的MgCl2的物质的量为_____________ ,AlCl3的物质的量为___________ ,NaOH的物质的量为________ .
(3)HCl溶液在C点的体积数是________ mL.

(1)从0开始到A点沉淀物的化学式为
(2)原混合物中的MgCl2的物质的量为
(3)HCl溶液在C点的体积数是
您最近一年使用:0次

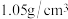 ,HCl的质量分数为
,HCl的质量分数为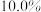 ,试计算:
,试计算: ,充分反应共生成
,充分反应共生成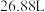 气体(标准状况),求混合物中镁和铝的质量各为多少?
气体(标准状况),求混合物中镁和铝的质量各为多少?

