请回答下列问题:
(1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为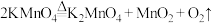 ,氧化产物是
,氧化产物是___________ (填化学式)。
(2)查阅资料可知,铜和浓 共热,发生反应
共热,发生反应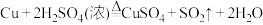 ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为___________ ,其中 在反应中表现的性质为
在反应中表现的性质为___________ 。
(3)已知反应
① ;
;
②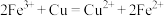 ;
;
③ ;
;
④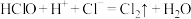 。
。
微粒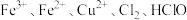 氧化性由强到弱的顺序为
氧化性由强到弱的顺序为___________
(4)请配平下列反应方程式:___________
___________ ___________
___________ (浓)=___________
(浓)=___________ ___________
___________ ___________
___________ ___________
___________
若反应中发生氧化反应的 物质的量为
物质的量为 ,则反应中转移的电子数为
,则反应中转移的电子数为___________ 。
(1)已知实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为
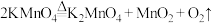 ,氧化产物是
,氧化产物是(2)查阅资料可知,铜和浓
 共热,发生反应
共热,发生反应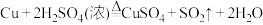 ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为 在反应中表现的性质为
在反应中表现的性质为(3)已知反应
①
 ;
;②
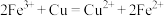 ;
;③
 ;
;④
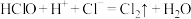 。
。微粒
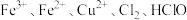 氧化性由强到弱的顺序为
氧化性由强到弱的顺序为(4)请配平下列反应方程式:
___________
 ___________
___________ (浓)=___________
(浓)=___________ ___________
___________ ___________
___________ ___________
___________
若反应中发生氧化反应的
 物质的量为
物质的量为 ,则反应中转移的电子数为
,则反应中转移的电子数为
更新时间:2023-12-02 19:01:42
|
相似题推荐
【推荐1】高锰酸钾是一种典型的强氧化剂。
(1)在用 KMnO4 酸性溶液处理固体 Cu2S 时,发生的反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
①还原产物为_____ 。
②被氧化的元素是_____
③氧化剂与还原剂的物质的量之比为_____
④每生成 2.24 L(标况下)SO2,转移电子数目是_____
(2)用 KMnO4 酸性溶液处理固体 CuS 时,也可将 CuS 反应成 Cu2+和 SO2。写出该离子反应方程式_____
(3)15.8g KMnO4,加热分解后剩余固体 15.0 g。该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体 A,产物中锰元素以 Mn2+存在,则气体 A 的物质的量为_____ mol。
(1)在用 KMnO4 酸性溶液处理固体 Cu2S 时,发生的反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
①还原产物为
②被氧化的元素是
③氧化剂与还原剂的物质的量之比为
④每生成 2.24 L(标况下)SO2,转移电子数目是
(2)用 KMnO4 酸性溶液处理固体 CuS 时,也可将 CuS 反应成 Cu2+和 SO2。写出该离子反应方程式
(3)15.8g KMnO4,加热分解后剩余固体 15.0 g。该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体 A,产物中锰元素以 Mn2+存在,则气体 A 的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】现用Zn与实验室中的盐酸反应制取4.48LH2(标准状况)。
(1)求消耗得还原剂的质量为多少克___________ ?
(2)如果选用所贴标签为7%(密度为1.043g·mL-1)的盐酸,至少需该盐酸多少毫升___________ ?
(1)求消耗得还原剂的质量为多少克
(2)如果选用所贴标签为7%(密度为1.043g·mL-1)的盐酸,至少需该盐酸多少毫升
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】双氧水是重要的化学试剂。
(1)一定条件下,O2得电子转化为超氧自由基(·O ),并实现如下图所示的转化:
),并实现如下图所示的转化:
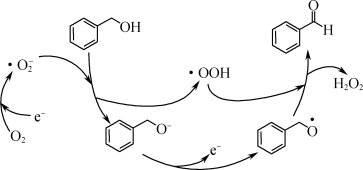
①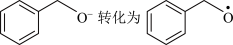 是
是________ (填“氧化”或“还原”)反应。
②写出图示转化总反应的化学方程式:________ 。
(2) K2Cr2O7酸性条件下与H2O2反应生成CrO5,反应为非氧化还原反应。据此分析,CrO5中-2价O与-1价O的数目比为________ 。
(3) H2O2可用于测定酒精饮料中乙醇的含量。现有20.00 mL某鸡尾酒,将其中CH3CH2OH蒸出并通入17.0 mL 0.200 0 mol·L-1 K2Cr2O7溶液(H2SO4酸化)中,发生反应:K2Cr2O7+C2H5OH+H2SO4―→Cr2(SO4)3+CH3COOH+K2SO4+H2O(未配平)
再用0.400 0 mol·L-1的双氧水滴定反应后所得的混合液,用去19.00 mL双氧水,滴定过程中发生如下反应:
反应1:4H2O2+K2Cr2O7+H2SO4===K2SO4+2CrO5+5H2O
反应2:H2O2+CH3COOH===CH3COOOH+H2O
则该鸡尾酒中CH3CH2OH的物质的量浓度为________ mol·L-1(写出计算过程)。
(1)一定条件下,O2得电子转化为超氧自由基(·O
 ),并实现如下图所示的转化:
),并实现如下图所示的转化:
①
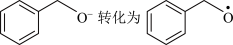 是
是②写出图示转化总反应的化学方程式:
(2) K2Cr2O7酸性条件下与H2O2反应生成CrO5,反应为非氧化还原反应。据此分析,CrO5中-2价O与-1价O的数目比为
(3) H2O2可用于测定酒精饮料中乙醇的含量。现有20.00 mL某鸡尾酒,将其中CH3CH2OH蒸出并通入17.0 mL 0.200 0 mol·L-1 K2Cr2O7溶液(H2SO4酸化)中,发生反应:K2Cr2O7+C2H5OH+H2SO4―→Cr2(SO4)3+CH3COOH+K2SO4+H2O(未配平)
再用0.400 0 mol·L-1的双氧水滴定反应后所得的混合液,用去19.00 mL双氧水,滴定过程中发生如下反应:
反应1:4H2O2+K2Cr2O7+H2SO4===K2SO4+2CrO5+5H2O
反应2:H2O2+CH3COOH===CH3COOOH+H2O
则该鸡尾酒中CH3CH2OH的物质的量浓度为
您最近一年使用:0次
【推荐1】已知:i.用毛笔蘸取少量30%的FeCl3溶液在铜片上写一个“Cu”,放置片刻后用少量蒸馏水冲洗铜片后,在铜片上会出现凹凸的“Cu”。
ii.Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。
(1)写出i中反应的离子方程式:___________ 。
(2)反应ii中氧化剂与还原剂的物质的量之比为___________ ,用双线桥法标出电子转移的方向与数目:___________ ,当反应中有0.6 mol电子转移时,生成NO的体积为___________ L(标准状况)。
(3)向含有0.2 mol FeCl3、0.2 mol CuCl2的混合溶液中加入0.1 mol Zn,充分反应后溶液中没有固体存在,则溶液中的金属阳离子有Zn2+、___________ 。
(4)HNO3、Fe3+、Cu2+的氧化性由强到弱的顺序为___________ 。
ii.Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。
(1)写出i中反应的离子方程式:
(2)反应ii中氧化剂与还原剂的物质的量之比为
(3)向含有0.2 mol FeCl3、0.2 mol CuCl2的混合溶液中加入0.1 mol Zn,充分反应后溶液中没有固体存在,则溶液中的金属阳离子有Zn2+、
(4)HNO3、Fe3+、Cu2+的氧化性由强到弱的顺序为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色环保水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,应用广泛。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应氧化产物是_____ (填化学式)。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO−、OH−、FeO42-、Cl−、H2O。
①写出并配平碱性条件下湿法制高铁酸钾的离子反应方程式:________________________________ 。
②每生成1molFeO42-转移________ mol电子;若反应过程中转移了0.3mol电子,则还原产物的物质的量为________ mol。
Ⅱ.氧化还原反应在生产生活中应用广泛,思考回答以下问题
已知:2Fe3++2I−===2Fe2++I2,2Fe2++Br2===2Fe3++2Br−,2Fe2++Cl2===2Fe3++2Cl−
(1)含有1mol FeI2和2mol FeBr2的溶液中通入2mol Cl2,此时被氧化的离子是________ 。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c molCl2,当Br−被氧化一半时,c为_______________ (用含a、b的代数式表示)。
(3)已知:S2O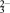 具有较强的还原性,实验室可用I-测定测定K2S2O8样品的纯度:有关反应方程式为: I2+2S2O32-→2I−+S4O62-,S2O82-+2I−→2SO42-+I2,则S2O82-、S4O62-、I2氧化性强弱顺序为:
具有较强的还原性,实验室可用I-测定测定K2S2O8样品的纯度:有关反应方程式为: I2+2S2O32-→2I−+S4O62-,S2O82-+2I−→2SO42-+I2,则S2O82-、S4O62-、I2氧化性强弱顺序为:____________ 。
(4)已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-;向含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如下图所示。
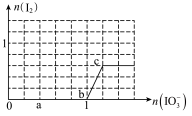
写出a点处还原产物是_______________ ;b点到c点反应的离子方程式________________
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应氧化产物是
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO−、OH−、FeO42-、Cl−、H2O。
①写出并配平碱性条件下湿法制高铁酸钾的离子反应方程式:
②每生成1molFeO42-转移
Ⅱ.氧化还原反应在生产生活中应用广泛,思考回答以下问题
已知:2Fe3++2I−===2Fe2++I2,2Fe2++Br2===2Fe3++2Br−,2Fe2++Cl2===2Fe3++2Cl−
(1)含有1mol FeI2和2mol FeBr2的溶液中通入2mol Cl2,此时被氧化的离子是
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c molCl2,当Br−被氧化一半时,c为
(3)已知:S2O
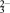 具有较强的还原性,实验室可用I-测定测定K2S2O8样品的纯度:有关反应方程式为: I2+2S2O32-→2I−+S4O62-,S2O82-+2I−→2SO42-+I2,则S2O82-、S4O62-、I2氧化性强弱顺序为:
具有较强的还原性,实验室可用I-测定测定K2S2O8样品的纯度:有关反应方程式为: I2+2S2O32-→2I−+S4O62-,S2O82-+2I−→2SO42-+I2,则S2O82-、S4O62-、I2氧化性强弱顺序为:(4)已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-;向含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如下图所示。

写出a点处还原产物是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】金属与人类的生产生活密切相关,牢固掌握金属的知识十分必要。
(1)将锌粉加入到含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤。
①若滤液中只含一种溶质,请分析则滤渣的成分______________ ;
②若滤渣中含有两种金属,请分析滤液的成分______________ 。
(2)合金的用途十分广泛。某化学小组欲测定黄铜片(铜锌合金)的组成进行如下实验:取黄铜片30g放入烧杯,将250g稀硫酸分5次加入烧杯中,充分反应后,测得剩余固体的质量记录如下。请计算:
(1)黄铜片中铜的含量______________ 。
(2)稀硫酸中溶质的质量分数______________ 。
(1)将锌粉加入到含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤。
①若滤液中只含一种溶质,请分析则滤渣的成分
②若滤渣中含有两种金属,请分析滤液的成分
(2)合金的用途十分广泛。某化学小组欲测定黄铜片(铜锌合金)的组成进行如下实验:取黄铜片30g放入烧杯,将250g稀硫酸分5次加入烧杯中,充分反应后,测得剩余固体的质量记录如下。请计算:
| 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 23.5 | 17 | 11.5 | 9.6 | 9.6 |
(1)黄铜片中铜的含量
(2)稀硫酸中溶质的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】一种由CuO和KHC2O4溶液反应得到的蓝色结晶[KaCub(C2O4)c·dH2O]。为测定其组成,进行了如下实验:
步骤1:称取3.5400g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100mL溶液A。
步骤2:量取20.00mLA溶液,滴加0.2000mol·L-1KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00mL。
步骤3:另取20.00mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16g。
已知:步骤2中发生反应如下,请配平:___ 。
 + H2C2O4+ H+= Mn2++ CO2↑+ H2O
+ H2C2O4+ H+= Mn2++ CO2↑+ H2O
(1)3.5400g该样品中含n( )=
)=___ mol。
(2)3.5400g该样品中含n(Cu2+)=___ mol。
(3)通过计算确定该蓝色晶体的化学式(计算过程)___ 。
步骤1:称取3.5400g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100mL溶液A。
步骤2:量取20.00mLA溶液,滴加0.2000mol·L-1KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00mL。
步骤3:另取20.00mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16g。
已知:步骤2中发生反应如下,请配平:
 + H2C2O4+ H+= Mn2++ CO2↑+ H2O
+ H2C2O4+ H+= Mn2++ CO2↑+ H2O(1)3.5400g该样品中含n(
 )=
)=(2)3.5400g该样品中含n(Cu2+)=
(3)通过计算确定该蓝色晶体的化学式(计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】黑火药的成分是硝酸钾、硫磺、木炭。当加热或点燃时会发生剧烈反应而爆炸。生成物中硫元素变为最低价,碳、氮两元素均变成空气中常见的气体。
(1)写出有关反应的化学方程式:_____________________
(2)10.1g KNO3完全反应时,被它氧化的碳为________ g。
(1)写出有关反应的化学方程式:
(2)10.1g KNO3完全反应时,被它氧化的碳为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】硫化钠是用于皮革鞣制的重要化学试剂,可用无水芒硝(Na2SO4)与炭粉在高温下反应而制得,反应方程式如下:Na2SO4+4C →Na2S+ 4CO,Na2SO4+4CO→Na2S+4CO2
(1)现有无水芒硝17.75g,若生成过程中无水芒硝的利用率为80%,则理论上可得到Na2S_____ g,最多生成标况下的CO_____ L。
(2)若在反应过程中生成的Na2S3mol,则消耗的碳单质的物质的量 n的范围是____ mol≤n≤___ mol,若生成等物质的量CO和CO2,则消耗的碳的物质的量为____ mol。
(3)Na2S放置在空气中,会被缓慢氧化成Na2SO4及 Na2SO3,现称取已经部分氧化的硫化钠样品78.40g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20g,放出H2S气体2.24L(标准状况)。请计算:78.40g样品中各氧化产物的物质的量(写出必要的计算过程)。_____
(1)现有无水芒硝17.75g,若生成过程中无水芒硝的利用率为80%,则理论上可得到Na2S
(2)若在反应过程中生成的Na2S3mol,则消耗的碳单质的物质的量 n的范围是
(3)Na2S放置在空气中,会被缓慢氧化成Na2SO4及 Na2SO3,现称取已经部分氧化的硫化钠样品78.40g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20g,放出H2S气体2.24L(标准状况)。请计算:78.40g样品中各氧化产物的物质的量(写出必要的计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】酸性条件下,许多氧化剂可使KI溶液中的I-氧化,例如KIO3(IO3-→I2)、H2O2(H2O2→H2O)、FeCl3(Fe3+→Fe2+)、K2Cr2O7(Cr2O72-→Cr3+).请根据题目要求填空:
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式______________ 。
(2)在酸性条件下(足量),各取1L浓度为1mol•L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3):n(H2O2):n(FeCl3):n(K2Cr2O7)=______________________ (要求写出最简比)
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式
(2)在酸性条件下(足量),各取1L浓度为1mol•L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3):n(H2O2):n(FeCl3):n(K2Cr2O7)=
您最近一年使用:0次



