现有如下物质:
①明矾 ②一水合氨 ③碳酸氢钠 ④硫酸铁 ⑤硝酸钡 ⑥硝酸
请完成下列问题:
(1)属于弱电解质的是___________________ ;(选填编号)
(2)由于促进水的电离平衡而使溶液显酸性的是__________________ ;(选填编号)
(3)它们水溶液PH >7的有_________________ ;(选填编号)
(4)写出下列物质之间发生反应的离子方程式:
①+⑤__________________ ②+④___________________ ③+⑥__________________
(5)明矾溶于水后能净水,是由于Al3+水解后能形成Al(OH)3胶体,该胶体具有吸附性,请写出Al3+水解的方程式:____________________ ;
硫酸铁溶液水解可以得到一系列具有净水作用的碱式硫酸铁(xFe2O3⋅ySO3⋅zH2O),为测定某碱式硫酸铁的组成,取5.130g样品溶于足量盐酸中,然后加入过量的BaCl2溶液,经过滤、洗涤、干燥得白色固体5.825g,向上述滤液中加入过量的NaOH溶液,经过滤、洗涤、灼烧得到固体1.600g,该样品的化学式中x、y、z的值分别为_______________ (填整数)
①明矾 ②一水合氨 ③碳酸氢钠 ④硫酸铁 ⑤硝酸钡 ⑥硝酸
请完成下列问题:
(1)属于弱电解质的是
(2)由于促进水的电离平衡而使溶液显酸性的是
(3)它们水溶液PH >7的有
(4)写出下列物质之间发生反应的离子方程式:
①+⑤
(5)明矾溶于水后能净水,是由于Al3+水解后能形成Al(OH)3胶体,该胶体具有吸附性,请写出Al3+水解的方程式:
硫酸铁溶液水解可以得到一系列具有净水作用的碱式硫酸铁(xFe2O3⋅ySO3⋅zH2O),为测定某碱式硫酸铁的组成,取5.130g样品溶于足量盐酸中,然后加入过量的BaCl2溶液,经过滤、洗涤、干燥得白色固体5.825g,向上述滤液中加入过量的NaOH溶液,经过滤、洗涤、灼烧得到固体1.600g,该样品的化学式中x、y、z的值分别为
更新时间:2020-03-24 08:56:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】在图(Ⅰ)所示的装置中,烧杯中盛放的是Ba(OH)2溶液,当从滴定管中逐渐加入某种溶液A时,溶液的导电性的变化趋势如图(Ⅱ)所示。
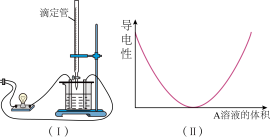
(1)滴加液体至图(Ⅱ)中曲线最低点时,灯泡可能熄灭,可能的原因是______________ 。
(2)试根据离子反应的特点分析,溶液A中含有的溶质可能是(填序号)____________ 。
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(3)已知0.1 mol·L-1NaHSO4溶液中c(H+)=0.1 mol·L-1,请回答下列问题:
①写出NaHSO4在水溶液中的电离方程式_______________________________ 。
②NaHSO4属于________ (填“酸”、“碱”或“盐”)。
③向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:_______ ;在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:_________ 。写出NaHSO4溶液与NaHCO3溶液混合的离子方程式_________ 。
(4)有以下物质:①石墨; ②氯化氢气体; ③酒精; ④铝; ⑤二氧化碳; ⑥碳酸氢钠固体;⑦氢氧化钡溶液; ⑧液态醋酸; ⑨氯化银固体; ⑩氨气。
①其中能导电的是:____________________________ ;
②属于非电解质的是:__________________________ 。

(1)滴加液体至图(Ⅱ)中曲线最低点时,灯泡可能熄灭,可能的原因是
(2)试根据离子反应的特点分析,溶液A中含有的溶质可能是(填序号)
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(3)已知0.1 mol·L-1NaHSO4溶液中c(H+)=0.1 mol·L-1,请回答下列问题:
①写出NaHSO4在水溶液中的电离方程式
②NaHSO4属于
③向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:
(4)有以下物质:①石墨; ②氯化氢气体; ③酒精; ④铝; ⑤二氧化碳; ⑥碳酸氢钠固体;⑦氢氧化钡溶液; ⑧液态醋酸; ⑨氯化银固体; ⑩氨气。
①其中能导电的是:
②属于非电解质的是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】以下为中学化学中常见的几种物质:①Cu ②熔融NaCl ③NaHSO4固体 ④CO2 ⑤盐酸⑥蔗糖 ⑦KHCO3溶液。请按下列分类标准回答问题。(以下填写物质编号)
(1)能导电的是_______________ ;
(2)属于非电解质的是________________ ;
(3)属于电解质的写出在水溶液中的电离方程式____________ 。
(1)能导电的是
(2)属于非电解质的是
(3)属于电解质的写出在水溶液中的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】 、
、 和
和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1) 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为_______ 。
(2) 和
和 的处理。已除去
的处理。已除去 的硝酸尾气可用
的硝酸尾气可用 溶液吸收,主要反应为:
溶液吸收,主要反应为: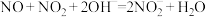 ;
;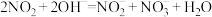
①下列措施能提高尾气中 和
和 去除率的有
去除率的有_______ (填字母)。
A. 加快通入尾气的速率
B. 采用气、液逆流的方式吸收尾气
C. 吸收尾气过程中定期补加适量 溶液
溶液
②吸收后的溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是_______ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
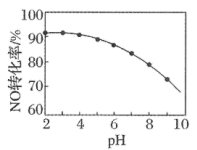
(3) 的氧化吸收。用
的氧化吸收。用 溶液吸收硝酸尾气,可提高尾气中
溶液吸收硝酸尾气,可提高尾气中 的去除率。其他条件相同,
的去除率。其他条件相同, 转化为
转化为 的转化率随
的转化率随 溶液初始
溶液初始 (用稀盐酸调节)的变化如图所示。
(用稀盐酸调节)的变化如图所示。
在酸性 溶液中,
溶液中, 氧化
氧化 生成
生成 和
和 ,其离子方程式为
,其离子方程式为_______ 。
 、
、 和
和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。(1)
 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为(2)
 和
和 的处理。已除去
的处理。已除去 的硝酸尾气可用
的硝酸尾气可用 溶液吸收,主要反应为:
溶液吸收,主要反应为: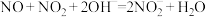 ;
;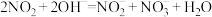
①下列措施能提高尾气中
 和
和 去除率的有
去除率的有A. 加快通入尾气的速率
B. 采用气、液逆流的方式吸收尾气
C. 吸收尾气过程中定期补加适量
 溶液
溶液②吸收后的溶液经浓缩、结晶、过滤,得到
 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是(3)
 的氧化吸收。用
的氧化吸收。用 溶液吸收硝酸尾气,可提高尾气中
溶液吸收硝酸尾气,可提高尾气中 的去除率。其他条件相同,
的去除率。其他条件相同, 转化为
转化为 的转化率随
的转化率随 溶液初始
溶液初始 (用稀盐酸调节)的变化如图所示。
(用稀盐酸调节)的变化如图所示。
在酸性
 溶液中,
溶液中, 氧化
氧化 生成
生成 和
和 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有以下物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是________ (填序号,下同),属于电解质的是________ 。
(2)向④中逐滴滴加⑦,可观察到的现象是_____________________ 。
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是________ (填字母)。

(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表示)_____________ 。
Ⅰ.现有以下物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H2O。请举个例子反驳上述观点(用离子方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题。
(1)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是___________ 。
②上述物质中既不是电解质也不是非电解质的是___________ 。
③有下列三种物质: ;
; ;
; ;
;
a.写出上述物质中的盐在熔融状态下的电离方程式___________ ,
b.写出上述物质中的酸与氨水反应的离子方程式___________ 。
(2)在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来;
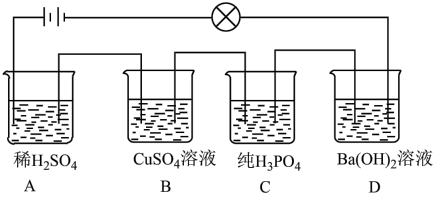
①加水的烧杯为___________ 。
②向烧杯A滴入 溶液,溶液导电性
溶液,溶液导电性___________ 。
A.变强 B.变弱 C.先变弱后变强 D.先变强后变弱
③ 是三元酸,能生成
是三元酸,能生成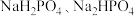 两种酸式盐和
两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸 (H3PO3)。已知:
一种正盐。磷还有一种含氧酸叫亚磷酸 (H3PO3)。已知: 与
与 反应只生成
反应只生成 和
和 两种盐。那么
两种盐。那么 为
为___________ (填“正盐”或“酸式盐”);写出 与少量
与少量 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(1)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是
②上述物质中既不是电解质也不是非电解质的是
③有下列三种物质:
 ;
; ;
; ;
;a.写出上述物质中的盐在熔融状态下的电离方程式
b.写出上述物质中的酸与氨水反应的离子方程式
(2)在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来;

①加水的烧杯为
②向烧杯A滴入
 溶液,溶液导电性
溶液,溶液导电性A.变强 B.变弱 C.先变弱后变强 D.先变强后变弱
③
 是三元酸,能生成
是三元酸,能生成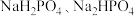 两种酸式盐和
两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸 (H3PO3)。已知:
一种正盐。磷还有一种含氧酸叫亚磷酸 (H3PO3)。已知: 与
与 反应只生成
反应只生成 和
和 两种盐。那么
两种盐。那么 为
为 与少量
与少量 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】我们的生活离不开化学。化学物质在不同的领域发挥着重要的作用。
(1)明矾是常用的一种净水剂,用离子方程式和相应的文字叙述解释其净水的原理:______________________________________________________________________ 。
(2)化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时发生如下分解反应:
2Mg5Al3(OH)19(H2O)4 27H2O+10MgO+3Al2O3
27H2O+10MgO+3Al2O3
写出该化合物作阻燃剂的两条依据:____________________ 、____________________ 。
(3)焦亚硫酸钠(Na2S2O5)是一种常见的食品抗氧化剂,焦亚硫酸钠中硫元素的化合价为__________ 。
(4)铵盐是重要的化肥,NH4Cl溶液中离子浓度大小顺序是____________ 。
(5)NaHCO3可以中和胃酸又是常用的食品添加剂,室温下pH=8的NaHCO3溶液中水电离出的OH-浓度为_____________ 。
(1)明矾是常用的一种净水剂,用离子方程式和相应的文字叙述解释其净水的原理:
(2)化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时发生如下分解反应:
2Mg5Al3(OH)19(H2O)4
 27H2O+10MgO+3Al2O3
27H2O+10MgO+3Al2O3写出该化合物作阻燃剂的两条依据:
(3)焦亚硫酸钠(Na2S2O5)是一种常见的食品抗氧化剂,焦亚硫酸钠中硫元素的化合价为
(4)铵盐是重要的化肥,NH4Cl溶液中离子浓度大小顺序是
(5)NaHCO3可以中和胃酸又是常用的食品添加剂,室温下pH=8的NaHCO3溶液中水电离出的OH-浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,盐碱地呈碱性的原因:_______ (试用化学方程式表示,下同);农业上用石膏降低其碱性的反应原理:_______ 。
(2)Na2CO3、NaHCO3溶液中微粒种类_______ 填(“相同”或“不相同”),NaHCO3溶液中c(H2CO3)_______ c(CO ) 填(“>”、“=”或“<”)。
) 填(“>”、“=”或“<”)。
(3)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=_______ 。
(4)25℃时,将amol·L-1氨水与0.01mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显_______ (填“酸”“碱”或“中”)性,用含a的代数式表示NH3·H2O的电离常数Kb=_______ 。
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,盐碱地呈碱性的原因:
(2)Na2CO3、NaHCO3溶液中微粒种类
 ) 填(“>”、“=”或“<”)。
) 填(“>”、“=”或“<”)。(3)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=
(4)25℃时,将amol·L-1氨水与0.01mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
①0.1 mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______ c(HCO3-)(填“>”、“<”或“=”)。
②常温下,物质的量浓度相同的三种溶液:A.CH3COONa B.NaCN C.Na2CO3,其pH由大到小的顺序是________ (填编号)。
③将少量CO2通入NaCN溶液,反应的离子方程式是__________ 。
④室温下,-定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是______ ,溶液中c(CH3COO-)/c(CH3COOH) =________ 。
(2)某温度下, pH=3的盐酸中[OH-]=10-9 mol/L. 该温度下, pH=2的H2SO4与pH=11的NaOH混合后pH变为9,则硫酸与氢氧化钠的体积比为______ .
(3)室温下,用0.100 mol/L盐酸溶液滴定20.00mL 0.l00mol/L 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。

①d点所示的溶液中离子浓度由大到小的顺序依次为_____ 。
②b点所示的溶液中c(NH4+)-c(NH3·H2O)=______ (写出准确数值)。
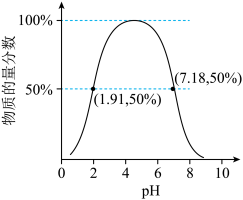
(4)在SO2溶于水形成的二元弱酸溶液中,含S元素的某微粒占所有含S元素微粒的物质的量分数与溶液pH的关系如下图所示,该微粒的化学式为_______ ;该二元弱酸的一级电离常数为Ka1,则pKa1=-lgKa1≈____ 。
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka = 1.8×10-5 | Ka=4.3×l0-10 | Ka1=5.0×l0-7 Ka2=5.6×l0-11 |
①0.1 mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)
②常温下,物质的量浓度相同的三种溶液:A.CH3COONa B.NaCN C.Na2CO3,其pH由大到小的顺序是
③将少量CO2通入NaCN溶液,反应的离子方程式是
④室温下,-定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
(2)某温度下, pH=3的盐酸中[OH-]=10-9 mol/L. 该温度下, pH=2的H2SO4与pH=11的NaOH混合后pH变为9,则硫酸与氢氧化钠的体积比为
(3)室温下,用0.100 mol/L盐酸溶液滴定20.00mL 0.l00mol/L 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。

①d点所示的溶液中离子浓度由大到小的顺序依次为
②b点所示的溶液中c(NH4+)-c(NH3·H2O)=
(4)在SO2溶于水形成的二元弱酸溶液中,含S元素的某微粒占所有含S元素微粒的物质的量分数与溶液pH的关系如下图所示,该微粒的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求完成下列方程式的书写
(1) 溶液显碱性的离子方程式
溶液显碱性的离子方程式_______
(2)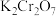 溶液中存在的化学平衡的离子方程式
溶液中存在的化学平衡的离子方程式_______
(3)硫代硫酸钠溶液与稀硫酸反应的化学方程式_______
(4)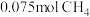 在常温常压下完全燃烧放出66kJ的热量,写出
在常温常压下完全燃烧放出66kJ的热量,写出 燃烧热的热化学方程式
燃烧热的热化学方程式_______ 。
(1)
 溶液显碱性的离子方程式
溶液显碱性的离子方程式(2)
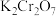 溶液中存在的化学平衡的离子方程式
溶液中存在的化学平衡的离子方程式(3)硫代硫酸钠溶液与稀硫酸反应的化学方程式
(4)
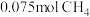 在常温常压下完全燃烧放出66kJ的热量,写出
在常温常压下完全燃烧放出66kJ的热量,写出 燃烧热的热化学方程式
燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)常温下,氯化铵的水溶液pH_____ 7(选填“>”、“=”或“<”),其原因为_____ (用离子方程式表示),下列措施能使溶液中c(NH4+)增大是_____ 。
①通入HCl气体 ②加入Na2CO3固体 ③加入NaOH固体 ④加热
(2)已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,现向AgCl悬浊液中滴加KI溶液,可观察到的现象为_____ 。
(1)常温下,氯化铵的水溶液pH
①通入HCl气体 ②加入Na2CO3固体 ③加入NaOH固体 ④加热
(2)已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,现向AgCl悬浊液中滴加KI溶液,可观察到的现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ、下列物质中:A.KI(s) B.C2H5OH(l) C.Cl2(g) D.CH3COOH(l) E.BaSO4(s) F.NaHSO4(s) G.石墨(s) H.蔗糖(s) I.NaOH(l)
(1)属于非电解质的是____________ (填序号,下同),属于强电解质的是____________ ,属于弱电解质的是____________ 。
(2)能直接导电的是________________ ,能溶于水,且水溶液能导电的是________________ 。
Ⅱ、 根据下列事实,完成相关的离子方程式或电离方程式
(1)Na2S溶液使酚酞显红色_________________________________ 。
(2)硫酸铝钾[明矾KAl(SO4)2·12H2O]可以作净水剂_______________________________ 。
(1)属于非电解质的是
(2)能直接导电的是
Ⅱ、 根据下列事实,完成相关的离子方程式或电离方程式
(1)Na2S溶液使酚酞显红色
(2)硫酸铝钾[明矾KAl(SO4)2·12H2O]可以作净水剂
您最近一年使用:0次



