铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有Al2O3、Fe2O3、FeO、SiO2等)来制备绿矾(FeSO4·7H2O)和氧化铝,其工艺流程如图:
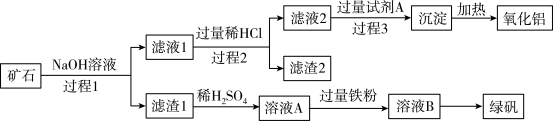
回答下列问题:
(1)滤渣1的成分是___ ,举例说明滤渣2的用途___ 。
(2)用离子方程式表示溶液A加入过量铁粉的目的是___ 。
(3)写出由滤液1生成滤液2的离子方程式___ 。
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有___ 。
(5)由溶液B得到绿矾的具体操作为___ 、过滤、洗涤和干燥。
(6)过程3需要加入的试剂A是___ ,写出此过程的离子方程式___ 。

回答下列问题:
(1)滤渣1的成分是
(2)用离子方程式表示溶液A加入过量铁粉的目的是
(3)写出由滤液1生成滤液2的离子方程式
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有
(5)由溶液B得到绿矾的具体操作为
(6)过程3需要加入的试剂A是
更新时间:2020-04-03 18:17:53
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】从某废催化剂(含ZnO、CuO、Fe2O3、石墨及MnO2等)中回收金属并制取活性氧化锌的工艺流程如下(已知:Zn及其氧化物、氢氧化物的性质与Al及其相应化合物性质类似):
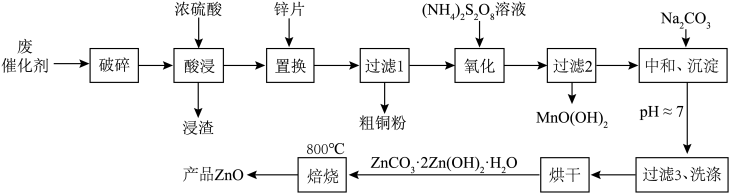
(1)废催化剂“破碎”的目的是____________________________________________ 。
(2)“氧化”时Mn2+被氧化的离子方程式为_________________________________ 。
(3)“中和、沉淀”时,若pH过高,则碱式碳酸锌的产率偏小。写出其反应的离子方程式(任写一个即可):____________________________________________ 。
(4)测得“粗铜粉”中铜的质量分数的实验步骤如下:
I.准确称取粗铜粉mg,加入足量盐酸和H2O2溶液使其完全溶解。
Ⅱ.将溶液煮沸1~2min,除去过量的H2O2。
Ⅲ.滴入铁掩蔽剂排除Fe3+的干扰。然后加入稍过量的KI溶液(反应:2Cu2++4I-=2CuI↓+I2),再加入几滴淀粉溶液作指示剂,用 c mol ·L-1Na2S2O3标准溶液滴定至蓝色消失(I2+2S2O32-=2I-+S4O62-)且半分钟内不变色,共消耗Na2S2O3标准溶液VmL。
①铜的质量分数为______________________ 。
②缺少步骤Ⅱ哙会使测得的铜的质量分数___________ (填“偏大”、“偏小”、或“不变”)

(1)废催化剂“破碎”的目的是
(2)“氧化”时Mn2+被氧化的离子方程式为
(3)“中和、沉淀”时,若pH过高,则碱式碳酸锌的产率偏小。写出其反应的离子方程式(任写一个即可):
(4)测得“粗铜粉”中铜的质量分数的实验步骤如下:
I.准确称取粗铜粉mg,加入足量盐酸和H2O2溶液使其完全溶解。
Ⅱ.将溶液煮沸1~2min,除去过量的H2O2。
Ⅲ.滴入铁掩蔽剂排除Fe3+的干扰。然后加入稍过量的KI溶液(反应:2Cu2++4I-=2CuI↓+I2),再加入几滴淀粉溶液作指示剂,用 c mol ·L-1Na2S2O3标准溶液滴定至蓝色消失(I2+2S2O32-=2I-+S4O62-)且半分钟内不变色,共消耗Na2S2O3标准溶液VmL。
①铜的质量分数为
②缺少步骤Ⅱ哙会使测得的铜的质量分数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】利用铝热炼镁还原渣[Al、Ca(AlO2)2、Al2O3、MgO及少量不能被碱液溶出的尖晶石型铝的化合物等]制取Al(OH)3的工艺流程如下:
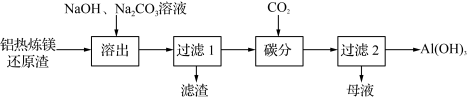
(1) “滤渣”成分包括:水合铝酸钙、尖晶石型铝的化合物、不含铝的化合物______________ (写两种物质的化学式)。
(2) “溶出”时,在适当条件下,铝及其大部分含铝化合物以NaAlO2溶出。
①金属Al与NaOH溶液反应的化学方程式为________________________________ 。
②其他条件相同时,Na2CO3、NaOH溶液的浓度对铝的溶出率的影响如图所示:
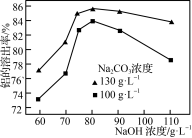
NaOH溶液浓度一定时,130 g·L-1的Na2CO3溶液对铝的溶出率比100 g·L-1的大,这是因为______________ (从平衡移动角度分析);Na2CO3溶液浓度一定时,当NaOH溶液浓度大于80 g·L-1,铝的溶出率随NaOH溶液浓度增大而减小,可能原因是______________ 。
(3) “碳分”时,溶液与过量CO2反应的离子方程式为________________________ 。
(4) “过滤2”的母液经再生处理可返回“溶出”工序循环使用,再生的方法是____________ 。

(1) “滤渣”成分包括:水合铝酸钙、尖晶石型铝的化合物、不含铝的化合物
(2) “溶出”时,在适当条件下,铝及其大部分含铝化合物以NaAlO2溶出。
①金属Al与NaOH溶液反应的化学方程式为
②其他条件相同时,Na2CO3、NaOH溶液的浓度对铝的溶出率的影响如图所示:

NaOH溶液浓度一定时,130 g·L-1的Na2CO3溶液对铝的溶出率比100 g·L-1的大,这是因为
(3) “碳分”时,溶液与过量CO2反应的离子方程式为
(4) “过滤2”的母液经再生处理可返回“溶出”工序循环使用,再生的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某铝土矿中主要含有Al2O3、Al(OH)3、AlO(OH),还含有Fe2O3等杂质。利用拜耳法生产氧化铝的流程如图所示:
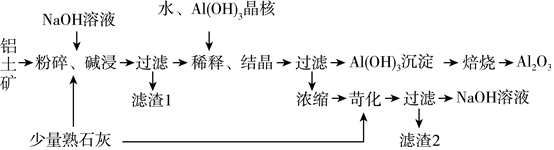
请回答下列问题:
(1)粉碎后的铝土矿碱浸时应在高温下进行,其目的是_______ 。
(2)AlO(OH)与NaOH溶液反应的化学方程式为___________ 。
(3)在稀释、结晶过程中,稀释的目的是_____________ ;加Al(OH)3晶核的目的是促进Al(OH)3的析出。上述“稀释、结晶”工艺,也可用通入足量的________ 气体的方法来代替。
(4)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化反应除去,写出苛化反应的化学方程式:__________ 。
(5)该生产流程能实现________ (填化学式)的循环利用。

请回答下列问题:
(1)粉碎后的铝土矿碱浸时应在高温下进行,其目的是
(2)AlO(OH)与NaOH溶液反应的化学方程式为
(3)在稀释、结晶过程中,稀释的目的是
(4)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化反应除去,写出苛化反应的化学方程式:
(5)该生产流程能实现
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铁是人类比较早使用的金属之一。完成下列问题:
Ⅰ.电子工业中用30%的FeCl3 溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程如图所示。
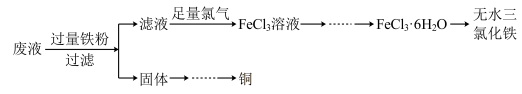
(1)FeCl3 溶液蚀刻铜箔反应的离子方程式为:___________________________ ;
(2)滤液中存在较多的阳离子是____________________ ;
(3)以下试剂也可以替代氯气完成转化,最好选用的是________ (填序号)。
a.酸性KMnO4溶液 b.溴水 c.H2O2 溶液
Ⅱ.某氯化铁样品中含有少量FeCl2杂质,现要测定其中铁元素的质量分数,实验步骤如下:

(4)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有_________________________ (填仪器名称)。
(5)写出②加入过量氨水的离子方程式:_____________________ 。
(6)样品中铁元素的质量分数为________________ 。
(7)若沉淀灼烧不充分,对最终测量结果的影响:________________ (填“偏大”“偏小”或“无影响”)。
Ⅰ.电子工业中用30%的FeCl3 溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程如图所示。

(1)FeCl3 溶液蚀刻铜箔反应的离子方程式为:
(2)滤液中存在较多的阳离子是
(3)以下试剂也可以替代氯气完成转化,最好选用的是
a.酸性KMnO4溶液 b.溴水 c.H2O2 溶液
Ⅱ.某氯化铁样品中含有少量FeCl2杂质,现要测定其中铁元素的质量分数,实验步骤如下:

(4)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有
(5)写出②加入过量氨水的离子方程式:
(6)样品中铁元素的质量分数为
(7)若沉淀灼烧不充分,对最终测量结果的影响:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某铜矿石的主要成分是Cu2O,还含有少量的Al2O3、Fe2O3和SiO2。某工厂利用此矿石炼制精铜的工艺流程如图所示(已知:Cu2O+2H+=Cu+Cu2++H2O)。
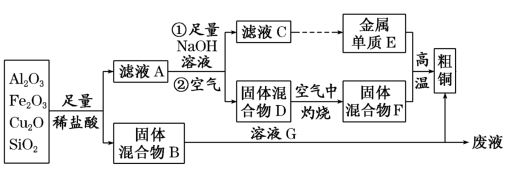
(提示:粗铜为不纯的铜)
(1)滤液A中铁元素的存在形式为_______ (填离子符号),生成该离子的离子方程式为_______ ,检验滤液A中存在该离子的试剂为_______ (填试剂名称) 。
(2)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为_______ 。
(3)高温时,SiO2与焦炭反应制得单质Si,写出其化学方程式_______ 。
(4)溶液G常用于刻蚀玻璃,则溶液G与混合物B发生反应的离子方程式是_______ 。

(提示:粗铜为不纯的铜)
(1)滤液A中铁元素的存在形式为
(2)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为
(3)高温时,SiO2与焦炭反应制得单质Si,写出其化学方程式
(4)溶液G常用于刻蚀玻璃,则溶液G与混合物B发生反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】炼锌厂产生的工业废渣——锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4·7H2O和金属镉是一个有益的尝试,其流程如下:
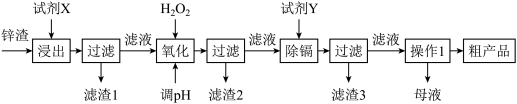
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。
试回答下列问题:
(1)“浸出”时用到的“试剂X”为____________ (填名称)。
(2)写出“氧化”过程的离子方程式_______________ 。
(3)“调pH”过程可以选用__________。(从以下选项选择, 填序号)
(4)“滤渣2”的主要成分是______________ (填化学式,下同)。
(5)“试剂Y”是______________ ;“滤渣3”的成分为____________ 。
(6)“操作1”的方法是_________ ;在“操作1”时,必须采取的实验措施是__________ 。

已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。
试回答下列问题:
(1)“浸出”时用到的“试剂X”为
(2)写出“氧化”过程的离子方程式
(3)“调pH”过程可以选用__________。(从以下选项选择, 填序号)
| A.H2SO4 |
| B.ZnO |
| C.NaOH |
(5)“试剂Y”是
(6)“操作1”的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】以某工业副产物盐泥[主要成分为Mg(OH)2,还含有少量Al(OH)3、FeCO3、MnCO3、SiO2、CaCO3等]为原料制备防火材料MgSO4·7H2O的工艺流程如图:
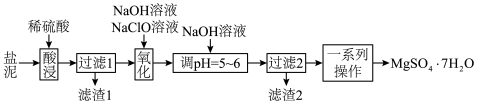
回答下列问题:
(1)以MgSO4为原料可制备阴、阳离子个数比为1:1的化合物MgC2。已知MgC2中各元素原子都达到了稳定结构,则MgC2的电子式为__ 。
(2)“酸浸”时,FeCO3与稀硫酸反应的化学方程式为__ 。滤渣1的主要成分为SiO2和__ (填化学式);为了提高浸取率,除了适当增大稀硫酸的浓度和升温外,还可采取的措施有__ (写出两点)。
(3)“氧化”时,次氯酸钠溶液将MnSO4氧化为MnO2的离子方程式为__ ;滤渣2的主要成分为MnO2和__ 、__ (填化学式)。
(4)“一系列操作”主要是__ 。
(5)一种碱式碳酸镁[4MgCO3·Mg(OH)2·5H2O]可用作防火保温材料,用化学方程式说明其可做防火材料的原理:__ 。

回答下列问题:
(1)以MgSO4为原料可制备阴、阳离子个数比为1:1的化合物MgC2。已知MgC2中各元素原子都达到了稳定结构,则MgC2的电子式为
(2)“酸浸”时,FeCO3与稀硫酸反应的化学方程式为
(3)“氧化”时,次氯酸钠溶液将MnSO4氧化为MnO2的离子方程式为
(4)“一系列操作”主要是
(5)一种碱式碳酸镁[4MgCO3·Mg(OH)2·5H2O]可用作防火保温材料,用化学方程式说明其可做防火材料的原理:
您最近一年使用:0次
【推荐2】钴元素是一种重要的战略资源,一种有机物净化钴渣梯级分离与富集钴新工艺如图。
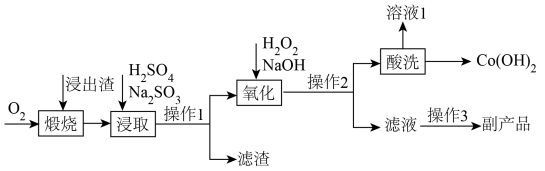
已知:用有机物净化钴渣后钴主要以有机整合物状态存在,在水溶液中难溶,可以水洗预处理得到浸出渣,进一步再继续处理富集钴,浸出渣中还含有Zn、Fe、Cd(与Zn同族)等元素。回答下列问题:
(1)“煅烧”的主要目的是________ 。
(2)“浸取”过程中发生氧化还原反应的离子方程式是________ 。操作2是________ ,得到的固体物质中含有________ (填化学式,下同);若副产品为含结晶水的固体,则其主要成分为_______ 。
(3)当溶液中可溶组分浓度c≤1.0×10-5mol•L-1时,可认为已除尽。
已知:①Ksp[Co(OH)3]=1×10-44
②金属离子开始沉淀和沉淀完全的pH数据如表所示:
则“酸洗”时溶液pH的理论范围为________ 。

已知:用有机物净化钴渣后钴主要以有机整合物状态存在,在水溶液中难溶,可以水洗预处理得到浸出渣,进一步再继续处理富集钴,浸出渣中还含有Zn、Fe、Cd(与Zn同族)等元素。回答下列问题:
(1)“煅烧”的主要目的是
(2)“浸取”过程中发生氧化还原反应的离子方程式是
(3)当溶液中可溶组分浓度c≤1.0×10-5mol•L-1时,可认为已除尽。
已知:①Ksp[Co(OH)3]=1×10-44
②金属离子开始沉淀和沉淀完全的pH数据如表所示:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.5 | 3.3 |
| Cd2+ | 7.2 | 9.5 |
| Zn2+ | 6.2 | 8.0 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】ⅰ NaOH溶液可用于多种气体的处理。
(1) 是温室气体,可用NaOH溶液吸收得到
是温室气体,可用NaOH溶液吸收得到 或
或 。
。
① 俗称纯碱,因
俗称纯碱,因 水解而使其水溶液呈碱性,写出
水解而使其水溶液呈碱性,写出 第一步水解的离子方程式:
第一步水解的离子方程式:_______ 。
已知25℃时, 第一步水解的平衡常数
第一步水解的平衡常数 ,当溶液中
,当溶液中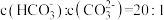 时,溶液的pH=
时,溶液的pH=______ 。
②泡沫灭火器中通常装有 溶液和
溶液和 溶液,请写出这两种溶液混合时的离子反应方程式:
溶液,请写出这两种溶液混合时的离子反应方程式:______ 。
ⅱ电子工业中,常用 溶液作为印刷电路铜板蚀刻液.请按要求回答下列问题:
溶液作为印刷电路铜板蚀刻液.请按要求回答下列问题:
(2)若向 溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该过程中调节溶液的pH为5,则
溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该过程中调节溶液的pH为5,则
______  。(已知:
。(已知: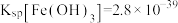 )
)
(3)某探究小组设计如图所示线路处理废液和资源回收:
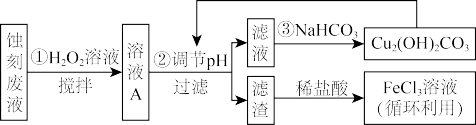
①用足量 溶液蚀刻铜板后的废液中含有的金属阳离子有
溶液蚀刻铜板后的废液中含有的金属阳离子有_______________________ 。
② 蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是
蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是______________________________ 。
③步骤①中加入 溶液的目的是
溶液的目的是_______________________________________________ 。
④已知:生成氢氧化物沉淀时溶液的pH如表所示:
根据表中数据推测调节溶液pH的范围是__________________ 。
(1)
 是温室气体,可用NaOH溶液吸收得到
是温室气体,可用NaOH溶液吸收得到 或
或 。
。①
 俗称纯碱,因
俗称纯碱,因 水解而使其水溶液呈碱性,写出
水解而使其水溶液呈碱性,写出 第一步水解的离子方程式:
第一步水解的离子方程式:已知25℃时,
 第一步水解的平衡常数
第一步水解的平衡常数 ,当溶液中
,当溶液中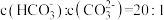 时,溶液的pH=
时,溶液的pH=②泡沫灭火器中通常装有
 溶液和
溶液和 溶液,请写出这两种溶液混合时的离子反应方程式:
溶液,请写出这两种溶液混合时的离子反应方程式:ⅱ电子工业中,常用
 溶液作为印刷电路铜板蚀刻液.请按要求回答下列问题:
溶液作为印刷电路铜板蚀刻液.请按要求回答下列问题:(2)若向
 溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该过程中调节溶液的pH为5,则
溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该过程中调节溶液的pH为5,则
 。(已知:
。(已知: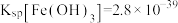 )
)(3)某探究小组设计如图所示线路处理废液和资源回收:

①用足量
 溶液蚀刻铜板后的废液中含有的金属阳离子有
溶液蚀刻铜板后的废液中含有的金属阳离子有②
 蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是
蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是③步骤①中加入
 溶液的目的是
溶液的目的是④已知:生成氢氧化物沉淀时溶液的pH如表所示:
|
|
| |
开始沉淀时 | 4.7 | 7.0 | 1.9 |
沉淀完全时 | 6.7 | 9.0 | 3.2 |
根据表中数据推测调节溶液pH的范围是
您最近一年使用:0次






