几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。(请用化学用语答题)
(1)R的元素符号为________ ; M在元素周期表中的位置为________________ 。
(2)X与M按原子个数比1∶1构成的物质为______________ 。
(3)X+、 Y2-、M2-离子半径大小顺序为____________________________________ 。
(4)将YM2通入FeCl3溶液中的离子方程式:_________________________________
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(1)R的元素符号为
(2)X与M按原子个数比1∶1构成的物质为
(3)X+、 Y2-、M2-离子半径大小顺序为
(4)将YM2通入FeCl3溶液中的离子方程式:
更新时间:2020-04-03 12:52:22
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】NaBH4(硼氢化钠)是典型的离子化合物,在有机反应中可将醛、酮变为醇。
(1)硼氢化钠与水反应的离子方程式是BH4—+2H2O=BO2—+4H2↑,该反应中氧化剂是____________ ,生成1mol H2时转移电子的数目是_____________________ 。
(2)已知HBO2是弱酸,溶液的酸性对硼氢化钠与水的反应速率有影响,酸性越强,其反应速率越____ ,这是因为____ 。
(3)硼氢化钠能把许多金属离子还原为金属单质,为抑制它与水的反应,反应在________ (填“酸性”“中性”或“碱性”)条件下进行,试完成并配平金离子(Au3+)被硼氢化钠还原的离子方程式:____ Au3++____ BH4—+__________ =____ Au↓+____ BO2— +__________ 。
(1)硼氢化钠与水反应的离子方程式是BH4—+2H2O=BO2—+4H2↑,该反应中氧化剂是
(2)已知HBO2是弱酸,溶液的酸性对硼氢化钠与水的反应速率有影响,酸性越强,其反应速率越
(3)硼氢化钠能把许多金属离子还原为金属单质,为抑制它与水的反应,反应在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】海洋中蕴含丰富的资源,利用海水提取淡水、溴、镁和碘的部分过程如图所示:

(1)海水中部分离子的含量如下:
其中,Mg2+的物质的量浓度是________ mol·L-1。
(2)滤液中通入Cl2后发生反应的离子方程式为________ 。
(3)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是________ (用离子方程式表示)。
(4)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为________ L(忽略Cl2的溶解)。
(5)由无水MgCl2制取Mg的化学方程式为________ 。

(1)海水中部分离子的含量如下:
| 成分 | 含量(mg/L) | 成分 | 含量(mg/L) |
| Na+ | 10560 | Cl- | 18980 |
| Mg2+ | 1272 | Br- | 64 |
| Ca2+ | 400 | SO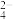 | 2560 |
(2)滤液中通入Cl2后发生反应的离子方程式为
(3)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是
(4)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为
(5)由无水MgCl2制取Mg的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】四氯化锡(SnCl4),常温下为无色液体,易水解。某研究小组利用氯气与硫渣反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。
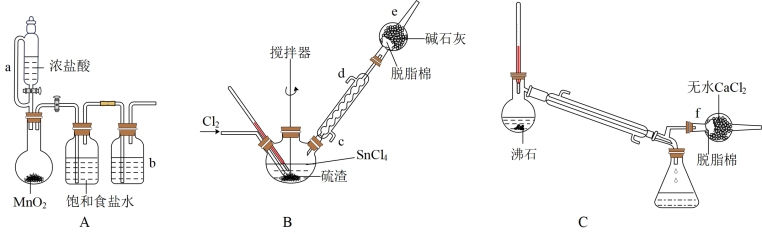
硫渣的化学组成
氯气与硫渣反应相关产物的熔沸点
请回答以下问题:
(1)A装置中,盛浓盐酸装置中a管的作用是______ ,b瓶中的试剂是________ 。
(2)氮气保护下,向B装置的三颈瓶中加入适量SnCl4浸没硫渣,通入氯气发生反应。
①生成SnCl4的化学反应方程式为_______ 。
②其中冷凝水的入口是_______ ,e中试剂使用碱石灰而不用无水氯化钙的原因是_______ 。
③实验中所得固体渣经过处理,可回收的主要金属有______ 和_______ 。
(3)得到的粗产品经C装置提纯,应控制温度为_______ ℃。

硫渣的化学组成
| 物质 | Sn | Cu2S | Pb | As | Sb | 其他杂质 |
| 质量分数/% | 64.43 | 25.82 | 7.34 | 1.23 | 0.37 | 0.81 |
| 物质 性质 | SnCl4 | CuCl | PbCl2 | AsCl3 | SbCl3 | S |
| 熔点/℃ | -33 | 426 | 501 | -18 | 73 | 112 |
| 沸点/℃ | 114 | 1490 | 951 | 130 | 221 | 444 |
(1)A装置中,盛浓盐酸装置中a管的作用是
(2)氮气保护下,向B装置的三颈瓶中加入适量SnCl4浸没硫渣,通入氯气发生反应。
①生成SnCl4的化学反应方程式为
②其中冷凝水的入口是
③实验中所得固体渣经过处理,可回收的主要金属有
(3)得到的粗产品经C装置提纯,应控制温度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。
请回答:
(1)这九种元素分别是①_______ (填元素符号,下同)、②_______ 、③_______ 、④_______ 、⑤_______ 、⑥_______ 、⑦_______ 、⑧_______ 、⑨_______ ,其中化学性质最不活泼的是_______ 。
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是_______ (填化学式)。
(3)①、②、③三种元素按原子半径由大到小的顺序依次为_______ (填元素符号)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
(1)这九种元素分别是①
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是
(3)①、②、③三种元素按原子半径由大到小的顺序依次为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有部分短周期主族元素的有关信息,如表:
(1)Z在周期表中的位置是___ 。Y的最外电子层排布式是__ ,它与T的最高价氧化物对应水化物反应的化学方程式___ 。
(2)在短周期主族元素中,X元素与其相邻元素的原子半径从小到大的顺序是__ (写元素符号)。
(3)W形成的一种单质,其式量为256,易溶于CS2,该单质的化学式为__ ,它属于__ 晶体(写晶体类型)。
(4)如图为Z元素所在周期气态氢化物R—H键的键能大小,则该周期元素气态氢化物键能大小与键长的关系为___ (用文字简述)。
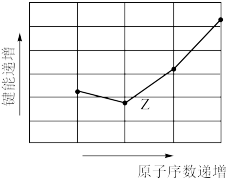
| 元素编号 | T | X | Y | Z | W |
| 元素的性质或原子结构情况 | 核外共有11种运动状态不同的电子 | M层上的电子数比次外层少1个 | 第三周期元素形成的简单离子中半径最小 | 若低温蒸发液态空气,因其沸点较低可先获得它的单质 | 核外有5种不同能量的电子且其中有两个未成对的电子 |
(2)在短周期主族元素中,X元素与其相邻元素的原子半径从小到大的顺序是
(3)W形成的一种单质,其式量为256,易溶于CS2,该单质的化学式为
(4)如图为Z元素所在周期气态氢化物R—H键的键能大小,则该周期元素气态氢化物键能大小与键长的关系为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
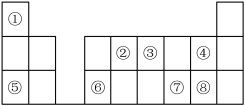
【推荐3】下图是元素周期表的一部分。按要求填写下列空白:______ 。
(2)①~⑧元素的最高价氧化物中,具有两性的是_______ (填化学式)。
(3)元素⑦的最简单气态氢化物的电子式是_______ ;元素③形成单质的电子式_____ 。
(4)④、⑤、⑥、⑦对应简单离子的半径最小的是_______ (填离子符号)。
(5)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式______ 。
(6)下列方案中不能证明非金属性⑧比⑦强的是_____(填选项字母)。
(2)①~⑧元素的最高价氧化物中,具有两性的是
(3)元素⑦的最简单气态氢化物的电子式是
(4)④、⑤、⑥、⑦对应简单离子的半径最小的是
(5)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式
(6)下列方案中不能证明非金属性⑧比⑦强的是_____(填选项字母)。
| A.最高价氧化物对应水化物的酸性⑧比⑦的强 |
| B.单质与变价金属反应,产物的价态⑧比⑦的高 |
| C.简单气态氢化物对应水溶液的酸性⑧比⑦的强 |
| D.⑧的单质可将⑦的单质从其化合物中置换出来 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有X、Y、Z、M、R、Q六种短周期的主族元素,部分信息如下表所示:
请回答下列问题:
(1)R在元素周期表中的位置是_______ 。
(2)根据表中数据推测,Y的原子半径的最小范围是_______ <r(Y)<_______ (填数字,不必注明单位)。
(3)Z、M、Q的简单离子的半径由大到小的顺序为_______ (用离子符号表示)。
(4)由元素X、M、Z组成的化合物属于_______ 化合物(填“共价”或“离子”)。写出Z2M2的电子式_______ ,若Z2M2与X2M充分反应后,生成的气体在标准状况下的体积为11.2L,则反应转移的电子数目为_______ 。
(5)下列事实能作为比较元素Y与R的非金属性相对强弱依据的是_______(选填字母序号)。
(6)写出R的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式_______ 。
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.160 | ||
| 主要化合价 | -4、+4 | -2 | -1、+7 | |||
| 其它信息 | 某种核素无中子 | 常用的半导体材料 | 短周期主族元素中原子半径最大 | 次外层电子数是最外层电子数的4倍 |
(1)R在元素周期表中的位置是
(2)根据表中数据推测,Y的原子半径的最小范围是
(3)Z、M、Q的简单离子的半径由大到小的顺序为
(4)由元素X、M、Z组成的化合物属于
(5)下列事实能作为比较元素Y与R的非金属性相对强弱依据的是_______(选填字母序号)。
| A.常温下Y的单质呈固态,R的单质呈气态 |
| B.稳定性:XR>YX4 |
| C.Y与R形成的化合物中Y呈正价 |
| D.酸性HR>H2YO3 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表所列是五种短周期元素的原子半径及主要化合价(已知铍的原子半径为0.089 nm)。
(1)用元素代号标出它们在周期表中对应位置(以下为周期表的一部分)___________ 。
(2)B元素处于周期表中第________ 周期第________ 族。
(3)C、D的简单离子的半径由大到小顺序为_________ (填离子符号)。
(4)上述五种元素的最高价氧化物对应的水化物中酸性最强的是________________ (填化学式)。
(5)C、E形成的化合物为________________ (填化学式)。
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -2 |
(1)用元素代号标出它们在周期表中对应位置(以下为周期表的一部分)
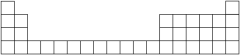
(2)B元素处于周期表中第
(3)C、D的简单离子的半径由大到小顺序为
(4)上述五种元素的最高价氧化物对应的水化物中酸性最强的是
(5)C、E形成的化合物为
您最近一年使用:0次
【推荐1】X、Y、Z、W、R是原子序数依次增大的前20号主族元素.X元素的一种原子核内只有质子,没有中子;Y的一种核素14Y用于考古时测定一些文物的年代;Z的最高价氧化物的水化物显两性;W的单质是一种黄绿色气体;R电子层数是最外层电子数的两倍.回答下列问题:
(1)R在周期表中的位置是_______ ,14Y的原子中,中子数与质子数的差为_______ .
(2)Y2X4分子中在同一平面上的原子数为_______ ,RW2的电子式是_______ .
(3)ZW3溶液呈酸性的原因是(用离子方程式表示)_______ .
(4)某传感器可以检测空气中W2的含量,其工作原理如图所示,W2气体在多孔电极被消耗并在负极和正极之间产生电流.
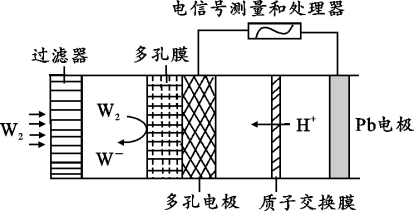
多孔电极的电极反应式为_______ ,0.01molW2气体参加反应时,理论上通过质子交换膜的H+数为_______ .
(1)R在周期表中的位置是
(2)Y2X4分子中在同一平面上的原子数为
(3)ZW3溶液呈酸性的原因是(用离子方程式表示)
(4)某传感器可以检测空气中W2的含量,其工作原理如图所示,W2气体在多孔电极被消耗并在负极和正极之间产生电流.

多孔电极的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如图是部分短周期元素的常见化合价与原子序数的关系图:
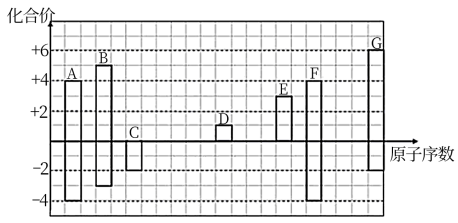
(1)元素A在周期表中的位置___________ ,元素E的名称为___________ 。
(2)写出D2C2的电子式___________ ,其所含化学键类型为___________ 。
(3)C2-、D+、G2-离子半径大小顺序是___________>___________>___________(用离子符号回答)___________ 。
(4)某同学设计实验证明A、B、F的非金属性强弱关系。
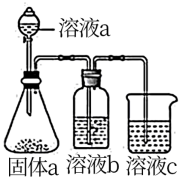
①溶液a和b分别为___________ ;___________ 。
②溶液c中的离子方程式为___________ 。
③下列事实或解释能说明非金属性B>A的是___________ 。
甲.原子半径B<A,最外层电子数B>A,核对最外层电子的束缚力B>A
乙.B的氢化物分子间有氢键,而A的氢化物分子间没有
丙.B的单质是双原子分子,常温下是气态,而A的单质常温下为固态
丁.元素的氧化物的水化物的酸性B弱于A

(1)元素A在周期表中的位置
(2)写出D2C2的电子式
(3)C2-、D+、G2-离子半径大小顺序是___________>___________>___________(用离子符号回答)
(4)某同学设计实验证明A、B、F的非金属性强弱关系。

①溶液a和b分别为
②溶液c中的离子方程式为
③下列事实或解释能说明非金属性B>A的是
甲.原子半径B<A,最外层电子数B>A,核对最外层电子的束缚力B>A
乙.B的氢化物分子间有氢键,而A的氢化物分子间没有
丙.B的单质是双原子分子,常温下是气态,而A的单质常温下为固态
丁.元素的氧化物的水化物的酸性B弱于A
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W为四种常见元素,其中X、Y、Z为短周期元素。有关信息如表所示.
(1)W在周期表中的位置为______ , 在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为
在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为______
(2)X的简单阴离子的结构示意图为______ ,X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为________
(3)Z的氧化物在通讯领域用来作______ ,工业上制备Z的单质的化学反应方程式为______ 。锗与Z是同一主族元素,它可用来制造半导体晶体管.研究表明:有机锗具有明显的抗肿瘤活性,锗不与 溶液反应但在有
溶液反应但在有 存在时可与
存在时可与 溶液反应生成锗酸盐,反应的化学方程式为
溶液反应生成锗酸盐,反应的化学方程式为_______
| 原子或分子相关信息 | 单质或化合物相关信息 | |
| X |  分子是由粗Z提纯Z的中间产物 分子是由粗Z提纯Z的中间产物 | X的最高价氧化物对应的水化物为无机酸中的最强酸 |
| Y | Y原子的最外层电子数等于电子层数 | Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 |
| Z | Z原子的最外层电子数是次外层电子数的 | Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 |
| W | W原子的最外层电子数小于4 | W的常见化合价有 、 、 , , 的稀溶液呈黄色 的稀溶液呈黄色 |
 在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为
在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为(2)X的简单阴离子的结构示意图为
(3)Z的氧化物在通讯领域用来作
 溶液反应但在有
溶液反应但在有 存在时可与
存在时可与 溶液反应生成锗酸盐,反应的化学方程式为
溶液反应生成锗酸盐,反应的化学方程式为
您最近一年使用:0次



