1 . 在含等物质的量的 和
和 混合溶液中,通入一定量的
混合溶液中,通入一定量的 ,当一半的
,当一半的 被氧化时,参与置换反应的
被氧化时,参与置换反应的 的物质的量与原
的物质的量与原 的物质的量之比为
的物质的量之比为
 和
和 混合溶液中,通入一定量的
混合溶液中,通入一定量的 ,当一半的
,当一半的 被氧化时,参与置换反应的
被氧化时,参与置换反应的 的物质的量与原
的物质的量与原 的物质的量之比为
的物质的量之比为A.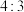 | B.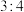 | C. | D. |
您最近一年使用:0次
2 . 某小组通过实验探究氧化还原反应的规律。
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性强弱:数值越大,氧化性越强;数值越小,还原性越强。测得几种物质的电位值如下表所示:(注意:实验中进行酸化时均用稀硫酸)
根据表中数据,回答下列问题:
(1)浓度相同的下列三种溶液,氧化性由强到弱的顺序为___________ (填序号)。
① ②酸性
②酸性 ③酸性
③酸性
(2)已知 与
与 不能共存,由此推测下列能大量共存的离子组是
不能共存,由此推测下列能大量共存的离子组是___________ 。
a. b.
b. c.
c.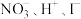 d.
d.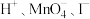
(3)向等浓度的 和FeCl2混合溶液滴加少量酸性
和FeCl2混合溶液滴加少量酸性 溶液(对应还原产物为
溶液(对应还原产物为 ),发生反应的离子方程式为
),发生反应的离子方程式为___________ 。
(4)已知常温下 遇淀粉变蓝。现往淀粉
遇淀粉变蓝。现往淀粉 溶液中逐滴加入氯水(含
溶液中逐滴加入氯水(含 ),观察到溶液先变蓝后褪色。小组同学就溶液褪色的原因,提出两种猜想,并设计如下实验进行验证。猜想1:
),观察到溶液先变蓝后褪色。小组同学就溶液褪色的原因,提出两种猜想,并设计如下实验进行验证。猜想1: 将淀粉氧化; 猜想2:
将淀粉氧化; 猜想2: 被
被 继续氧化(为
继续氧化(为 )。
)。
①实验1所用试剂a为___________ 。
②试剂b是一种可溶性含碘化合物,该反应的离子方程式为___________ 。
结合上述信息思考:对于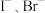 混合溶液,若控制性氧化
混合溶液,若控制性氧化 而不氧化
而不氧化 ,请提出合理的氧化方案:加入
,请提出合理的氧化方案:加入___________ 。(合理即给分)
已知:氧化还原反应电位传感器可以测量不同溶液的电位值,根据电位值大小可比较物质的氧化性/还原性强弱:数值越大,氧化性越强;数值越小,还原性越强。测得几种物质的电位值如下表所示:(注意:实验中进行酸化时均用稀硫酸)
| 物质 | FeCl3 | KMnO4(酸化) | NaNO3(酸化) | Br2 | I2 | Na2S |
| 浓度 | 0.10M(M为物质的量浓度的单位) | |||||
| 电位值/mV | 171 | 1130 | 603 | 662 | 116 | -361 |
(1)浓度相同的下列三种溶液,氧化性由强到弱的顺序为
①
 ②酸性
②酸性 ③酸性
③酸性
(2)已知
 与
与 不能共存,由此推测下列能大量共存的离子组是
不能共存,由此推测下列能大量共存的离子组是a.
 b.
b. c.
c.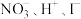 d.
d.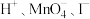
(3)向等浓度的
 和FeCl2混合溶液滴加少量酸性
和FeCl2混合溶液滴加少量酸性 溶液(对应还原产物为
溶液(对应还原产物为 ),发生反应的离子方程式为
),发生反应的离子方程式为(4)已知常温下
 遇淀粉变蓝。现往淀粉
遇淀粉变蓝。现往淀粉 溶液中逐滴加入氯水(含
溶液中逐滴加入氯水(含 ),观察到溶液先变蓝后褪色。小组同学就溶液褪色的原因,提出两种猜想,并设计如下实验进行验证。猜想1:
),观察到溶液先变蓝后褪色。小组同学就溶液褪色的原因,提出两种猜想,并设计如下实验进行验证。猜想1: 将淀粉氧化; 猜想2:
将淀粉氧化; 猜想2: 被
被 继续氧化(为
继续氧化(为 )。
)。| 序号 | 实验操作 | 试剂 | 观察实验现象 | 结论 |
| 1 | 分别取少量褪色后溶液于三支试管中,并加入对应试剂 | a | 溶液变蓝 | 猜想1不正确 |
| 2 | 淀粉溶液 | 溶液不变蓝 | 猜想2正确 | |
| 3 | b+稀H2SO4 | 溶液变蓝 |
②试剂b是一种可溶性含碘化合物,该反应的离子方程式为
结合上述信息思考:对于
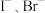 混合溶液,若控制性氧化
混合溶液,若控制性氧化 而不氧化
而不氧化 ,请提出合理的氧化方案:加入
,请提出合理的氧化方案:加入
您最近一年使用:0次
名校
解题方法
3 . 对下列图像的解释正确的是
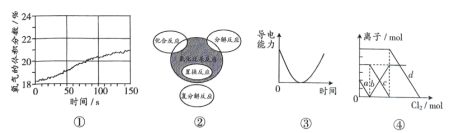

| A.图①表示强光照射氯水,氧气体积分数与时间的关系,说明在光照下,水分解生成了氧气 |
| B.过氧化钠与H2O的反应类型属于图②的阴影部分 |
| C.图③可表示向硫酸铜溶液中逐滴加入氢氧化钠溶液时,混合溶液导电能力随时间的变化 |
D.将Cl2通入FeI2和FeBr2的混合溶液中,图④中a曲线表示 随氯气加入量的变化曲线 随氯气加入量的变化曲线 |
您最近一年使用:0次
2024-02-03更新
|
75次组卷
|
2卷引用:山西省吕梁市2023-2024学年高一上学期期末调研测试化学试题
4 . 2023年9月12日,天舟五号货运飞船再人大气层。天舟五号飞船的天线用钛镍记忆合金制造,工业上用钛酸亚铁  冶炼钛的原理如下,下列有关说法正确的是
冶炼钛的原理如下,下列有关说法正确的是
①高温下:
②在氩气氛围高温中:
 冶炼钛的原理如下,下列有关说法正确的是
冶炼钛的原理如下,下列有关说法正确的是①高温下:

②在氩气氛围高温中:

A.①中化合价变化的元素为  |
B.①中每生成标况下 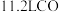 ,转移的电子数为 ,转移的电子数为  |
C.②中可以得出  得电子的能力强于 得电子的能力强于 |
D.②中氩气的作用是防止  被氧化 被氧化 |
您最近一年使用:0次
5 . 把图2中的物质补充到图1中,可得到一个完整的氧化还原型离子方程式(未配平)。
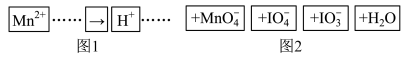
对该氧化还原反应型离子方程式,说法不正确的是
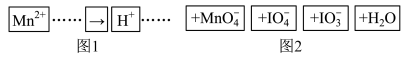
对该氧化还原反应型离子方程式,说法不正确的是
A. 作氧化剂具有氧化性 作氧化剂具有氧化性 |
| B.氧化剂和还原剂的个数之比为5:2 |
C.若有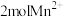 参加反应时则转移电子的个数为 参加反应时则转移电子的个数为 |
D.氧化性: |
您最近一年使用:0次
2024-02-02更新
|
105次组卷
|
2卷引用:天津市第四十七中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
6 . 按要求填空:
(1)以下为中学化学中常见的几种物质:①二氧化碳 ②熔融 KCl ③NaHSO4固体④铜 ⑤稀硫酸 ⑥澄清石灰水,其中属于电解质的有_______ (填编号,下同),属于非电解质的 有_______ ,能导电的有_______ 。
(2)高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O;该反应中氧化剂是_______ (用化学式表示,下同) ,_______ 元素被氧化,还原产物与氧化产物之比为_______ 。
(3)已知次磷酸(H3PO2)是一元弱酸,其与氢氧化钠溶液反应的离子方程式为_______ 。
(1)以下为中学化学中常见的几种物质:①二氧化碳 ②熔融 KCl ③NaHSO4固体④铜 ⑤稀硫酸 ⑥澄清石灰水,其中属于电解质的有
(2)高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O;该反应中氧化剂是
(3)已知次磷酸(H3PO2)是一元弱酸,其与氢氧化钠溶液反应的离子方程式为
您最近一年使用:0次
解题方法
7 . 在稀硫酸中有如图所示的转化:
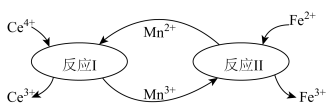
下列说法正确的是

下列说法正确的是
A.反应Ⅰ中 被氧化 被氧化 | B.氧化性: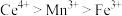 |
C.反应Ⅱ的还原剂为 | D.预测: 不可能还原 不可能还原 |
您最近一年使用:0次
8 . 向 和
和 的混合液中通入足量
的混合液中通入足量 ,溶液中部分离子的物质的量随通入
,溶液中部分离子的物质的量随通入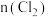 的变化如图所示。
的变化如图所示。 表示一种含氧酸根离子,且
表示一种含氧酸根离子,且 和
和 含有同一种元素。下列说法正确的是
含有同一种元素。下列说法正确的是
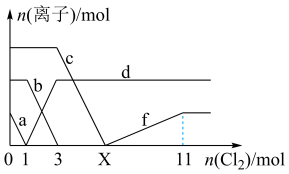
 和
和 的混合液中通入足量
的混合液中通入足量 ,溶液中部分离子的物质的量随通入
,溶液中部分离子的物质的量随通入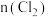 的变化如图所示。
的变化如图所示。 表示一种含氧酸根离子,且
表示一种含氧酸根离子,且 和
和 含有同一种元素。下列说法正确的是
含有同一种元素。下列说法正确的是
A. 表示 表示 的变化情况 的变化情况 | B.由图像可推断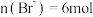 |
C.每生成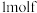 转移 转移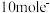 | D.原溶液中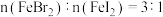 |
您最近一年使用:0次
9 . 已知常温下在溶液中发生如下反应:①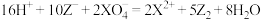 ;②
;②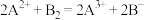 ;③
;③ 。由此判断下列说法错误的是
。由此判断下列说法错误的是
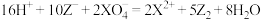 ;②
;②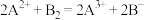 ;③
;③ 。由此判断下列说法错误的是
。由此判断下列说法错误的是A.氧化性: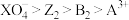 | B.反应 可以进行 可以进行 |
| C.元素在反应①中被氧化,反应③中被还原 | D.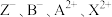 中 中 的还原性最强 的还原性最强 |
您最近一年使用:0次
名校
解题方法
10 . 向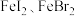 的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。下列有关说法中,正确的是
的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。下列有关说法中,正确的是
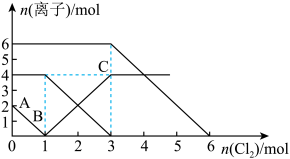
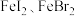 的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。下列有关说法中,正确的是
的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。下列有关说法中,正确的是
A.还原性: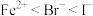 |
B.当通入 时,溶液中已发生的离子反应可表示为: 时,溶液中已发生的离子反应可表示为: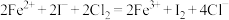 |
C.原溶液中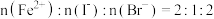 |
D.原混合溶液中 的物质的量为 的物质的量为 |
您最近一年使用:0次



