2024高三下·全国·专题练习
解题方法
1 . 乙酸是基本的有机化工原料,乙酸制氢具有重要意义,制氢过程发生如下反应:
热裂解反应Ⅰ: CH3COOH(g) 2CO (g)+ 2H2(g) ΔH1
2CO (g)+ 2H2(g) ΔH1
脱羧基反应Ⅱ:CH3COOH(g) CO2 (g)+CH4(g) ΔH2
CO2 (g)+CH4(g) ΔH2
若利用合适的催化剂发生热裂解反应Ⅰ和脱羧基反应Ⅱ,温度为TK时达到平衡,总压强为p kPa,乙酸体积分数为20%,其中热裂解反应Ⅰ消耗的乙酸占投入量的20%,脱羧基反应Ⅱ的平衡常数Kp为_____ kPa (Kp为以分压表示的平衡常数)。
热裂解反应Ⅰ: CH3COOH(g)
 2CO (g)+ 2H2(g) ΔH1
2CO (g)+ 2H2(g) ΔH1脱羧基反应Ⅱ:CH3COOH(g)
 CO2 (g)+CH4(g) ΔH2
CO2 (g)+CH4(g) ΔH2若利用合适的催化剂发生热裂解反应Ⅰ和脱羧基反应Ⅱ,温度为TK时达到平衡,总压强为p kPa,乙酸体积分数为20%,其中热裂解反应Ⅰ消耗的乙酸占投入量的20%,脱羧基反应Ⅱ的平衡常数Kp为
您最近半年使用:0次
2024高三下·全国·专题练习
2 . 一定条件下,CO2与H2反应可合成CH2=CH2,2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g),该反应分两步进行:
CH2=CH2(g)+4H2O(g),该反应分两步进行:
i.CO2(g)+H2(g) CO(g)+H2O(g) ΔH1
CO(g)+H2O(g) ΔH1
ii.2CO(g)+4H2(g) CH2=CH2(g)+2H2O(g) ΔH2
CH2=CH2(g)+2H2O(g) ΔH2
T℃,压强恒定为100kPa时,将n(CO2):n(H2)=1:3的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示:
CO2的平衡转化率为________ ,反应i的平衡常数Kp=________ (Kp是以分压表示的平衡常数,分压=总压×物质的量分数)
 CH2=CH2(g)+4H2O(g),该反应分两步进行:
CH2=CH2(g)+4H2O(g),该反应分两步进行:i.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH1
CO(g)+H2O(g) ΔH1ii.2CO(g)+4H2(g)
 CH2=CH2(g)+2H2O(g) ΔH2
CH2=CH2(g)+2H2O(g) ΔH2T℃,压强恒定为100kPa时,将n(CO2):n(H2)=1:3的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示:
| 组分 | H2 | CO | CH2=CH2 |
| 物质的量分数(%) | 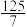 |  | 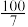 |
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
3 . 1200K时,假定体系内只有反应C40H12 (g) C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为
C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为
C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
4 . 对于基元反应,如aA+bB cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
反应Ⅰ:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
反应Ⅱ:8NH3(g)+6NO2(g) 7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
反应Ⅲ:N2(g)+O2(g)=2NO(g)ΔH3=+182.6kJ·mol-1
对于基元反应Ⅳ:2NO(g)+O2(g) 2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
(1)ΔH4=______ kJ·mol-1
(2)计算653K时的平衡常数K=______ 。
(3)653K时,若NO的浓度为0.006mol·L-1,O2的浓度为0.290mol·L-1,则正反应速率为______ mol·L-1·s-1
 cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:反应Ⅰ:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1反应Ⅱ:8NH3(g)+6NO2(g)
 7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1反应Ⅲ:N2(g)+O2(g)=2NO(g)ΔH3=+182.6kJ·mol-1
对于基元反应Ⅳ:2NO(g)+O2(g)
 2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1(1)ΔH4=
(2)计算653K时的平衡常数K=
(3)653K时,若NO的浓度为0.006mol·L-1,O2的浓度为0.290mol·L-1,则正反应速率为
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
5 . 工业上,可以采用 催化还原制备
催化还原制备 、
、 。发生反应如下:
。发生反应如下:
① (主反应);
(主反应);
② (主反应);
(主反应);
③ (副反应)。
(副反应)。
一定温度下,向总压强恒定为100kPa的反应器中充入 和
和 ,发生(4)中反应①②③,达到平衡时
,发生(4)中反应①②③,达到平衡时 转化率为50%,甲醇选择性为
转化率为50%,甲醇选择性为 ,生成
,生成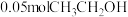 ,则反应①的平衡常数
,则反应①的平衡常数 为
为___________ 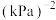 (写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数
(写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数 ,分压=总压×物质的量分数;甲醇选择性:
,分压=总压×物质的量分数;甲醇选择性: ]。
]。
 催化还原制备
催化还原制备 、
、 。发生反应如下:
。发生反应如下:①
 (主反应);
(主反应);②
 (主反应);
(主反应);③
 (副反应)。
(副反应)。一定温度下,向总压强恒定为100kPa的反应器中充入
 和
和 ,发生(4)中反应①②③,达到平衡时
,发生(4)中反应①②③,达到平衡时 转化率为50%,甲醇选择性为
转化率为50%,甲醇选择性为 ,生成
,生成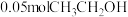 ,则反应①的平衡常数
,则反应①的平衡常数 为
为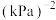 (写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数
(写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数 ,分压=总压×物质的量分数;甲醇选择性:
,分压=总压×物质的量分数;甲醇选择性: ]。
]。
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
6 . 在一定条件下 、
、 主要发生以下反应:
主要发生以下反应:
①
 kJ⋅mol-1
kJ⋅mol-1
②
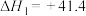 kJ⋅mol-1
kJ⋅mol-1
若在一定温度下,投料比例相同(充入物质的量之比为1∶4的 和
和 ),通入恒容密闭容器中,发生上述反应达到平衡,测得反应前容器内压强为
),通入恒容密闭容器中,发生上述反应达到平衡,测得反应前容器内压强为 ,平衡时
,平衡时 压强为
压强为 ,甲烷压强为
,甲烷压强为 。则甲烷的选择性为
。则甲烷的选择性为________ (用 、
、 、
、 中相关字母表示,下同),反应②的压强平衡常数
中相关字母表示,下同),反应②的压强平衡常数 的值为
的值为_______ 。
 、
、 主要发生以下反应:
主要发生以下反应:①

 kJ⋅mol-1
kJ⋅mol-1②

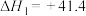 kJ⋅mol-1
kJ⋅mol-1若在一定温度下,投料比例相同(充入物质的量之比为1∶4的
 和
和 ),通入恒容密闭容器中,发生上述反应达到平衡,测得反应前容器内压强为
),通入恒容密闭容器中,发生上述反应达到平衡,测得反应前容器内压强为 ,平衡时
,平衡时 压强为
压强为 ,甲烷压强为
,甲烷压强为 。则甲烷的选择性为
。则甲烷的选择性为 、
、 、
、 中相关字母表示,下同),反应②的压强平衡常数
中相关字母表示,下同),反应②的压强平衡常数 的值为
的值为
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
7 . 在体积为 的密闭容器中,进行如下化学反应:
的密闭容器中,进行如下化学反应: ,化学平衡常数
,化学平衡常数 与温度
与温度 的关系如下表:
的关系如下表:
回答下列问题:
在 条件下,将
条件下,将 和
和 按体积比
按体积比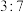 通入
通入 的恒容密闭容器中发生上述反应,
的恒容密闭容器中发生上述反应, 后反应达平衡,此时压强为
后反应达平衡,此时压强为 。该反应的分压平衡常数
。该反应的分压平衡常数
___________ 。( 为以分压表示的平衡常数,分压
为以分压表示的平衡常数,分压 总压
总压 物质的量分数)
物质的量分数)
 的密闭容器中,进行如下化学反应:
的密闭容器中,进行如下化学反应: ,化学平衡常数
,化学平衡常数 与温度
与温度 的关系如下表:
的关系如下表: | 700 | 800 | 850 | 1000 | 1200 |
 | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
在
 条件下,将
条件下,将 和
和 按体积比
按体积比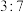 通入
通入 的恒容密闭容器中发生上述反应,
的恒容密闭容器中发生上述反应, 后反应达平衡,此时压强为
后反应达平衡,此时压强为 。该反应的分压平衡常数
。该反应的分压平衡常数
 为以分压表示的平衡常数,分压
为以分压表示的平衡常数,分压 总压
总压 物质的量分数)
物质的量分数)
您最近半年使用:0次
2023高三·全国·专题练习
解题方法
8 . 苯催化加氢制备环己烷是化工生产中的重要工艺,一定条件下,发生如下反应:
Ⅰ.主反应: (g)+3H2(g)
(g)+3H2(g)
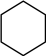 (g) ΔH1<0
(g) ΔH1<0
Ⅱ.副反应: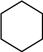 (g)
(g) 
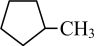 (g) ΔH2>0
(g) ΔH2>0
回答下列问题:
恒压反应器中,按照n(H2)∶n(C6H6)=4∶1投料,发生Ⅰ、Ⅱ反应,总压为p0,平衡时苯的转化率为α,环己烷的分压为p,则反应Ⅰ的Kp=___________ (列出计算式即可,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅰ.主反应:
 (g)+3H2(g)
(g)+3H2(g)
 (g) ΔH1<0
(g) ΔH1<0Ⅱ.副反应:
 (g)
(g) 
 (g) ΔH2>0
(g) ΔH2>0回答下列问题:
恒压反应器中,按照n(H2)∶n(C6H6)=4∶1投料,发生Ⅰ、Ⅱ反应,总压为p0,平衡时苯的转化率为α,环己烷的分压为p,则反应Ⅰ的Kp=
您最近半年使用:0次
2023高三·全国·专题练习
9 . 反应SO2(g)+NO2(g) SO3(g)+NO(g),若在一定温度下,将物质的量浓度均为2mol·L-1的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则在该温度下:
SO3(g)+NO(g),若在一定温度下,将物质的量浓度均为2mol·L-1的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则在该温度下:
(1)此反应的平衡常数为_____ 。
(2)在上述温度下,若SO2(g)的初始浓度增大到3mol·L-1,NO2(g)的初始浓度仍为2mol·L-1,达到化学平衡状态时,计算下列各物质的平衡浓度及SO2和NO2的平衡转化率。
①c(SO3)=_____ mol·L-1,c(SO2)=_____ mol·L-1。
②SO2的转化率为_____ ,NO2的转化率为_____ 。
 SO3(g)+NO(g),若在一定温度下,将物质的量浓度均为2mol·L-1的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则在该温度下:
SO3(g)+NO(g),若在一定温度下,将物质的量浓度均为2mol·L-1的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,则在该温度下:(1)此反应的平衡常数为
(2)在上述温度下,若SO2(g)的初始浓度增大到3mol·L-1,NO2(g)的初始浓度仍为2mol·L-1,达到化学平衡状态时,计算下列各物质的平衡浓度及SO2和NO2的平衡转化率。
①c(SO3)=
②SO2的转化率为
您最近半年使用:0次
解题方法
10 . 顺1,2二甲基环丙烷和反1,2二甲基环丙烷可发生如下转化:

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K=_______ 。

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K=
您最近半年使用:0次



