名校
1 . 某化学研究性学习小组模拟工业合成氨的反应。在容积固定为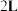 的密闭容器内充入
的密闭容器内充入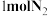 和
和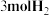 ,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下表:
,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下表:
1.请写出合成氨逆反应的平衡常数表达式:___________ 。
2.反应后的气体总物质的量是___________ 。
3.则从反应开始到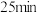 时,以
时,以 表示的平均反应速率
表示的平均反应速率
___________ 。
4.实验中, 时向容器中充入一定量
时向容器中充入一定量 ,则正反应速率
,则正反应速率___________ 。
A.增大 B.减小 C.不变
5.实验中, 时若容器体积减少一半,则平衡
时若容器体积减少一半,则平衡___________ 。
A.正向移动 B.逆向移动 C.不移动
6.改变条件能改变合成氨的反应速率,下列改变的条件中能降低反应物所需能量的是 。
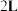 的密闭容器内充入
的密闭容器内充入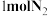 和
和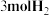 ,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下表:
,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下表:反应时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
压强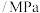 | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
2.反应后的气体总物质的量是
3.则从反应开始到
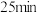 时,以
时,以 表示的平均反应速率
表示的平均反应速率
4.实验中,
 时向容器中充入一定量
时向容器中充入一定量 ,则正反应速率
,则正反应速率A.增大 B.减小 C.不变
5.实验中,
 时若容器体积减少一半,则平衡
时若容器体积减少一半,则平衡A.正向移动 B.逆向移动 C.不移动
6.改变条件能改变合成氨的反应速率,下列改变的条件中能降低反应物所需能量的是 。
| A.温度 | B.压强 | C.浓度 | D.催化剂 |
您最近半年使用:0次
名校
解题方法
2 . 一定温度下体积为 的密闭容器中:
的密闭容器中: 的
的 ,在此温度下该容器中含有
,在此温度下该容器中含有 、
、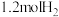 、
、 、
、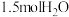 ,判断此时反应
,判断此时反应 和
和 的相对大小并说明理由
的相对大小并说明理由_______ 。
 的密闭容器中:
的密闭容器中: 的
的 ,在此温度下该容器中含有
,在此温度下该容器中含有 、
、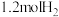 、
、 、
、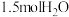 ,判断此时反应
,判断此时反应 和
和 的相对大小并说明理由
的相对大小并说明理由
您最近半年使用:0次
解题方法
3 . 研究和深度开发CO、CO2的应用对环境保护具有重要的意义。请回答下列问题:
I.在2L恒容密闭容器中,充入10molCO2和32molH2,在催化剂、200°C的条件下发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)。部分反应物和产物随时间变化如下图所示:
CH3OH(g)+H2O(g)。部分反应物和产物随时间变化如下图所示:___________
(2)该温度下反应的化学平衡常数为___________
(3)下列情况能说明该反应达到化学平衡状态的是___________ (填字母)。
A.单位时间内消耗1molCO2,同时生成1molCH3OH
B.密闭容器中气体的压强不再改变
C.CO2、H2、CH3OH浓度之比为1:3:1的状态
D.密闭容器内混合气体的平均摩尔质量不发生变化
E.密闭容器内混合气体的密度不再改变
II.CO和H2也可合成甲醇:CO(g)+2H2(g) CH3OH(g),△H<0
CH3OH(g),△H<0
(4)下列措施中能增大反应速率且利于平衡正向移动的是___________
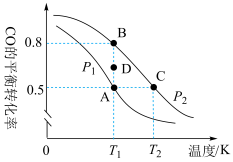
(5)一定条件下向2L的恒容密闭容器中充入1molCO和2molH2发生反应,CO的平衡转化率与温度、压强的关系如图所示:___________ p2(“>”“<”或“=”);A、B、C三点平衡常数KA、KB、KC的大小关系是___________ ;在温度为T2,压强为p2的条件下达平衡后,再加入0.5molCO、1molH2和0.5molCH3OH,化学平衡会向___________ (填“正反应”或“逆反应”)方向移动。
I.在2L恒容密闭容器中,充入10molCO2和32molH2,在催化剂、200°C的条件下发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。部分反应物和产物随时间变化如下图所示:
CH3OH(g)+H2O(g)。部分反应物和产物随时间变化如下图所示: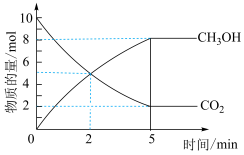
(2)该温度下反应的化学平衡常数为
(3)下列情况能说明该反应达到化学平衡状态的是
A.单位时间内消耗1molCO2,同时生成1molCH3OH
B.密闭容器中气体的压强不再改变
C.CO2、H2、CH3OH浓度之比为1:3:1的状态
D.密闭容器内混合气体的平均摩尔质量不发生变化
E.密闭容器内混合气体的密度不再改变
II.CO和H2也可合成甲醇:CO(g)+2H2(g)
 CH3OH(g),△H<0
CH3OH(g),△H<0(4)下列措施中能增大反应速率且利于平衡正向移动的是___________
| A.升高反应温度 | B.将CH3OH与反应混合物分离 | C.使用高效催化剂 | D.增大体系压强 |
(5)一定条件下向2L的恒容密闭容器中充入1molCO和2molH2发生反应,CO的平衡转化率与温度、压强的关系如图所示:
您最近半年使用:0次
名校
解题方法
4 . 汽车尾气中含有CO、NO2等有毒气体,对汽车家装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
已知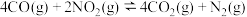
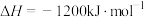
(1)该反应在___________ (填“高温、低温或任何温度”)下能自发进行。
(2)对于该反应,改变某一反应条件(温度 ),下列图象正确的是___________(填标号)。
),下列图象正确的是___________(填标号)。
(3)某实验小组模拟上述净化过程,一定温度下,在 的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲:
的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲: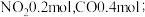 乙:
乙: ,经过一段时间后达到平衡状态。
,经过一段时间后达到平衡状态。
① 的平衡体积分数:甲
的平衡体积分数:甲___________ 乙(填“>、=、<或不确定”,下同)。
② 的平衡浓度:甲
的平衡浓度:甲___________ 乙。
③甲中 的转化率为
的转化率为 ,该反应的平衡常数为
,该反应的平衡常数为___________ 。
已知
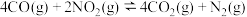
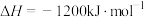
(1)该反应在
(2)对于该反应,改变某一反应条件(温度
 ),下列图象正确的是___________(填标号)。
),下列图象正确的是___________(填标号)。A.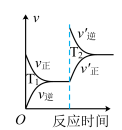 | B.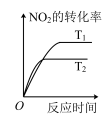 | C.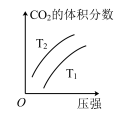 | D.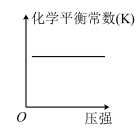 |
(3)某实验小组模拟上述净化过程,一定温度下,在
 的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲:
的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲: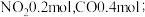 乙:
乙: ,经过一段时间后达到平衡状态。
,经过一段时间后达到平衡状态。①
 的平衡体积分数:甲
的平衡体积分数:甲②
 的平衡浓度:甲
的平衡浓度:甲③甲中
 的转化率为
的转化率为 ,该反应的平衡常数为
,该反应的平衡常数为
您最近半年使用:0次
5 . 回答下列问题。
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g)∆H<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。平衡时H2的转化率为
2NH3(g)∆H<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。平衡时H2的转化率为___________ %。
(2)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g) 2NH3(g)∆H<0,其化学平衡常数K与温度T的关系如表所示:请完成下列问题:
2NH3(g)∆H<0,其化学平衡常数K与温度T的关系如表所示:请完成下列问题:
①写出化学平衡常数K的表达式___________ 。
②试比较K1、K2的大小,K1___________ K2(填“>”、“<”或“=”);
③400℃时,当测得NH3、N2和H2物质的量分别为3mol、2mol和1mol时,则该反应的v(N2)正___________ v(N2)逆(填“>”、“<”或“=”)。
(3)平衡后,若提高H2的转化率,可以采取的措施有___________。
(1)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g)
 2NH3(g)∆H<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。平衡时H2的转化率为
2NH3(g)∆H<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。平衡时H2的转化率为(2)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)
 2NH3(g)∆H<0,其化学平衡常数K与温度T的关系如表所示:请完成下列问题:
2NH3(g)∆H<0,其化学平衡常数K与温度T的关系如表所示:请完成下列问题:| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②试比较K1、K2的大小,K1
③400℃时,当测得NH3、N2和H2物质的量分别为3mol、2mol和1mol时,则该反应的v(N2)正
(3)平衡后,若提高H2的转化率,可以采取的措施有___________。
| A.加了催化剂 | B.增大容器体积 | C.降低反应体系的温度 | D.加入一定量N2 |
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
6 . 硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑穗病,制造磁性氧化铁、铁催化剂等。回答下列问题:
(1)将 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: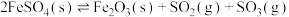 (I)。平衡时
(I)。平衡时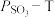 的关系如下图所示。
的关系如下图所示。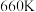 时,该反应的平衡总压
时,该反应的平衡总压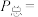
___________  、平衡常数
、平衡常数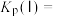
___________  。
。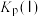 随反应温度升高而
随反应温度升高而___________ (填“增大”“减小”或“不变”)。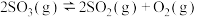 (II),平衡时
(II),平衡时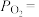
___________ (用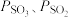 表示)。在
表示)。在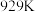 时,
时, ,则
,则
___________  ,
,
___________  (列出计算式)。
(列出计算式)。
(1)将
 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: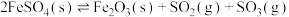 (I)。平衡时
(I)。平衡时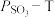 的关系如下图所示。
的关系如下图所示。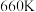 时,该反应的平衡总压
时,该反应的平衡总压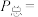
 、平衡常数
、平衡常数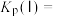
 。
。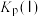 随反应温度升高而
随反应温度升高而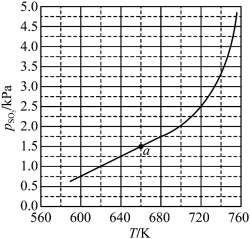
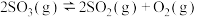 (II),平衡时
(II),平衡时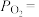
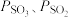 表示)。在
表示)。在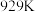 时,
时, ,则
,则
 ,
,
 (列出计算式)。
(列出计算式)。
您最近半年使用:0次
2024高三下·全国·专题练习
7 . 雾霾主要成分为灰尘、SO2、NOx和有机碳氢化合物等粒子。烟气脱硝是治理雾霾的方法之一、
(1)以臭氧为烟气脱硝剂时,脱硝过程涉及的反应之一为:2NO2(g)+O3(g)⇌N2O5(g)+O2(g)。不同温度下,控制其它条件一定,在两个恒容容器中发生该反应,相关信息如下表及图所示:
①T1___________ T2(填“<"、“>”或“无法确定”),该反应的 H
H___________ 0(填“<”或“>”)。
②0~25min内乙容器中反应的平均速率:v(NO2)=___________ 。
③T1温度下,混合气体的起始总压为p,则达到平衡时,NO2的转化率为___________ ,平衡常数Kp=___________ (以分压表示,分压=总压×物质的量分数)。
(1)以臭氧为烟气脱硝剂时,脱硝过程涉及的反应之一为:2NO2(g)+O3(g)⇌N2O5(g)+O2(g)。不同温度下,控制其它条件一定,在两个恒容容器中发生该反应,相关信息如下表及图所示:

| 容器 | 甲 | 乙 |
| 温度/K | T1 | T2 |
| 容积/L | 2 | |
| 起始充入量 | 4molNO2和2molO3 | |
 H
H②0~25min内乙容器中反应的平均速率:v(NO2)=
③T1温度下,混合气体的起始总压为p,则达到平衡时,NO2的转化率为
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
8 . 二氧化碳催化加氢制甲醇,能助力“碳达峰”,涉及反应有:
反应①
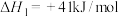
反应②
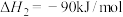
反应③

(1)在 下,
下, 和
和 按物质的量之比为
按物质的量之比为 进行投料,只发生反应①和反应③,平衡时CO和
进行投料,只发生反应①和反应③,平衡时CO和 在含碳产物中的物质的量分数及
在含碳产物中的物质的量分数及 转化率随温度的变化如图所示。
转化率随温度的变化如图所示。
___________ ( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
反应①

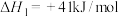
反应②

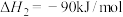
反应③


(1)在
 下,
下, 和
和 按物质的量之比为
按物质的量之比为 进行投料,只发生反应①和反应③,平衡时CO和
进行投料,只发生反应①和反应③,平衡时CO和 在含碳产物中的物质的量分数及
在含碳产物中的物质的量分数及 转化率随温度的变化如图所示。
转化率随温度的变化如图所示。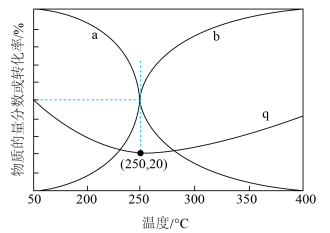

 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
您最近半年使用:0次
9 .  时,将
时,将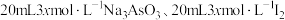 和
和 溶液混合,发生反应:
溶液混合,发生反应: 。溶液中
。溶液中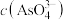 与反应时间(t)的关系如图所示。(忽略混合前后溶液体积的变化)
与反应时间(t)的关系如图所示。(忽略混合前后溶液体积的变化)
2.比较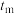 和
和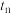 时的化学反应速率,其中
时的化学反应速率,其中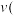 逆)较大的时刻为___________。
逆)较大的时刻为___________。
3.若平衡时溶液的 ,则该反应的平衡常数
,则该反应的平衡常数
___________ 。(用含 和
和 的代数式表示)
的代数式表示)
 时,将
时,将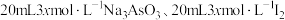 和
和 溶液混合,发生反应:
溶液混合,发生反应: 。溶液中
。溶液中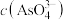 与反应时间(t)的关系如图所示。(忽略混合前后溶液体积的变化)
与反应时间(t)的关系如图所示。(忽略混合前后溶液体积的变化)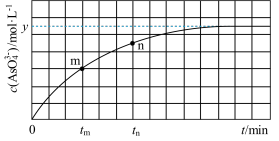
A.溶液的 不再变化 不再变化 | B.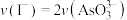 |
C.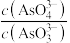 不再变化 不再变化 | D.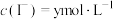 |
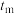 和
和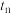 时的化学反应速率,其中
时的化学反应速率,其中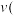 逆)较大的时刻为___________。
逆)较大的时刻为___________。A. | B.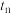 | C.两者相等 | D.无法比较 |
 ,则该反应的平衡常数
,则该反应的平衡常数
 和
和 的代数式表示)
的代数式表示)
您最近半年使用:0次
解题方法
10 . 二氧化碳的开发利用是化学家和化学工作者一直关注的热门话题,试回答:
(1)在 恒容密闭容器中投入
恒容密闭容器中投入 和
和 发生反应
发生反应 ,实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示。
,实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示。___________ 反应,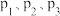 从大到小的关系排序为
从大到小的关系排序为___________ 。
②M点对应的平衡常数
___________ ,在 及
及 时,图中N点
时,图中N点
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)二氧化碳催化加氢合成乙烯是综合利用 的热点研究领域,化学方程式为
的热点研究领域,化学方程式为 。理论计算表明,原料初始组成
。理论计算表明,原料初始组成 ,在体系压强为
,在体系压强为 ,反应达到平衡,四种组分的物质的量分数x随温度T的变化如图所示。回答下列问题:
,反应达到平衡,四种组分的物质的量分数x随温度T的变化如图所示。回答下列问题: 变化的曲线分别是
变化的曲线分别是___________ 。 催化加氢合成
催化加氢合成 反应的
反应的
___________ 0(填“大于”或“小于”)。
②根据图中点 ,计算该温度时反应的平衡常数
,计算该温度时反应的平衡常数
___________  (列出计算式。以分压表示,分压=总压×物质的量分数)。
(列出计算式。以分压表示,分压=总压×物质的量分数)。
(1)在
 恒容密闭容器中投入
恒容密闭容器中投入 和
和 发生反应
发生反应 ,实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示。
,实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示。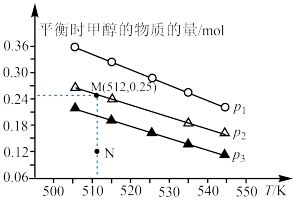
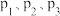 从大到小的关系排序为
从大到小的关系排序为②M点对应的平衡常数

 及
及 时,图中N点
时,图中N点
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)二氧化碳催化加氢合成乙烯是综合利用
 的热点研究领域,化学方程式为
的热点研究领域,化学方程式为 。理论计算表明,原料初始组成
。理论计算表明,原料初始组成 ,在体系压强为
,在体系压强为 ,反应达到平衡,四种组分的物质的量分数x随温度T的变化如图所示。回答下列问题:
,反应达到平衡,四种组分的物质的量分数x随温度T的变化如图所示。回答下列问题: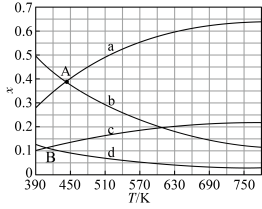
 变化的曲线分别是
变化的曲线分别是 催化加氢合成
催化加氢合成 反应的
反应的
②根据图中点
 ,计算该温度时反应的平衡常数
,计算该温度时反应的平衡常数
 (列出计算式。以分压表示,分压=总压×物质的量分数)。
(列出计算式。以分压表示,分压=总压×物质的量分数)。
您最近半年使用:0次



