解题方法
1 . 在一体积为2 L的密闭容器中充入1 mol N2、2 mol H2,在催化剂作用下发生可逆反应:N2(g)+3H2(g)⇌2NH3(g),NH3的物质的量随时间变化如图所示。回答下列问题:
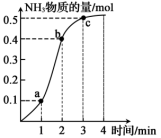
(1)0~1min的反应速率v1与2~3min的反应速率v2相比较,v1_______ (填“>”“=”或“<”)v2,1~2min的反应速率v(H2)=_______ mol·L-1·min-1。
(2)从图象可以看出,前3min内,1~2min反应速率最快,1~2min反应速率变快的原因是_ 。
(3)反应最大限度是在_______ min时,此时密闭容器中总物质的量为_______ mol。
(4)研究发现降低温度有利于平衡向生成NH3的方向移动,而工业实际采用在较高温度下进行反应的原因是_______ 。
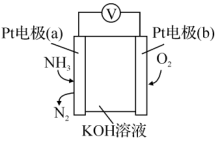
(5)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图。则电池负极为_______ (填“a”或“b”)。

(1)0~1min的反应速率v1与2~3min的反应速率v2相比较,v1
(2)从图象可以看出,前3min内,1~2min反应速率最快,1~2min反应速率变快的原因是
(3)反应最大限度是在
(4)研究发现降低温度有利于平衡向生成NH3的方向移动,而工业实际采用在较高温度下进行反应的原因是
(5)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图。则电池负极为

您最近半年使用:0次
解题方法
2 . 依据如下有关铝的三个装置图,回答问题。
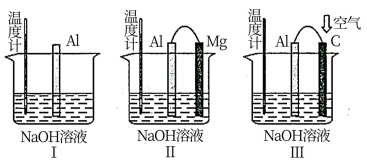
(1)三个装置同时开始反应,单位时间内温度计示数最高的是___________ (填“图Ⅰ”“图Ⅱ”或“图Ⅲ”)。
(2)写出图Ⅱ装置Al电极的电极反应式:___________ ;写出图Ⅲ装置正极的电极反应式:___________ ;写出图Ⅲ装置的总反应化学方程式:___________ 。
(3)图Ⅰ装置中为使生成氢气的速率加快,下列方法可行的是___________ (填序号)。
①适当升高温度②把铝棒加粗
③将NaOH溶液换成浓硫酸④用铝碳合金代替铝棒
(4)某同学欲收集 和碘蒸气,在某绝热且体积固定的密闭容器中发生反应:
和碘蒸气,在某绝热且体积固定的密闭容器中发生反应: ,下列叙述能证明该反应达到化学平衡状态的是
,下列叙述能证明该反应达到化学平衡状态的是___________ (填序号)。
A.容器内温度不变
B.混合气体密度不变
C.混合气体平均相对分子质量不变
D.HI的体积分数不变
E.1mol 键断裂的同时有2mol
键断裂的同时有2mol 键生成现向容积为1L密闭容器中充入0.10mol
键生成现向容积为1L密闭容器中充入0.10mol 和0.15mol
和0.15mol ,在不同温度下测定同一时刻
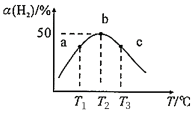
,在不同温度下测定同一时刻 的转化率,结果如图。当温度为
的转化率,结果如图。当温度为 ℃时,从反应开始经过2min达到b点,用
℃时,从反应开始经过2min达到b点,用 表示这段时间的反应速率为
表示这段时间的反应速率为___________ ,此时 的转化率为
的转化率为___________ (保留2位有效数字)。

(1)三个装置同时开始反应,单位时间内温度计示数最高的是
(2)写出图Ⅱ装置Al电极的电极反应式:
(3)图Ⅰ装置中为使生成氢气的速率加快,下列方法可行的是
①适当升高温度②把铝棒加粗
③将NaOH溶液换成浓硫酸④用铝碳合金代替铝棒
(4)某同学欲收集
 和碘蒸气,在某绝热且体积固定的密闭容器中发生反应:
和碘蒸气,在某绝热且体积固定的密闭容器中发生反应: ,下列叙述能证明该反应达到化学平衡状态的是
,下列叙述能证明该反应达到化学平衡状态的是
A.容器内温度不变
B.混合气体密度不变
C.混合气体平均相对分子质量不变
D.HI的体积分数不变
E.1mol
 键断裂的同时有2mol
键断裂的同时有2mol 键生成现向容积为1L密闭容器中充入0.10mol
键生成现向容积为1L密闭容器中充入0.10mol 和0.15mol
和0.15mol ,在不同温度下测定同一时刻
,在不同温度下测定同一时刻 的转化率,结果如图。当温度为
的转化率,结果如图。当温度为 ℃时,从反应开始经过2min达到b点,用
℃时,从反应开始经过2min达到b点,用 表示这段时间的反应速率为
表示这段时间的反应速率为 的转化率为
的转化率为
您最近半年使用:0次



