依据如下有关铝的三个装置图,回答问题。
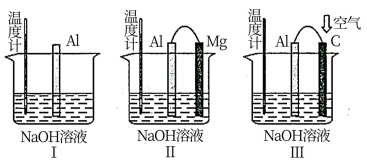
(1)三个装置同时开始反应,单位时间内温度计示数最高的是___________ (填“图Ⅰ”“图Ⅱ”或“图Ⅲ”)。
(2)写出图Ⅱ装置Al电极的电极反应式:___________ ;写出图Ⅲ装置正极的电极反应式:___________ ;写出图Ⅲ装置的总反应化学方程式:___________ 。
(3)图Ⅰ装置中为使生成氢气的速率加快,下列方法可行的是___________ (填序号)。
①适当升高温度②把铝棒加粗
③将NaOH溶液换成浓硫酸④用铝碳合金代替铝棒
(4)某同学欲收集 和碘蒸气,在某绝热且体积固定的密闭容器中发生反应:
和碘蒸气,在某绝热且体积固定的密闭容器中发生反应: ,下列叙述能证明该反应达到化学平衡状态的是
,下列叙述能证明该反应达到化学平衡状态的是___________ (填序号)。
A.容器内温度不变
B.混合气体密度不变
C.混合气体平均相对分子质量不变
D.HI的体积分数不变
E.1mol 键断裂的同时有2mol
键断裂的同时有2mol 键生成现向容积为1L密闭容器中充入0.10mol
键生成现向容积为1L密闭容器中充入0.10mol 和0.15mol
和0.15mol ,在不同温度下测定同一时刻
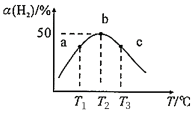
,在不同温度下测定同一时刻 的转化率,结果如图。当温度为
的转化率,结果如图。当温度为 ℃时,从反应开始经过2min达到b点,用
℃时,从反应开始经过2min达到b点,用 表示这段时间的反应速率为
表示这段时间的反应速率为___________ ,此时 的转化率为
的转化率为___________ (保留2位有效数字)。

(1)三个装置同时开始反应,单位时间内温度计示数最高的是
(2)写出图Ⅱ装置Al电极的电极反应式:
(3)图Ⅰ装置中为使生成氢气的速率加快,下列方法可行的是
①适当升高温度②把铝棒加粗
③将NaOH溶液换成浓硫酸④用铝碳合金代替铝棒
(4)某同学欲收集
 和碘蒸气,在某绝热且体积固定的密闭容器中发生反应:
和碘蒸气,在某绝热且体积固定的密闭容器中发生反应: ,下列叙述能证明该反应达到化学平衡状态的是
,下列叙述能证明该反应达到化学平衡状态的是
A.容器内温度不变
B.混合气体密度不变
C.混合气体平均相对分子质量不变
D.HI的体积分数不变
E.1mol
 键断裂的同时有2mol
键断裂的同时有2mol 键生成现向容积为1L密闭容器中充入0.10mol
键生成现向容积为1L密闭容器中充入0.10mol 和0.15mol
和0.15mol ,在不同温度下测定同一时刻
,在不同温度下测定同一时刻 的转化率,结果如图。当温度为
的转化率,结果如图。当温度为 ℃时,从反应开始经过2min达到b点,用
℃时,从反应开始经过2min达到b点,用 表示这段时间的反应速率为
表示这段时间的反应速率为 的转化率为
的转化率为
更新时间:2021-07-13 21:31:30
|
相似题推荐
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐1】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】
【实验内容及记录】
回答下列问题:
(1)根据上表中的实验数据,可以得到的结论是___________ 。
(2)利用实验3中数据计算,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
___________  。
。
(3)实验2中a的数值为___________ ,实验中加入 的目的是
的目的是___________ 。
(4)该小组同学根据经验绘制了 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中
随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中 随时间变化的趋势应如图2所示。
随时间变化的趋势应如图2所示。

该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①该小组同学提出的假设:生成的 对该反应有催化作用。
对该反应有催化作用。
②请你帮助该小组同学完成实验方案,并填写表中空白。
③现象及结论:依据现象___________ ,得出该小组同学提出的假设成立。
【实验原理】

【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
0.6mol/L 溶液 溶液 |  | 0.04mol/L 溶液 溶液 | 3mol/L稀硫酸 | ||
| 1 | 1.0 | 4.0 | 3.0 | 2.0 | 6.4 |
| 2 | 2.0 | a | 3.0 | 2.0 | 5.2 |
| 3 | 3.0 | 2.0 | 3.0 | 2.0 | 2.0 |
(1)根据上表中的实验数据,可以得到的结论是
(2)利用实验3中数据计算,用
 的浓度变化表示的反应速率
的浓度变化表示的反应速率
 。
。(3)实验2中a的数值为
 的目的是
的目的是(4)该小组同学根据经验绘制了
 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中
随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中 随时间变化的趋势应如图2所示。
随时间变化的趋势应如图2所示。
该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①该小组同学提出的假设:生成的
 对该反应有催化作用。
对该反应有催化作用。②请你帮助该小组同学完成实验方案,并填写表中空白。
| 实验编号 | 室温下,试管中所加试剂及其用量/ | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
0.6mol/L 溶液 溶液 |  | 0.04mol/L 溶液 溶液 | 3mol/L稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | t | |
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】某同学做浓度对化学反应速率的影响的实验时,将3支试管分别编号为①②③,并按下表中的量进行实验,记录下的时间数据是16 s、28 s、33 s。请将3个数据填入下面的适当位置,并写出实验结论。
(1)将对应①、②、③的时间分别写出:a________ , b________ , c________ 。
(2)实验结论:________________________________________ 。
| 试管编号 | 加3% Na2S2O3 | 加H2O | 加H2SO4 (1∶5) | 出现浑浊 时间 |
| ① | 3 mL | 3 mL | 5滴 | a |
| ② | 4 mL | 2 mL | 5滴 | b |
| ③ | 5 mL | 1 mL | 5滴 | c |
(2)实验结论:
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐3】实验室中通常用MnO2作催化剂分解H2O2,已知CuSO4溶液对H2O2的分解也具有催化作用,某实验兴趣小组同学猜想其他盐溶液也可能在这个反应中起同样的作用,于是他们做了以下探究。请你帮助他们完成实验报告:
(1)实验过程:在一支试管中加入5 mL 5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管。
实验现象:_______ 。
实验结论:FeCl3溶液可以催化分解H2O2。
(2)已知FeCl3在水中可解离出Fe3+和Cl-,同学们提出以下猜想:
甲同学的猜想:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Cl-。
你认为最不可能的是_______ 同学的猜想,理由是_______ 。
(3)同学们对余下的两个猜想,用实验进行了探究,请你仔细分析后填表:
(1)实验过程:在一支试管中加入5 mL 5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管。
实验现象:
实验结论:FeCl3溶液可以催化分解H2O2。
(2)已知FeCl3在水中可解离出Fe3+和Cl-,同学们提出以下猜想:
甲同学的猜想:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Cl-。
你认为最不可能的是
(3)同学们对余下的两个猜想,用实验进行了探究,请你仔细分析后填表:
| 实验过程 | 实验现象 | 结论 |
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
解题方法
【推荐1】填空
(1)断开气态物质中1mol某种共价键生成气态原子需要吸收的能量称为键能(kJ·mol−1)。如表所示是一些共价键的键能。
根据上表的数据,在合成1mol氨_____ (“放出”或“吸收”)的热量为_____ kJ。
(2)在2L容器中投入2molSO2和bmolO2,下图是部分反应物与生成物随时间的变化曲线。
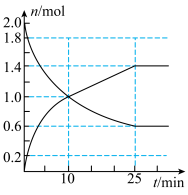
①10min时v(正)_____ v(逆)(填“大于”或“小于”或“等于”);0~10min内,v(SO3)=_____ 。
②平衡时,SO2的转化率为_____ 。
③下列条件能够加快反应速率的是_____ 。
A.升高温度
B.保持压强不变,充入He使容积增大
C.保持体积不变,充入He使压强增大
D.充入一定量的氧气
④下列情况能说明该反应达到化学平衡的是_____ 。
A.v(SO3)=v(SO2)
B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变
D.混合气体的总物质的量不再改变
E.SO2、O2、SO3的物质的量之比达到2∶1∶2
(1)断开气态物质中1mol某种共价键生成气态原子需要吸收的能量称为键能(kJ·mol−1)。如表所示是一些共价键的键能。
| 共价键 | H-H | N≡N | N-H |
| 键能(kJ·mol-1) | 436 | 946 | 391 |
(2)在2L容器中投入2molSO2和bmolO2,下图是部分反应物与生成物随时间的变化曲线。

①10min时v(正)
②平衡时,SO2的转化率为
③下列条件能够加快反应速率的是
A.升高温度
B.保持压强不变,充入He使容积增大
C.保持体积不变,充入He使压强增大
D.充入一定量的氧气
④下列情况能说明该反应达到化学平衡的是
A.v(SO3)=v(SO2)
B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变
D.混合气体的总物质的量不再改变
E.SO2、O2、SO3的物质的量之比达到2∶1∶2
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐2】乙酸乙酯是一种非常重要的有机化工原料,用途十分广泛.根据所学内容填空。
I.由乙烯合成乙酸乙酯的流程如下;
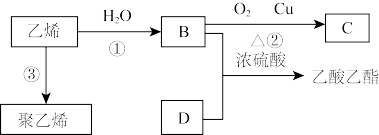
(1)写出B与D反应的化学方程式________ ;反应类型:_________ ;
(2)写出反应③的化学方程式:_________ 。
II.实验室用如图所示装置制备乙酸乙酯.
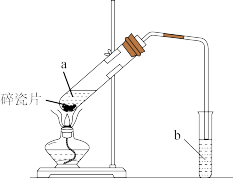
(1)实验前,向试管a中加入3mL______ ,然后边振荡试管边慢慢加入2mL______ 和2mL乙酸。
(2)试管b中盛放的试剂是饱和_____ 溶液。试管b中的导管不能伸入液面下的原因是____ 。
(3)反应结束后,从试管b中分离出乙酸乙酯的方法是______ 。
(4)下列描述不能说明乙醇与乙酸的反应已达到化学平衡状态的有_____ (填序号)。
a.单位时间里,生成lmol乙酸乙酯,同时生成lmol水
b.单位时间区,生成lmol乙酸乙酯,同时生成1mol乙酸
c.单位时间里,消耗lmol乙醇,同时消耗1mol乙酸
d.正反应的速率与逆反应的速率相等
e.混合物中各物质的浓度不再变化
I.由乙烯合成乙酸乙酯的流程如下;

(1)写出B与D反应的化学方程式
(2)写出反应③的化学方程式:
II.实验室用如图所示装置制备乙酸乙酯.

(1)实验前,向试管a中加入3mL
(2)试管b中盛放的试剂是饱和
(3)反应结束后,从试管b中分离出乙酸乙酯的方法是
(4)下列描述不能说明乙醇与乙酸的反应已达到化学平衡状态的有
a.单位时间里,生成lmol乙酸乙酯,同时生成lmol水
b.单位时间区,生成lmol乙酸乙酯,同时生成1mol乙酸
c.单位时间里,消耗lmol乙醇,同时消耗1mol乙酸
d.正反应的速率与逆反应的速率相等
e.混合物中各物质的浓度不再变化
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
解题方法
【推荐3】 Ⅰ. 已知某反应:A(g)+ 3B(g)  C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
(1)t1 h时,c(D) ___________ mol/L。
(2)0-t2 h内,以A的浓度变化表示反应的平均速率:v(A)___________ mol·L-1·h-1。
(3)下列能说明该反应达到平衡状态的是___________(填标号)。
Ⅱ.
(4)合成氨反应中,温度越低,氨的产率越高,但在生产中选定的反应温度为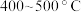 ,原因是
,原因是_________________________ 。
(5)合成氨反应可能的微观历程如图所示:
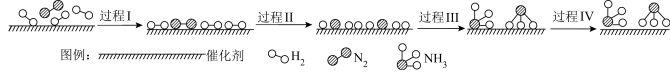
吸附在催化剂表面的物质用*标注。已知过程Ⅱ可以表示为 ,则过程Ⅲ可以表示为
,则过程Ⅲ可以表示为___________ 。
 C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。浓度/( ) ) | c(A) | c(B) | c(D) |
| 0 | 1.0 | 3.0 | 0 |
 h h | 0.8 | ||
 h h | 2.1 |
(2)0-t2 h内,以A的浓度变化表示反应的平均速率:v(A)
(3)下列能说明该反应达到平衡状态的是___________(填标号)。
| A.容器中的压强不随时间变化 | B.气体密度不再变化 |
| C.B和D的浓度之比为3:4 | D.消耗0.3 mol B的同时生成0.4 mol D |
Ⅱ.
(4)合成氨反应中,温度越低,氨的产率越高,但在生产中选定的反应温度为
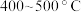 ,原因是
,原因是(5)合成氨反应可能的微观历程如图所示:

吸附在催化剂表面的物质用*标注。已知过程Ⅱ可以表示为
 ,则过程Ⅲ可以表示为
,则过程Ⅲ可以表示为
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
名校
解题方法
【推荐1】硫、氮的氧化物治理是当前化学研究的热点。回答下列问题:
(1)烟气脱硫过程涉及的反应如下:
Ca(ClO)2 (aq)+ H2SO4 (aq) CaSO4(s) +2HClO(aq) △H =a kJ·mol-1;
CaSO4(s) +2HClO(aq) △H =a kJ·mol-1;
SO2(g)+ H2O(l) + HClO(aq) H2SO4(aq) + HCl(aq) △H =b kJ·mol-1。
H2SO4(aq) + HCl(aq) △H =b kJ·mol-1。
则脱硫反应:Ca(ClO)2(aq) + 2SO2(g) + 2H2O(l) CaSO4 (s)+ H2SO4(aq) +2HCl(aq)的△H=
CaSO4 (s)+ H2SO4(aq) +2HCl(aq)的△H=_______ (用含 a、b的代数式表示)kJ·mol-1。
(2)一定温度下,向一个2 L的恒容密闭容器中充入0.4 mol NO2 ,发生反应:2NO2(g) N2O4(g) △H<0,测得不同时间时容器中NO2的浓度如下表所示。
N2O4(g) △H<0,测得不同时间时容器中NO2的浓度如下表所示。
①在0~3 min时间段内,N2O4的平均反应速率为_______ ,NO2的平衡转化率为_______ 。
②该温度下,反应的平衡常数K=_______ L·mol-1。
(1)烟气脱硫过程涉及的反应如下:
Ca(ClO)2 (aq)+ H2SO4 (aq)
 CaSO4(s) +2HClO(aq) △H =a kJ·mol-1;
CaSO4(s) +2HClO(aq) △H =a kJ·mol-1;SO2(g)+ H2O(l) + HClO(aq)
 H2SO4(aq) + HCl(aq) △H =b kJ·mol-1。
H2SO4(aq) + HCl(aq) △H =b kJ·mol-1。则脱硫反应:Ca(ClO)2(aq) + 2SO2(g) + 2H2O(l)
 CaSO4 (s)+ H2SO4(aq) +2HCl(aq)的△H=
CaSO4 (s)+ H2SO4(aq) +2HCl(aq)的△H=(2)一定温度下,向一个2 L的恒容密闭容器中充入0.4 mol NO2 ,发生反应:2NO2(g)
 N2O4(g) △H<0,测得不同时间时容器中NO2的浓度如下表所示。
N2O4(g) △H<0,测得不同时间时容器中NO2的浓度如下表所示。| 时间/min | 0 | 1 | 2 | 3 | 4 |
| c(NO2)/(mol·L-1) | 0.2 | 0.15 | 0.12 | 0.11 | 0.11 |
②该温度下,反应的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
解题方法
【推荐2】回答下列问题。
(1)一定条件下,在 密闭容器中充入
密闭容器中充入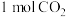 和
和 ,发生反应:
,发生反应: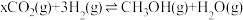 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
___________ ; 内
内 的平均反应速率
的平均反应速率
___________ 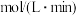 ,平衡时
,平衡时 的转化率为
的转化率为___________ 。
(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
(3)工业上常以水煤气( 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: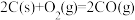
 ;
;
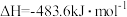 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为___________ 。
(1)一定条件下,在
 密闭容器中充入
密闭容器中充入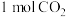 和
和 ,发生反应:
,发生反应: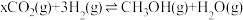 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。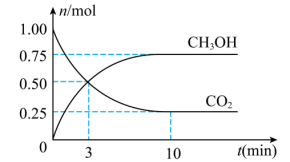

 内
内 的平均反应速率
的平均反应速率
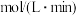 ,平衡时
,平衡时 的转化率为
的转化率为(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
| A.降低温度 | B.增加 的量 的量 | C.使用催化剂 | D.及时分离出甲醇 |
 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: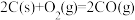
 ;
;
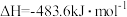 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为
您最近一年使用:0次
【推荐3】二氧化碳是用途非常广泛的化工基础原料,回答下列问题:
(1)工业上可以用CO2来生产燃料甲醇。
已知:CO2(g) +3H2(g) ⇌ CH3OH(l) +H2O(l) H= -130kJmol-1
2H2(g)+O2(g)=2H2O(l) H=-572kJmol-1
CH3OH(1)的燃烧热H=________ kJmol-1。
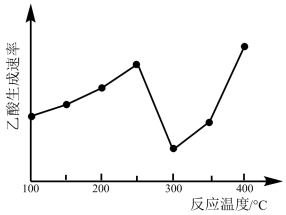
(2)在催化剂作用下,CO2和CH4可直接转化为乙酸:CO2(g)+CH4(g)=CH3COOH(g) H>0,在不同温度下乙酸的生成速率变化如图所示。
①当温度在250°C-300°C范围时,乙酸的生成速率减慢的主要原因是___________ 。
②欲使乙酸的平衡产率提高,应采取的措施是__________ (任写一条措施即可)。
(3)一定条件下,在密闭容器中发生反应,2CO(g) ⇌C(s)+CO2(g).
①下列能说明该反应达到平衡的是______________ 。
A 容器内混合物的质量不变
B CO和CO2的物质的量之比不再变化
C 混合气体的平均摩尔质量不再变化
D 生成amolCO2的同时消耗2amol.CO
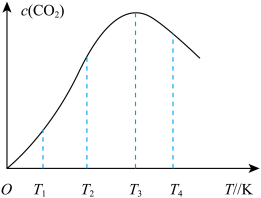
②向某恒容容器中通入一定量的CO发生上述反应,在不同温度下CO2的物质的量浓度c (CO2)随温度的变化如上图所示,则该反应为________ (填“放热”或“吸热”)反应。
③向容积可变的某恒压容器中通入amolCO,T°C时反应经过10min达平衡,CO的体积分数为75%。CO的平衡转化率为________ 。在容积改变的条件下,反应速率可用单位时间内反应物成生成物的物质的量变化来表示,则0-10min内平均反应速率v(CO2)=________ 。
(1)工业上可以用CO2来生产燃料甲醇。
已知:CO2(g) +3H2(g) ⇌ CH3OH(l) +H2O(l) H= -130kJmol-1
2H2(g)+O2(g)=2H2O(l) H=-572kJmol-1
CH3OH(1)的燃烧热H=
(2)在催化剂作用下,CO2和CH4可直接转化为乙酸:CO2(g)+CH4(g)=CH3COOH(g) H>0,在不同温度下乙酸的生成速率变化如图所示。

①当温度在250°C-300°C范围时,乙酸的生成速率减慢的主要原因是
②欲使乙酸的平衡产率提高,应采取的措施是
(3)一定条件下,在密闭容器中发生反应,2CO(g) ⇌C(s)+CO2(g).
①下列能说明该反应达到平衡的是
A 容器内混合物的质量不变
B CO和CO2的物质的量之比不再变化
C 混合气体的平均摩尔质量不再变化
D 生成amolCO2的同时消耗2amol.CO

②向某恒容容器中通入一定量的CO发生上述反应,在不同温度下CO2的物质的量浓度c (CO2)随温度的变化如上图所示,则该反应为
③向容积可变的某恒压容器中通入amolCO,T°C时反应经过10min达平衡,CO的体积分数为75%。CO的平衡转化率为
您最近一年使用:0次
【推荐1】化学反应速率、限度及能量与生产、生活密切相关。
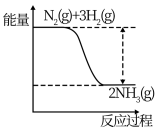
(1)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2+3H2 2NH3。合成氨反应中的能量变化如图所示,该反应中,反应物化学键断裂吸收的总能量
2NH3。合成氨反应中的能量变化如图所示,该反应中,反应物化学键断裂吸收的总能量___ (填“大于”或“小于”)生成物化学键形成放出的总能量。
(2)小王同学为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①求2~4分钟时间段以盐酸的浓度变化来表示的该反应速率___ 。(设溶液体积不变)
②小蒋同学认为在盐酸溶液中滴入少量的CuSO4溶液可以加快反应的速率,请从电化学的角度给子分析:构成的原电池中负极反应式为___ ;溶液中H+移向___ 极(填“正“或“负")。
(3)某温度下在4L恒容密闭容器中,3种气态物质X、Y、Z的物质的量随时间变化曲线如图。
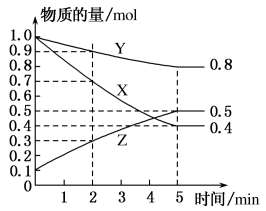
①写出该反应的化学方程式___ 。
②在5min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是___ 。
A.X、Y、Z的浓度相等
B.容器内气体压强保持不变
C.X、Y的反应速率比为3:1
D.生成1molY的同时生成2molZ
③该反应达平衡时,X的转化率为___ 。
(1)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2+3H2
 2NH3。合成氨反应中的能量变化如图所示,该反应中,反应物化学键断裂吸收的总能量
2NH3。合成氨反应中的能量变化如图所示,该反应中,反应物化学键断裂吸收的总能量
(2)小王同学为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 50 | 190 | 414 | 526 | 570 |
①求2~4分钟时间段以盐酸的浓度变化来表示的该反应速率
②小蒋同学认为在盐酸溶液中滴入少量的CuSO4溶液可以加快反应的速率,请从电化学的角度给子分析:构成的原电池中负极反应式为
(3)某温度下在4L恒容密闭容器中,3种气态物质X、Y、Z的物质的量随时间变化曲线如图。

①写出该反应的化学方程式
②在5min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是
A.X、Y、Z的浓度相等
B.容器内气体压强保持不变
C.X、Y的反应速率比为3:1
D.生成1molY的同时生成2molZ
③该反应达平衡时,X的转化率为
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
名校
解题方法
【推荐2】电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人类的一项重要贡献。
(1)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是___________ (填字母)。
A.锌锰电池工作一段时间后碳棒会变细
B.氢氧燃料电池可将化学能直接转变为电能
C.铅蓄电池负极是 ,正极是Pb
,正极是Pb
(2)氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都可表示为: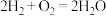 。
。
①酸式氢氧燃料电池的电解质是酸,其正极的电极反应式为___________ 。
②工作一段时间后,电解质溶液的pH将___________ (填“变大”、“变小”或“不变”)。
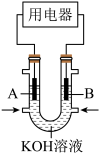
(3)将 设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为:
设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为: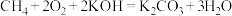 。
。___________ (填“A”或“B”)电极入口通甲烷,其电极反应式为___________ 。
(4)某同学欲把反应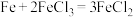 设计成原电池,请写出负极的电极反应式:
设计成原电池,请写出负极的电极反应式:___________ 。
(1)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是
A.锌锰电池工作一段时间后碳棒会变细
B.氢氧燃料电池可将化学能直接转变为电能
C.铅蓄电池负极是
 ,正极是Pb
,正极是Pb(2)氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都可表示为:
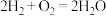 。
。①酸式氢氧燃料电池的电解质是酸,其正极的电极反应式为
②工作一段时间后,电解质溶液的pH将
(3)将
 设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为:
设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒),电池总反应为: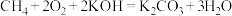 。
。
(4)某同学欲把反应
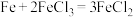 设计成原电池,请写出负极的电极反应式:
设计成原电池,请写出负极的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
名校
解题方法
【推荐3】原电池是将化学能转化为电能的装置。
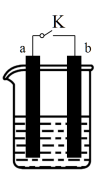
I.a为铜片,b为铁片,烧杯中是稀硫酸溶液,当开关K断开时产生的现象为___________ ;当开关K闭合时,产生的现象为___________ 。
A.a不断溶解 B.b不断溶解 C.a上产生气泡 D.b上产生气泡 E.溶液逐渐变蓝
(2)闭合开关K,反应一段时间后断开开关K,经过一段时间后,下列叙述不正确的是___________ 。
A.溶液中 浓度减小 B.正极附近
浓度减小 B.正极附近 浓度逐渐增大
浓度逐渐增大
C.溶液中含有 D.溶液中
D.溶液中 浓度基本不变
浓度基本不变
Ⅱ.某同学为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折算为标准状况下的体积),实验记录如下(累计值):
(3)反应速率最大的时间段是___________ (填“0~1min”“1~2min”“2~3min”“3~4min”或“4~5min”);反应速率最小的时间段是___________ (填“0~1min”“1~2min”“2~3min”“ 3~4min”或“4~5min”),
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在盐酸中分别加入等体积的下列液体,你认为可行的是___________ (填序号)。
A.蒸馏水 B.NaCl溶液 C. 溶液 D.
溶液 D. 溶液
溶液

I.a为铜片,b为铁片,烧杯中是稀硫酸溶液,当开关K断开时产生的现象为
A.a不断溶解 B.b不断溶解 C.a上产生气泡 D.b上产生气泡 E.溶液逐渐变蓝
(2)闭合开关K,反应一段时间后断开开关K,经过一段时间后,下列叙述不正确的是
A.溶液中
 浓度减小 B.正极附近
浓度减小 B.正极附近 浓度逐渐增大
浓度逐渐增大C.溶液中含有
 D.溶液中
D.溶液中 浓度基本不变
浓度基本不变Ⅱ.某同学为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折算为标准状况下的体积),实验记录如下(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在盐酸中分别加入等体积的下列液体,你认为可行的是
A.蒸馏水 B.NaCl溶液 C.
 溶液 D.
溶液 D. 溶液
溶液
您最近一年使用:0次



