名校
解题方法
1 . 草酸亚铁晶体(FeC2O4•2H2O)常用作生产锂电池、涂料、着色剂以及感光材料的原材料,难溶于水,受热易分解。
I.制备草酸亚铁晶体:
①称取硫酸亚铁铵晶体5g,放入250mL三颈烧瓶中,加入10滴左右1.0mol•L-1H2SO4溶液和15mL蒸馏水加热溶解;
②加入25mL饱和草酸溶液,加热搅拌至沸腾停止加热,静置;
③待黄色晶体FeC2O4•2H2O沉淀后倾析,洗涤,加入约20mL蒸馏水搅拌并温热5min,静置,弃去上层清液,即得黄色草酸亚铁晶体。

(1)B的名称是____ ;B的出水口是____ (填“上口”或“下口”)。
(2)硫酸亚铁铵晶体中可能混有Fe3+,检验其是否含有Fe3+的试剂是____ 溶液,若混有Fe3+,观察到的现象是____ 。
II.将一定质量的草酸亚铁晶体(FeC2O4•2H2O)在氩气气氛中进行热重分析示意图(TG%表示残留固体质量占原样品总质量的百分数)。

(3)B处时残留物的化学式为____ 。
(4)取上述分解得到的600℃时的固体放在空气中继续加热时其质量增加,发生反应的化学方程式为____ 。
I.制备草酸亚铁晶体:
①称取硫酸亚铁铵晶体5g,放入250mL三颈烧瓶中,加入10滴左右1.0mol•L-1H2SO4溶液和15mL蒸馏水加热溶解;
②加入25mL饱和草酸溶液,加热搅拌至沸腾停止加热,静置;
③待黄色晶体FeC2O4•2H2O沉淀后倾析,洗涤,加入约20mL蒸馏水搅拌并温热5min,静置,弃去上层清液,即得黄色草酸亚铁晶体。

(1)B的名称是
(2)硫酸亚铁铵晶体中可能混有Fe3+,检验其是否含有Fe3+的试剂是
II.将一定质量的草酸亚铁晶体(FeC2O4•2H2O)在氩气气氛中进行热重分析示意图(TG%表示残留固体质量占原样品总质量的百分数)。

(3)B处时残留物的化学式为
(4)取上述分解得到的600℃时的固体放在空气中继续加热时其质量增加,发生反应的化学方程式为
您最近一年使用:0次
2022-10-29更新
|
177次组卷
|
4卷引用:吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题
2 . 铟(In)是一种主要用于液晶显示屏和半导体生产的重要稀有金属。从铅、锌的冶炼过程中产生的高铟烟灰(主要含ZnO、PbO、Fe2O3、In2O3、In2S3)中提取铟的流程如图:

已知:滤液中铟以In3+的形式存在,In3+与Al3+相似,易水解。
回答下列问题:
(1)“氧化酸浸”需要加热,其目的是____ 。
(2)“氧化酸浸”时不能用浓盐酸代替硫酸,理由是____ (用化学方程式表示)。
(3)“氧化酸浸”过程中In2S3的硫元素被氧化为SO ,滤渣除含过量MnO2外,还有
,滤渣除含过量MnO2外,还有____ (填化学式)。
(4)“萃取”过程中的萃取剂可用H2A2表示,使In3+进入有机相,萃取过程In3+发生的反应方程式为:In3++3H2A2 In(HA2)3+3H+,平衡常数为K。“萃取”时萃取率的高低受溶液的pH影响很大,已知与萃取率(E%)的关系符合如下公式:lg
In(HA2)3+3H+,平衡常数为K。“萃取”时萃取率的高低受溶液的pH影响很大,已知与萃取率(E%)的关系符合如下公式:lg =lgK-lg
=lgK-lg 。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=____ (已知lg19=1.28忽略萃取剂浓度的变化,结果保留三位有效数字)。
(5)盐酸的浓度与铟、铁的反萃取率的关系如图所示。则“反萃取”过程中应选择盐酸的最佳浓度为____ mol•L-1。

(6)“置换”后所得浊液,需要经过过滤、洗涤、干燥等操作得到粗铟,在洗涤操作中,检验粗铟已洗涤干净的方法为____ 。

已知:滤液中铟以In3+的形式存在,In3+与Al3+相似,易水解。
回答下列问题:
(1)“氧化酸浸”需要加热,其目的是
(2)“氧化酸浸”时不能用浓盐酸代替硫酸,理由是
(3)“氧化酸浸”过程中In2S3的硫元素被氧化为SO
 ,滤渣除含过量MnO2外,还有
,滤渣除含过量MnO2外,还有(4)“萃取”过程中的萃取剂可用H2A2表示,使In3+进入有机相,萃取过程In3+发生的反应方程式为:In3++3H2A2
 In(HA2)3+3H+,平衡常数为K。“萃取”时萃取率的高低受溶液的pH影响很大,已知与萃取率(E%)的关系符合如下公式:lg
In(HA2)3+3H+,平衡常数为K。“萃取”时萃取率的高低受溶液的pH影响很大,已知与萃取率(E%)的关系符合如下公式:lg =lgK-lg
=lgK-lg 。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=(5)盐酸的浓度与铟、铁的反萃取率的关系如图所示。则“反萃取”过程中应选择盐酸的最佳浓度为

(6)“置换”后所得浊液,需要经过过滤、洗涤、干燥等操作得到粗铟,在洗涤操作中,检验粗铟已洗涤干净的方法为
您最近一年使用:0次
2022-10-29更新
|
608次组卷
|
3卷引用:吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题
名校
3 . 钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,如图为钠投入液氨中的溶剂化图。钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是
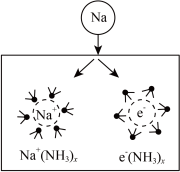

| A.钠的密度比液氨大 |
| B.溶液的导电性增强 |
| C.钠和液氨可发生以下反应:2NH3+2Na=2NaNH2+H2↑ |
| D.0.1mol钠投入液氨生成0.01molH2时,Na共失去0.02mol电子 |
您最近一年使用:0次
2021-05-07更新
|
1591次组卷
|
15卷引用:吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题
吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题山东省临沂市部分县区2020-2021学年高一下学期期中考试化学试题广东省广州市广州大学附属中学2020-2021学年高一下学期4月月考试题(已下线)课时14 钠及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)重庆市第一中学校 2021-2022学年高二上学期入学摸底考试化学试题黑龙江省实验中学2021-2022高三上学期第三次月考(开学考)化学试题天津市耀华中学2021-2022学年高三上学期第一次月考化学试题浙江省湖州市三贤联盟2021-2022学年高一上学期期中考试化学试题吉林省吉林市普通中学2022-2023学年高三第一次调研测试化学试题吉林省吉林市普通中学2022-2023学年高三上学期10月调研化学试题天津市耀华中学2022-2023学年高一上学期期中考试化学试题河南省许昌市禹州市高级中学2023-2024学年高三上学期9月月考化学试题福建省莆田第一中学2023-2024学年高一上学期期末考试化学试题
11-12高二下·内蒙古·期末
名校
解题方法
4 . Na2O2、HCl、Al2O3三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl-、OH-,且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为
| A.2:4:1 | B.3:2:1 | C.2:3:1 | D.4:2:1 |
您最近一年使用:0次
2020-08-20更新
|
220次组卷
|
20卷引用:2013届吉林省延边二中高三第一次阶段测试化学试卷
(已下线)2013届吉林省延边二中高三第一次阶段测试化学试卷 (已下线)2011-2012学年内蒙古巴市一中高二下学期期末考试化学试卷2014届河北省衡水中学高三上学期二调考试化学试卷2015届山东省曲阜市高三上学期期中考试化学试卷2015届甘肃省白银市第一中学高三上学期期中考试化学试卷2015届山东省曲阜师大附中高三上学期期中化学试卷2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷2015-2016学年河北省唐山一中高二下期末化学试卷2015-2016学年辽宁沈阳市第二中学高二下期末考化学卷2017届黑龙江省双鸭山一中高三上学期第一次质检化学试卷2017届山东省桓台第二中学高三上学期第一次月考化学试卷2017届河北省石家庄市辛集中学高三上第一次阶段考试化学卷四川省成都七中实验学校2016-2017学年高二下学期期中考试化学试题江西省赣州市第四中学2017届高三上学期第二次月考化学试题黑龙江省哈尔滨师范大学青冈实验中学校2019届高三上学期9月月考化学试题【市级联考】辽宁省凤城市2018-2019学年高二下学期5月联考化学试题山西省实验中学2020届高三化学复习针对性试题集(七)黑龙江省哈尔滨师范大学青冈实验中学校2019届高三10月月考化学试题河北省衡水中学2021届高三上学期二调考试化学试题四川省眉山市仁寿第二中学等四校2020-2021学年高一上学期12月月考化学试题
名校
5 . 下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语 回答下列问题:
(1)⑧元素氢化物的电子式是_____________ 。
(2)②、③、⑤元素的原子半径由大到小的顺序为____________________ 。
(3)②、④、⑦元素的气态氢化物稳定性由强到弱的顺序是_________________________ 。
(4)有两种化合物A和B都由①④⑤⑧四种元素组成。若A与B在水溶液中能发生离子反应,则该反应的离子方程式为_____________________________________________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)⑧元素氢化物的电子式是
(2)②、③、⑤元素的原子半径由大到小的顺序为
(3)②、④、⑦元素的气态氢化物稳定性由强到弱的顺序是
(4)有两种化合物A和B都由①④⑤⑧四种元素组成。若A与B在水溶液中能发生离子反应,则该反应的离子方程式为
您最近一年使用:0次
解题方法
6 . 海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是____________________ (填物理变化、化学变化);
(2)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的化学方程式为___________________________________________ ;
(3)实验室用MnO2和浓盐酸为原料制备氯气,该反应的化学方程式为_____________ ,尾气处理的化学方程式为_______________________________________ 。工业上制备漂白粉的化学方程式________________________________________ 。
(4)将实验室制的氯气配成新制的氯水含有多种微粒,试用化学方程式解释下列现象。
①将氯水滴加紫色石蕊溶液中,先变红后褪色________________________________ 。
②将氯水滴入硝酸银溶液中,有白色沉淀生成___________________________ 。
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是
(2)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的化学方程式为
(3)实验室用MnO2和浓盐酸为原料制备氯气,该反应的化学方程式为
(4)将实验室制的氯气配成新制的氯水含有多种微粒,试用化学方程式解释下列现象。
①将氯水滴加紫色石蕊溶液中,先变红后褪色
②将氯水滴入硝酸银溶液中,有白色沉淀生成
您最近一年使用:0次
2018-01-10更新
|
201次组卷
|
3卷引用:吉林省延边州敦化县2017-2018学年高一上学期期末考试化学试题
7 . 标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是
A.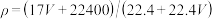 |
B.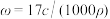 |
C.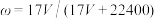 |
D. =1000Vρ/(17V+22400) =1000Vρ/(17V+22400) |
您最近一年使用:0次
2016-12-09更新
|
4931次组卷
|
130卷引用:【全国百强校】吉林省延边第二中学2018-2019学年高二下学期第二次月考化学试题
【全国百强校】吉林省延边第二中学2018-2019学年高二下学期第二次月考化学试题2010年普通高等学校招生全国统一考试理综化学部分(四川卷)2010年高考化学试题分项专题三 物质的量2010年高考化学试题分项专题十四 化学计算(已下线)2010年重庆一中高一下学期期末考试化学试题(已下线)2010年四川省成都七中高一上学期期中考试化学试卷(已下线)2010—2011学年黑龙江省哈六中高一上学期期末考试化学试卷(已下线)2010—2011学年辽宁省营口市高一上学期期末考试化学试卷(已下线)2011-2012学年浙江省嘉兴一中高一10月份月考化学试卷(已下线)2011-2012年辽宁省开原高中高一上学期第一次考试化学试卷(已下线)2011-2012学年浙江省嘉兴一中高二上学期期中考试化学试卷(已下线)2011-2012学年湖北省黄冈中学高一上学期期中考试化学试卷(已下线)2011-2012学年海南省琼海市嘉积中学高一上学期教学质量检测化学试卷(已下线)2011-2012学年甘肃省兰州市兰炼一中高一上学期期中考试化学试卷(已下线)2011-2012学年四川省成都市树德协进中学高一上学期期中考试化学试卷(已下线)2012-2013学年河北省石家庄市第二实验中学高一上学期期中考化学卷(已下线)2015届广西桂林市第十八中学高三上学期第一次月考化学试卷(已下线)2014-2015学年浙江嘉兴第一中学高一10月月考化学试卷2016届山东省枣庄市第二中学高三9月阶段性学情检测化学试题2016届广西桂林市第十八中学高三第一次月考化学试卷2015-2016学年山西大学附属中学高一上学期第一次月考化学试卷2015-2016学年广东省普宁一中高一上学期第三次月考化学试卷2015-2016学年四川省双流中学高一下入学考试化学试卷2015-2016学年广西桂林十八中高二下开学测化学试卷2015-2016学年河北省保定市高一上学期期末化学试卷2016-2017学年河北省邯郸一中高一上入学考试化学试卷2016-2017学年黑龙江牡丹江高级中学高一9月月考化学卷2017届湖北省大冶一中高三上学期8月月考化学试卷2017届福建省南安一中高三暑假阶段性考试化学试卷2016-2017学年宁夏育才中学高一上第一次月考化学试卷2016-2017学年河南省南阳一中高一上第一次月考化学卷2016-2017学年河北省定州二中高一上10月月考化学试卷2017届陕西省师范大学附属中学高三上学期第二次模考化学试卷山西省怀仁县第一中学(两校区)2016-2017学年高二下学期期末考试化学试题2018版化学(苏教版)高考总复习专题一对接高考精练--物质的量浓度及其溶液的配制山西省忻州市第一中学2016-2017学年高一必修一:第1章从实验学化学同步练习化学试题河南省南阳市第一中学2018届高三上学期第二次考试化学试题江西省新余市第一中学2018届高三毕业年级第二次模拟考试化学试题江西省崇义中学2017-2018学年高一上学期第一次月考化学试题湖南省长沙市实验中学2017-2018学年高一上学期第一次月考化学试题湖南省长沙市第一中学2017-2018学年高一上学期第一次阶段性检测化学试题黑龙江省哈尔滨市第三中学2017-2018学年高一上学期第一次验收考试化学试题新疆阿克苏市农一师中学2017-2018学年高一上学期第一次月考化学试题河南省周口市郸城县第一高级中学2017-2018学年高一10月月考化学试题河南省商丘市第一高级中学2017-2018学年高一上学期第一次月考化学试题天津市静海县第一中学2018届高三9月学生学业能力调研考试化学试题河南省中原名校(即豫南九校)2017-2018学年高一上学期期中联考化学试题安徽省定远重点中学2017-2018学年高一上学期期末考试化学试题陕西省西安市第一中学2017-2018学年高一上学期期末考试化学试题湖北省黄冈中学2017-2018学年高一上学期第一次月考化学试题【全国百强校】江西省新余市第一中学2017-2018学年高二下学期第三次段考化学试题【全国百强校】内蒙古集宁一中(东校区)2017-2018学年高二下学期期末考试化学试题黑龙江省青冈县一中2017-2018学年高二下学期期末考试化学试题(已下线)解密02 化学常用计量——备战2018年高考化学之高频考点解密安徽省肥东县高级中学2019届高三上学期8月调研考试化学试题(已下线)学科网2019年高考化学一轮复习讲练测1.2 物质的量浓度 测2018--2019高中化学《物质的量浓度》专项训练题【全国百强校】新疆维吾尔自治区乌鲁木齐市第一中学2019届高三上学期第一次月考(9月)化学试题湖南省岳阳县第一中学、汨罗市一中2018-2019学年高一上学期10月联考化学试题河南省豫西名校2018-2019学年高一上学期第一次联考化学试题湖南省长沙市周南梅溪湖中学2018-2019学年高一下学期一模检测化学试题河南省永城高中2018-2019学年高一上学期第一次月考化学试题【全国百强校】山西省太原市第五中学2018-2019学年高一上学期10月月考化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高一上学期10月模块诊断化学试题【全国百强校】辽宁省实验中学2018-2019学年高一上学期期中考试化学试题【全国百强校】甘肃省平凉市静宁县第一中学2019届高三上学期第三次模拟考试化学试题安徽省阜阳市第三中学2018-2019学年高一上学期小期末考试(期末模拟)化学试题【全国百强校】内蒙古自治区乌兰察布市集宁区第一中学2018-2019学年高一上学期期末考试化学试题河北省大名县第一中学2018-2019学年高二(普通班)5月月考化学试题贵州省铜仁第一中学2018-2019学年高二下学期期末考试化学试题(已下线)专题1.2 物质的量浓度(讲)-《2020年高考一轮复习讲练测》吉林省乾安县七中2017-2018学年高一上学期期中考试化学试卷河北省秦皇岛一中2019-2020学年高一上学期第一次月考化学试题黑龙江省鹤岗市第一中学2019-2020学年高一第一次月考化学试题河南省林州市第一中学2019-2020学年高一10月月考化学试题安徽省六安市舒城中学2019-2020学年高一上学期第一次月考化学试题2020届高三化学一轮复习 基本概念物质的量(过关检测)山西运城市康杰中学2019-2020学年高一上学期期中考试化学试题四川省遂宁市第二中学2019-2020学年高一上学期期中考试化学试题宁夏回族自治区石嘴山市第三中学2019-2020学年高一上学期期中考试化学试题内蒙古翁牛特旗乌丹第一中学2019-2020学年高一上学期期中考试化学试题山西省朔州市怀仁县第一中学2018-2019学年高一上学期第三次月考化学试题2020届高三化学化学二轮复习——高考常考题:质量分数、物质的量浓度的相关计算【精编25题】广西壮族自治区来宾市金秀县民族中学2019-2020学年高一上学期期末考试化学试题内蒙古包钢第一中学2019-2020学年高一上学期10月月考化学试题广西壮族自治区来宾市忻城县民族中学2019-2020学年高一上学期期末考试化学试题黑龙江省哈尔滨市第一中学2019-2020 学年高二下学期期末考试化学试题(已下线)2.2.2化学反应的计算 练习(2)——《高中新教材同步备课》(苏教版 必修第一册)(已下线)第1单元 化学计量在实验中的应用(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷鲁科版(2019)高一必修第一册第1章 认识化学科学 总结检测高一必修第一册(鲁科2019)第1章第3节 化学中常用的物理量——物质的量广东省深圳市外国语学校2021届高三第一次月考化学试题陕西省渭南高级中学2019-2020学年高一上学期第一次月考化学试题山西大学附属中学2020-2021学年高上学期10月月考化学试题四川省成都外国语学校2020-2021学年高一上学期10月月考化学试题甘肃省天水市第一中学2020-2021学年高一上学期第一学段考试化学试题(已下线)【新东方】【2019】【高一上】【期中考】【JEZ】【化学】【栾子豪制作】(已下线)【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二6月阶段性测试化学试题山西省太原市山西大学附属中学2020-2021学年高一上学期10月(总第一次)模块诊断化学试题四川省遂宁市射洪中学校2020-2021学年高一上学期第一次月考化学试题甘肃省临夏中学2020-2021学年高一上学期期中考试化学试题江西省上饶市横峰中学2020-2021学年高一上学期期中考试化学试题内蒙古自治区赤峰市第二实验中学2020-2021学年高一上学期10月月考化学试题四川省广元市川师大万达中学2020-2021学年高一上学期期中考试化学试题甘肃省天水市第三中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】绍兴qw72江西省南昌市八一中学、洪都中学等七校2020-2021学年高一上学期期末联考化学试题(已下线)专题03 溶液——备战2021年高考化学纠错笔记黑龙江省鹤岗市第一中学2020-2021学年高二下学期期中考试化学试题(已下线)专题02 物质的量在化学实验中的应用(热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)课时12 物质的量浓度与溶液的配制-2022年高考化学一轮复习小题多维练(全国通用)四川省遂宁市射洪中学2021-2022学年高一上学期第一次月考化学试题山东省济南市商河县第三中学2022届高三10月月考化学试题广东省湛江市第二十一中学2022届高三9月第二次月考化学试题上海实验高中2021-2022学年高一上学期第一次测试化学试题辽宁省实验中学分校2017-2018学年高一上学期期中考试化学试题北京市第二十中学2021-2022学年高一上学期期中考试化学试题辽宁省沈阳市东北育才学校2020届高三上学期第一次模拟考试化学试题上海市黄浦区大同中学2021-2022学年高一上学期期中考试化学试题上海外国语大学附属外国语学校松江云间中学2021-2022学年高一上学期10月测试化学试题黑龙江省大庆中学2021-2022学年高一上学期期末考试化学试题北京市汇文中学2021-2022学年高一上学期期末考试化学试卷(已下线)第02讲 物质的量浓度与溶液的配制(练)-2023年高考化学一轮复习讲练测(全国通用)黑龙江省哈尔滨师范大学附属中学2021-2022学年高一下学期期末考试化学试题(已下线)2.2.2 物质的量浓度相关计算(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)黑龙江省齐齐哈尔市八校联合体2022-2023学年高三上学期期中考试化学试题黑龙江省实验中学2022-2023学年高一上学期期中测试化学试题上海市浦东新区上海中学东校2022-2023学年高一上学期第一次阶段性素质评估化学试题上海市实验学校2021-2022学年高一上学期第一次测试化学试题甘肃省兰州第一中学2023-2024学年高一上学期12月月考化学试题



