名校
1 . 已知A、B、C、D、E、F、G、H是原子序数依次增大的短周期主族元素,已知A的某种原子核内没有中子,A和D,C和G分别为同一主族元素,B原子的最外层电子数比次外层多3,F的最高价氧化物的水化物既可以和强酸反应也可以和强碱溶液反应,G的单质常出现在火山口。
(1)C在元素周期表中的位置是_______ 。
(2)C、D分别形成的简单离子中,半径较大的是______ (填离子符号)。
(3)G和H的最高价氧化物的水化物酸性较强的是______ (填化学式)。
(4)由A、C、D形成的化合物中化学键的类型为_______ ,C、D形成摩尔质量为 的化合物的电子式为
的化合物的电子式为______ ,由A、B形成 化合物的结构式为
化合物的结构式为______ 。
(5)甲烷可与 组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式
组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式_______ 。
(6)D、F的最高价氧化物的水化物相互反应的离子方程式为_______ 。
(7)可用湿润的______ 试纸检验H对应单质,涉及反应的离子方程式为_______ 。
(8)由B、H形成的化合物分子中,B和H原子的最外层均达到8电子稳定结构,该化合物遇水可反应生成一种具有漂白性的化合物,写出反应的化学方程式:________ 。
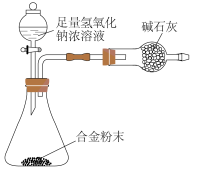
(9)E与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中E元素的含量。(装置中因空气质量引起的误差忽略不计)实验需要测定三个物理量:合金的质量m,反应前装置和药品的总质量a以及反应后装置和药品的总质量b,合金中E元素的质量分数是______ (用含m、a、b的式子表示)。
(1)C在元素周期表中的位置是
(2)C、D分别形成的简单离子中,半径较大的是
(3)G和H的最高价氧化物的水化物酸性较强的是
(4)由A、C、D形成的化合物中化学键的类型为
 的化合物的电子式为
的化合物的电子式为 化合物的结构式为
化合物的结构式为(5)甲烷可与
 组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式
组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式(6)D、F的最高价氧化物的水化物相互反应的离子方程式为
(7)可用湿润的
(8)由B、H形成的化合物分子中,B和H原子的最外层均达到8电子稳定结构,该化合物遇水可反应生成一种具有漂白性的化合物,写出反应的化学方程式:
(9)E与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中E元素的含量。(装置中因空气质量引起的误差忽略不计)实验需要测定三个物理量:合金的质量m,反应前装置和药品的总质量a以及反应后装置和药品的总质量b,合金中E元素的质量分数是
您最近半年使用:0次
2024-04-23更新
|
107次组卷
|
2卷引用:福建省厦门双十中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
2 . 五种短周期元素在周期表中的位置如图所示。已知:W元素原子的最外层电子数是次外层的2倍,下列说法正确的是

| A.5种元素最高价氧化物的水化物都是酸 |
| B.WZ4、MX2中所含化学键类型相同,熔点都很高 |
| C.简单氢化物的稳定性:X>Y |
| D.只有一种X的氢化物与Y的氧化物发生反应生成强酸 |
您最近半年使用:0次
解题方法
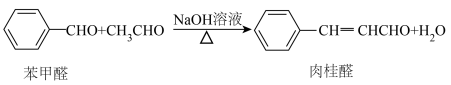
3 . 桂皮中含有的肉桂醛是一种食用香料,工业上可通过如下反应制备肉桂醛: 为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是
 为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是A.0.5mol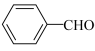 分子中含有的σ键数目为 分子中含有的σ键数目为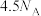 |
B.标准状况下, 含有的π键数目为 含有的π键数目为 |
C.1mol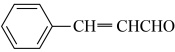 中 中 杂化的碳原子数为 杂化的碳原子数为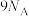 |
D.1L0.1mol/LNaOH溶液中含有的氧原子数目为 |
您最近半年使用:0次
4 . 短周期元素A、B、C、D的原子序数依次增大,A元素原子的核外电子只有一种运动状态:基态B原子s能级的电子总数比p能级的多1;基态C原子中成对电子数是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题
(1)B原子的轨道表示式___________ 。
(2)A和C原子个数比为1∶1的化合物的电子式___________ 。
(3)元素A、B、C中,第一电离能最大的是___________ (填元素名称)。
(4)在B、C、D三种元素的简单离子中,其离子的半径最小的是___________ 。(填离子符号)
(5)C的简单氢化物的键角小于B的简单氢化物,其原因是___________ 。
(6)BC₃的空间结构为___________ 。
(7)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB晶体的密度为a g⋅cm ,则晶体中两个最近D原子之间的距离为
,则晶体中两个最近D原子之间的距离为___________ pm(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
(1)B原子的轨道表示式
(2)A和C原子个数比为1∶1的化合物的电子式
(3)元素A、B、C中,第一电离能最大的是
(4)在B、C、D三种元素的简单离子中,其离子的半径最小的是
(5)C的简单氢化物的键角小于B的简单氢化物,其原因是
(6)BC₃的空间结构为
(7)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB晶体的密度为a g⋅cm
 ,则晶体中两个最近D原子之间的距离为
,则晶体中两个最近D原子之间的距离为 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。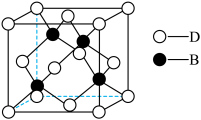
您最近半年使用:0次
5 . 元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表列出了七种元素在元素周期表中的位置,回答下列问题:
(1)表中C在周期表的位置是___________ 。
(2)元素E与元素H相比,金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ (填字母序号)。
a.H的最高价氧化物对应的水化物的碱性比E的强
b.E的化合价比H的低
c.常温下E的单质与水反应的程度很剧烈,而H的单质在加热条件下才能与水反应
(3)画出硫的原子结构示意图:___________ ;画出氧离子的结构示意图:___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | |||||
| 3 | E | F | ||||||
| 4 | H |
(2)元素E与元素H相比,金属性较强的是
a.H的最高价氧化物对应的水化物的碱性比E的强
b.E的化合价比H的低
c.常温下E的单质与水反应的程度很剧烈,而H的单质在加热条件下才能与水反应
(3)画出硫的原子结构示意图:
您最近半年使用:0次
名校
解题方法
6 . 下列电离方程式的书写正确的是
A.水溶液中:NaHCO3=Na++H++CO | B.H2CO3的电离:H2CO3 2H++CO 2H++CO |
C.Fe(OH)3的电离:Fe(OH)3 Fe3++3OH- Fe3++3OH- | D.水溶液中HF的电离:HF=H++F- |
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
7 . 探究pH对 溶液的配制和保存的影响。
溶液的配制和保存的影响。
I. 溶液的配制
溶液的配制
将 分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
II. 溶液的保存
溶液的保存
将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
(1)①中的浑浊主要是FeOOH,用离子方程式表示其生成过程_______ 。
(2)该实验的初步结论:保存 溶液的最佳pH是
溶液的最佳pH是_______ 。
(3)进一步探究pH对 变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后: 接近2mol/L,电流没有明显变化;
接近2mol/L,电流没有明显变化;
ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因_______ 。
b.依据实验i和ii推断:③比②中 更易变质的原因是
更易变质的原因是_______ 。
c.按上述原理进行实验,证实①中 更易变质的主要原因是
更易变质的主要原因是 的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,_______ 。
 溶液的配制和保存的影响。
溶液的配制和保存的影响。I.
 溶液的配制
溶液的配制将
 分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:| 编号 | 溶剂 | 溶液性状 | |
| ① | 蒸馏水 | 浅黄色澄清溶液 |  ;滴加1mol/LKSCN溶液无明显变化 ;滴加1mol/LKSCN溶液无明显变化 |
| ② |  | 无色澄清溶液 |  ;滴加1mol/LKSCN溶液微微变红 ;滴加1mol/LKSCN溶液微微变红 |
| ③ |  | 无色澄清溶液 | 滴加1mol/LKSCN溶液微微变红 |
 溶液的保存
溶液的保存将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
| 编号 | 溶液性状 | |
| ① | 橙色浑浊 | 用 酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 |
| ② | 无色溶液 | 滴加1mol/L的KSCN溶液后显浅红色 |
| ③ | 无色溶液 | 滴加1mol/L的KSCN溶液后显红色,颜色比②略深 |
(2)该实验的初步结论:保存
 溶液的最佳pH是
溶液的最佳pH是(3)进一步探究pH对
 变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后: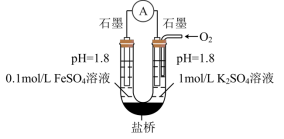
 接近2mol/L,电流没有明显变化;
接近2mol/L,电流没有明显变化;ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因
b.依据实验i和ii推断:③比②中
 更易变质的原因是
更易变质的原因是c.按上述原理进行实验,证实①中
 更易变质的主要原因是
更易变质的主要原因是 的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
您最近半年使用:0次
解题方法
8 . 短周期元素R、X、T、Z、Q中含有两种金属元素且原子半径依次增大,其中X和T同主族,R的最高正价与最低负价的绝对值相等,X、T的核电荷数之和等于Z、Q的核电荷数之和。下列说法错误的是
| A.非金属性:R<T<X |
| B.简单离子半径:Z<Q<X |
| C.常温下,T的最高价氧化物对应水化物的浓溶液与Z不反应 |
| D.Q、T分别与X形成的二元化合物的熔点:T<Q |
您最近半年使用:0次
解题方法
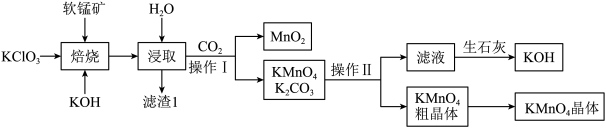
9 . 实验室模拟工业法用软锰矿(主要成分为MnO2,杂质不参与反应)制KMnO4,主要流程如下:
(1)补全“焙烧”时发生的化学反应方程式,并用单线桥标出电子转移方向和数目_____ 。_____ (填写范围)之间,理由是_____ 。
(3)有同学建议操作Ⅰ中用盐酸代替通CO2,分析是否合理_____ (选填“合理”或“不合理”),并说出理由_____ 。
(4)操作Ⅱ包括蒸发浓缩、_____ 、过滤、洗涤、干燥,为进一步提纯KMnO4晶体,应采用的实验方法是_____ 。
(5)为提高原料利用率,能循环利用的物质是_____ 。
A. KClO3 B. KOH C. K2MnO4 D. MnO2
(6)假设软锰矿中MnO2质量分数为52.2%,不考虑物质循环与制备过程中的损失,1t软锰矿理论上可制得KMnO4固体_____ kg。
(1)补全“焙烧”时发生的化学反应方程式,并用单线桥标出电子转移方向和数目
 MnO2+
MnO2+ KClO3+
KClO3+ KOH
KOH
 K2MnO4+
K2MnO4+ KCl+
KCl+
(3)有同学建议操作Ⅰ中用盐酸代替通CO2,分析是否合理
(4)操作Ⅱ包括蒸发浓缩、
(5)为提高原料利用率,能循环利用的物质是
A. KClO3 B. KOH C. K2MnO4 D. MnO2
(6)假设软锰矿中MnO2质量分数为52.2%,不考虑物质循环与制备过程中的损失,1t软锰矿理论上可制得KMnO4固体
您最近半年使用:0次
解题方法
10 . 某小组设计实验探究 和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
回答下列问题:
(1)装置B中试剂是________ (填名称),装置E的作用是____________ 。
(2)装置A中反应的离子方程式为______________ 。
(3)能证明氯的非金属性比硫强的实验现象是___________ 。经检验装置C中最终生成了 ,写出C中浑浊变澄清时反应的化学方程式:
,写出C中浑浊变澄清时反应的化学方程式:____________ 。
(4)根据装置D中现象,有人认为 被氧化了。请你设计实验证明他的观点是否正确:
被氧化了。请你设计实验证明他的观点是否正确:____________ 。
(5)实验完毕后,利用下列装置测定装置A中剩余盐酸的浓度:
将装置A中剩余溶液过滤,取 滤液进行实验,最终收集
滤液进行实验,最终收集 的体积为
的体积为 (已折合成标准状况)。
(已折合成标准状况)。
a.读数 b.冷却至室温 c.调平量气管和烧杯的液面
正确操作步骤的顺序为________ (填字母)。
②能与 反应的最低盐酸浓度为
反应的最低盐酸浓度为________  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
 和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
回答下列问题:
(1)装置B中试剂是
(2)装置A中反应的离子方程式为
(3)能证明氯的非金属性比硫强的实验现象是
 ,写出C中浑浊变澄清时反应的化学方程式:
,写出C中浑浊变澄清时反应的化学方程式:(4)根据装置D中现象,有人认为
 被氧化了。请你设计实验证明他的观点是否正确:
被氧化了。请你设计实验证明他的观点是否正确:(5)实验完毕后,利用下列装置测定装置A中剩余盐酸的浓度:
将装置A中剩余溶液过滤,取
 滤液进行实验,最终收集
滤液进行实验,最终收集 的体积为
的体积为 (已折合成标准状况)。
(已折合成标准状况)。
a.读数 b.冷却至室温 c.调平量气管和烧杯的液面
正确操作步骤的顺序为
②能与
 反应的最低盐酸浓度为
反应的最低盐酸浓度为 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
2024-04-18更新
|
425次组卷
|
4卷引用:河南省濮阳市2024届高三下学期第二次模拟考试理科综合化学试题
河南省濮阳市2024届高三下学期第二次模拟考试理科综合化学试题河南省濮阳市2024届高三第一次模拟考试理综-化学试题山西省晋中市2024届高三第二次优生测试理综合化学试题-(已下线)题型9 实验综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)



