名校
解题方法
1 . 反应Cl2+H2O=HCl+ HClO 生成的HClO具有杀菌消毒的作用。下列化学用语的表达正确的是
A.HClO 的电子式: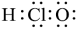 |
B.原子结构示意图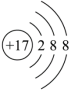 可表示 可表示 Cl-,也可表示 Cl-,也可表示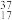 Cl- Cl- |
C.用电子式表示HCl的形成过程: |
D.水分子结构模型: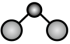 |
您最近一年使用:0次
2 . 用铁泥(主要成分为 、FeO和少量Fe)制备超顺磁性纳米
、FeO和少量Fe)制备超顺磁性纳米 (平均直径为25nm)的流程图如下(所加试剂均过量,部分步骤已省略),下列叙述正确的是
(平均直径为25nm)的流程图如下(所加试剂均过量,部分步骤已省略),下列叙述正确的是
 、FeO和少量Fe)制备超顺磁性纳米
、FeO和少量Fe)制备超顺磁性纳米 (平均直径为25nm)的流程图如下(所加试剂均过量,部分步骤已省略),下列叙述正确的是
(平均直径为25nm)的流程图如下(所加试剂均过量,部分步骤已省略),下列叙述正确的是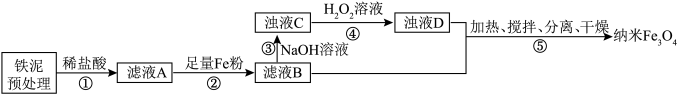
| A.滤液B的溶质主要为氯化铁 |
| B.步骤②中发生的反应均为置换反应 |
C.为防止在步骤⑤中继续氧化亚铁离子,步骤④反应完成后剩余的 需加热除去 需加热除去 |
D.将步骤⑤得到的纳米 均匀分散在水中时,不能产生丁达尔效应 均匀分散在水中时,不能产生丁达尔效应 |
您最近一年使用:0次
名校
解题方法
3 . 亚硝酸钙 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。 溶液能将NO氧化为
溶液能将NO氧化为 。
。
回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通 ,其目的是
,其目的是________ 。通 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是________ 。
(2)仪器a的名称为________ ,装置D中盛装的试剂是________ (填名称),装置E的作用是________ 。
(3)制备的产品 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为________ ,样品中 的纯度为
的纯度为________ (用含m、V的式子表示)。
 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。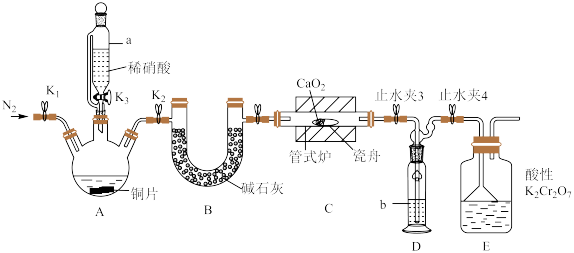
 溶液能将NO氧化为
溶液能将NO氧化为 。
。回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通
 ,其目的是
,其目的是 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是(2)仪器a的名称为
(3)制备的产品
 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: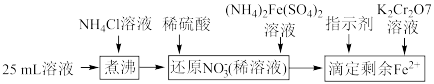
 ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为 的纯度为
的纯度为
您最近一年使用:0次
2024-06-01更新
|
292次组卷
|
7卷引用:江西省南昌市八一中学2024届高三下学期三模测试化学试题
解题方法
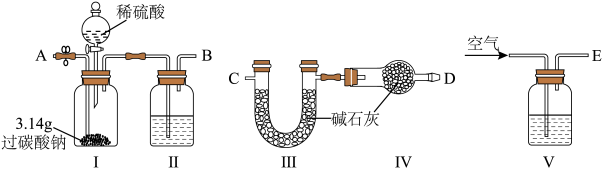
4 .  (过碳酸钠)是一种集洗涤、漂白、杀菌于一体的氧化系漂白剂,是碳酸钠和过氧化氢形成的不稳定加合物,易溶于水,难溶于乙醇。制备相关资料如下。
(过碳酸钠)是一种集洗涤、漂白、杀菌于一体的氧化系漂白剂,是碳酸钠和过氧化氢形成的不稳定加合物,易溶于水,难溶于乙醇。制备相关资料如下。
制备装置:如图所示。
i.按图组装仪器,控制实验温度不超过15℃;
ii.往A中加入25mL的过氧化氢(质量分数为30%)、硫酸镁和硅酸钠各0.1g,控温搅拌至所有试剂完全溶解;
iii.冷却至一定温度,加入100mL饱和碳酸钠溶液,搅拌反应30min,静置结晶;
iv.利用真空泵抽滤,滤饼用无水乙醇洗涤2~3次,通风橱风干得到产品过碳酸钠,滤液回收利用。
回答下列问题:
(1)仪器A的名称为___________ 。
(2)制备过程中,为了避免温度升高,导致产率下降,“加入100mL饱和碳酸钠溶液”的正确方法是___________ 。
(3)步骤iv用无水乙醇洗涤的原因是___________ 。
(4)下列有关过碳酸钠说法错误的是___________。
(5)采用下列装置验证过碳酸钠中碳酸钠和过氧化氢的物质的量之比是2∶3(不考虑过碳酸钠含有杂质)。 中的试剂为
中的试剂为___________ 。
②装置接口的连接顺序为___________ (用ABCDE字母表示)。
③若实验操作准确,则装置 理论上应增重
理论上应增重___________ g。
 (过碳酸钠)是一种集洗涤、漂白、杀菌于一体的氧化系漂白剂,是碳酸钠和过氧化氢形成的不稳定加合物,易溶于水,难溶于乙醇。制备相关资料如下。
(过碳酸钠)是一种集洗涤、漂白、杀菌于一体的氧化系漂白剂,是碳酸钠和过氧化氢形成的不稳定加合物,易溶于水,难溶于乙醇。制备相关资料如下。制备装置:如图所示。
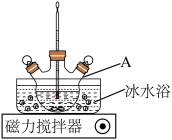
i.按图组装仪器,控制实验温度不超过15℃;
ii.往A中加入25mL的过氧化氢(质量分数为30%)、硫酸镁和硅酸钠各0.1g,控温搅拌至所有试剂完全溶解;
iii.冷却至一定温度,加入100mL饱和碳酸钠溶液,搅拌反应30min,静置结晶;
iv.利用真空泵抽滤,滤饼用无水乙醇洗涤2~3次,通风橱风干得到产品过碳酸钠,滤液回收利用。
回答下列问题:
(1)仪器A的名称为
(2)制备过程中,为了避免温度升高,导致产率下降,“加入100mL饱和碳酸钠溶液”的正确方法是
(3)步骤iv用无水乙醇洗涤的原因是
(4)下列有关过碳酸钠说法错误的是___________。
| A.过碳酸钠是一种混合物 |
| B.过碳酸钠既具有碳酸钠的性质,又具有双氧水性质 |
| C.往酸性高锰酸钾溶液中加入足量过碳酸钠,溶液褪成无色 |
| D.过碳酸钠既可用作绿色漂白剂也可用作鱼塘供氧剂 |
(5)采用下列装置验证过碳酸钠中碳酸钠和过氧化氢的物质的量之比是2∶3(不考虑过碳酸钠含有杂质)。
 中的试剂为
中的试剂为②装置接口的连接顺序为
③若实验操作准确,则装置
 理论上应增重
理论上应增重
您最近一年使用:0次
名校
解题方法
5 . 下列反应的离子方程式正确的是
A.向滴有酚酞的 溶液中滴入盐酸至红色恰好褪去: 溶液中滴入盐酸至红色恰好褪去: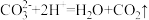 |
B.将硫酸铬溶液滴入含 的强碱性溶液中: 的强碱性溶液中: |
C.碳酸铵与氢氧化钙溶液反应:CO +Ca2+=CaCO3↓ +Ca2+=CaCO3↓ |
D.少量 通入苯酚钠溶液中: 通入苯酚钠溶液中: |
您最近一年使用:0次
名校
解题方法
6 . 实验室用含少量Fe2O3的废铁屑制取FeCO3的步骤如下:
i.用热的Na2CO3溶液洗涤废铁屑,过滤;
ii.向滤渣中加入稀硫酸和活性炭,充分溶解后过滤;
iii.向滤液中加入NH4HCO3溶液,过滤、洗涤可得FeCO3。
下列叙述错误的是
i.用热的Na2CO3溶液洗涤废铁屑,过滤;
ii.向滤渣中加入稀硫酸和活性炭,充分溶解后过滤;
iii.向滤液中加入NH4HCO3溶液,过滤、洗涤可得FeCO3。
下列叙述错误的是
| A.步骤i的目的是除去废铁屑表面的油脂 |
| B.活性炭可以加快铁屑与稀硫酸的反应速率 |
| C.步骤iii若用饱和Na2CO3溶液,FeCO3的产率会更高 |
| D.进行步骤iii前需要用KSCN溶液检验滤液中是否含有Fe3+ |
您最近一年使用:0次
7 . 实验室用如图所示装置检验草酸晶体( )分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入
)分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入 的盐酸溶液中生成黑色Pd粉。下列说法错误的是
的盐酸溶液中生成黑色Pd粉。下列说法错误的是
 )分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入
)分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入 的盐酸溶液中生成黑色Pd粉。下列说法错误的是
的盐酸溶液中生成黑色Pd粉。下列说法错误的是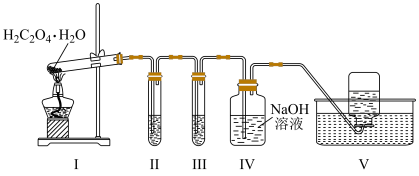
| A.Ⅰ中大试管口向上倾斜,可能因为草酸晶体的熔点低于分解温度 |
| B.由Ⅱ中现象可推断草酸晶体分解生成CO |
| C.Ⅱ、Ⅲ中现象可推断草酸晶体分解反应存在元素化合价变化 |
| D.可用燃烧法代替Ⅴ进行尾气处理 |
您最近一年使用:0次
8 . 根据所学知识填空
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:___________ 。
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
(3)向1mol KAl(SO4)2溶液中滴加Ba(OH)2溶液至沉淀的物质的量最大时的离子方程式___________
(4)现有以下四种物质:
请根据题意选择恰当的选项用字母代号填空。
①可与KSCN溶液反应,溶液变红的是___________ ;
②常用于焙制糕点,也可用作抗酸药的是___________ ;
③可用于制备硅胶和木材防火剂的是___________ ;
④可用于制造计算机芯片的是___________ 。
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
| A.黄绿色 | B.洋红色 | C.紫红色 | D.绿色 |
(4)现有以下四种物质:
| A.Si | B.FeCl3 | C.NaHCO3 | D.Na2SiO3 |
①可与KSCN溶液反应,溶液变红的是
②常用于焙制糕点,也可用作抗酸药的是
③可用于制备硅胶和木材防火剂的是
④可用于制造计算机芯片的是
您最近一年使用:0次
名校
解题方法
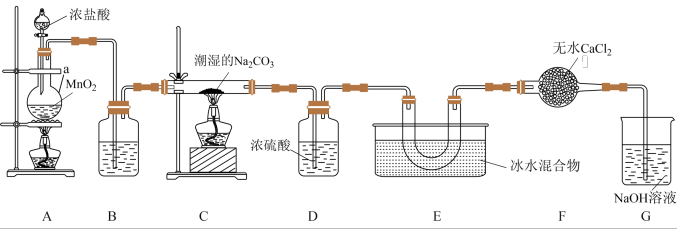
9 . 一氧化二氯( )是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集
)是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集 ,反应的原理如下:
,反应的原理如下: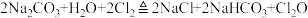 。
。
已知: 的部分性质如表所示
的部分性质如表所示
(1)装置A中仪器a的名称为______________ ,装置A中发生反应的化学方程式为______________ 。
(2)装置B中盛装的试剂的名称为______________ 。
(3)装置E采用冰水混合物冷却的目的是______________ 。
(4)装置F中无水 的作用是
的作用是______________ 。
(5)与传统消毒剂 比较,
比较, 消毒效率是
消毒效率是 的
的______________ 倍(产物视为 ,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
(6)某温度下,将氯气通入G装置中,反应得到 ,
, 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:_______________ 。
 )是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集
)是高效安全的杀菌消毒剂,某兴趣小组用下图所示装置制备并收集 ,反应的原理如下:
,反应的原理如下: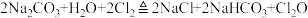 。
。已知:
 的部分性质如表所示
的部分性质如表所示| 物理性质 | 化学性质 |
常温下, 是棕黄色、有刺激性气味的气体;熔点:-120.6℃;沸点2.0℃ 是棕黄色、有刺激性气味的气体;熔点:-120.6℃;沸点2.0℃ |  易溶于水,同时与水反应生成 易溶于水,同时与水反应生成 |
(1)装置A中仪器a的名称为
(2)装置B中盛装的试剂的名称为
(3)装置E采用冰水混合物冷却的目的是
(4)装置F中无水
 的作用是
的作用是(5)与传统消毒剂
 比较,
比较, 消毒效率是
消毒效率是 的
的 ,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。
,消毒效率以单位质量得到的电子数表示,结果精确到0.01)。(6)某温度下,将氯气通入G装置中,反应得到
 ,
, 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是2NaCl(熔融) 2Na+Cl2↑。回答下列问题:
2Na+Cl2↑。回答下列问题:
(1)保存金属钠的正确方法是___________(填字母)。
(2)Na、NaOH久置在空气中最终都是变为___________ (填化学式)。
(3)将一小块金属钠投入CuCl2溶液中,发生反应的化学方程式为_______________ 。
Ⅱ. 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。
(4) 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与CO2反应的化学方程式
与CO2反应的化学方程式___________ 。
(5)将一定量的 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有___________ (填离子符号)。
(6)查阅资料知: 在一定条件下可以转化为
在一定条件下可以转化为 ,
, 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:
①已知 能发生如下反应:
能发生如下反应: ,上述反应中氧化产物是
,上述反应中氧化产物是___________ ;HI在反应中体现了什么性质___________ 。
②根据上述反应鉴别 和NaCl,可选择以下物质中的
和NaCl,可选择以下物质中的___________ 进行实验(填序号)。
A.食用白醋 B.碘化钾淀粉试纸 C.淀粉 D.白酒
 2Na+Cl2↑。回答下列问题:
2Na+Cl2↑。回答下列问题:(1)保存金属钠的正确方法是___________(填字母)。
| A.放在棕色瓶中 | B.放在细沙中 | C.放在水中 | D.放在煤油中 |
(3)将一小块金属钠投入CuCl2溶液中,发生反应的化学方程式为
Ⅱ.
 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。(4)
 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 与CO2反应的化学方程式
与CO2反应的化学方程式(5)将一定量的
 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有(6)查阅资料知:
 在一定条件下可以转化为
在一定条件下可以转化为 ,
, 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:①已知
 能发生如下反应:
能发生如下反应: ,上述反应中氧化产物是
,上述反应中氧化产物是②根据上述反应鉴别
 和NaCl,可选择以下物质中的
和NaCl,可选择以下物质中的A.食用白醋 B.碘化钾淀粉试纸 C.淀粉 D.白酒
您最近一年使用:0次



