1 . 用富含铁元素的食品,可以补充人体所需的铁元素。某班级研究性学习小组对菠菜中的铁元素展开了检测,实验如下:

(1)下列图示装置或操作合理的是________ 。
(2)写出试剂B的化学式___________ 。
(3)试剂C若为双氧水,请写出该反应的离子方程式:___________ ;该实验证明菠菜中含有的铁元素为_____ 价。
(4)其中一名同学在研究过程中向滤液A中先加入氯水,再加入试剂B,也看到溶液变红,由此也得出和其他同学一样的结论。他的做法是否正确?______ ,原因是什么?___________ 。
(5)另取少量滤液 ,向其中加入少量NaOH溶液,观察到的现象是
,向其中加入少量NaOH溶液,观察到的现象是________ ;原因是___________ 、________ (用离子方程式解释)。

(1)下列图示装置或操作合理的是
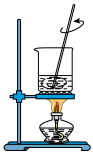 | 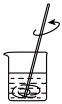 | 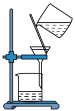 |  |
| A.灼烧 | B.溶解 | C.过滤 | D.检测菠菜液中的铁元素 |
(2)写出试剂B的化学式
(3)试剂C若为双氧水,请写出该反应的离子方程式:
(4)其中一名同学在研究过程中向滤液A中先加入氯水,再加入试剂B,也看到溶液变红,由此也得出和其他同学一样的结论。他的做法是否正确?
(5)另取少量滤液
 ,向其中加入少量NaOH溶液,观察到的现象是
,向其中加入少量NaOH溶液,观察到的现象是
您最近一年使用:0次
名校
解题方法
2 . 为测定某补血剂样品(主要成分是硫酸亚铁晶体 )中铁元素的含量,某学兴趣小组设计了如下实验方案:
)中铁元素的含量,某学兴趣小组设计了如下实验方案:
方案一:将 转化为
转化为 ,测定质量变化.
,测定质量变化.
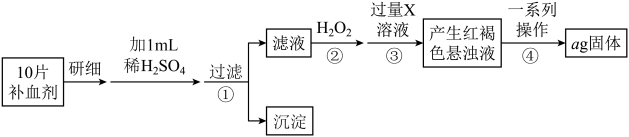
(1)写出步骤②中发生的反应的离子方程式__________________________
(2)步骤④中一系列操作依次是:过滤、洗涤、灼烧、冷却、称量,写出发生反应的化学方程式_______________________________ .
(3)假设实验无损耗,则每片补血剂含铁元素的质量为____________ g(用含a的代数式表示)。
方案二:用酸性 溶液滴定测定铁元素的含量
溶液滴定测定铁元素的含量
实验前,首先要准确配制 的酸性
的酸性 溶液250mL
溶液250mL
(4)计算所需 固体的质量为
固体的质量为____________ g.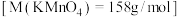
(5)配制溶液时,必须用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、________________
(6)配制过程中,下列操作导致溶液浓度偏小的是(填序号)_______
A.加水定容时俯视刻度线
B.定容加水时超过刻度线后,立即吸出多余的水
C.溶液从烧杯转移到容量瓶后没有洗涤烧杯
(7)若某同学取5片补血剂样品配成100mL溶液,取20.00mL,用上述操作配置的 溶液滴定,耗去
溶液滴定,耗去 ,反应的离子方程式为
,反应的离子方程式为______________________ ,每片补血剂含铁元素的质量____________ g(用代数式表示).
 )中铁元素的含量,某学兴趣小组设计了如下实验方案:
)中铁元素的含量,某学兴趣小组设计了如下实验方案:方案一:将
 转化为
转化为 ,测定质量变化.
,测定质量变化.
(1)写出步骤②中发生的反应的离子方程式
(2)步骤④中一系列操作依次是:过滤、洗涤、灼烧、冷却、称量,写出发生反应的化学方程式
(3)假设实验无损耗,则每片补血剂含铁元素的质量为
方案二:用酸性
 溶液滴定测定铁元素的含量
溶液滴定测定铁元素的含量实验前,首先要准确配制
 的酸性
的酸性 溶液250mL
溶液250mL(4)计算所需
 固体的质量为
固体的质量为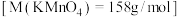
(5)配制溶液时,必须用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、
(6)配制过程中,下列操作导致溶液浓度偏小的是(填序号)
A.加水定容时俯视刻度线
B.定容加水时超过刻度线后,立即吸出多余的水
C.溶液从烧杯转移到容量瓶后没有洗涤烧杯
(7)若某同学取5片补血剂样品配成100mL溶液,取20.00mL,用上述操作配置的
 溶液滴定,耗去
溶液滴定,耗去 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
3 . 硅氯仿( ,熔点
,熔点 ,沸点
,沸点 )遇水分解,易发生氧化反应,实验室利用硅粉和氯化氢在温度为
)遇水分解,易发生氧化反应,实验室利用硅粉和氯化氢在温度为 条件下制备硅氯仿。
条件下制备硅氯仿。
回答下列问题:
(1)实验室将 固体与浓
固体与浓 混合加热制取
混合加热制取 。
。

①选用图甲所示装置制取并收集一瓶纯净且干燥的 ,连接顺序为
,连接顺序为___________ (用小写字母表示,气流方向从左往右,个别装置可以多次选用)。
② 固体与浓
固体与浓 反应还生成一种酸式盐,该反应的化学方程式为
反应还生成一种酸式盐,该反应的化学方程式为___________ 。
(2)硅粉和氯化氢反应制备硅氯仿的装置如图乙所示(夹持仪器已略去)。

① 在空气中能够自燃,其中氢元素的化合价为
在空气中能够自燃,其中氢元素的化合价为___________ 。
②仪器A中发生反应的化学方程式为___________ 。
③设置装置B的目的是___________ 。
④C口需要连接丙装置的___________ (填“D”或“E”)口, 溶液的作用是:a.
溶液的作用是:a.___________ ;b.吸收氧气,防止氧气进入A中与硅氯仿反应,用离子方程式表示其吸收 的原理:
的原理:___________ 。
 ,熔点
,熔点 ,沸点
,沸点 )遇水分解,易发生氧化反应,实验室利用硅粉和氯化氢在温度为
)遇水分解,易发生氧化反应,实验室利用硅粉和氯化氢在温度为 条件下制备硅氯仿。
条件下制备硅氯仿。回答下列问题:
(1)实验室将
 固体与浓
固体与浓 混合加热制取
混合加热制取 。
。
①选用图甲所示装置制取并收集一瓶纯净且干燥的
 ,连接顺序为
,连接顺序为②
 固体与浓
固体与浓 反应还生成一种酸式盐,该反应的化学方程式为
反应还生成一种酸式盐,该反应的化学方程式为(2)硅粉和氯化氢反应制备硅氯仿的装置如图乙所示(夹持仪器已略去)。

①
 在空气中能够自燃,其中氢元素的化合价为
在空气中能够自燃,其中氢元素的化合价为②仪器A中发生反应的化学方程式为
③设置装置B的目的是
④C口需要连接丙装置的
 溶液的作用是:a.
溶液的作用是:a. 的原理:
的原理:
您最近一年使用:0次
解题方法
4 . 工业废水任意排放,是造成环境污染的最大祸首。协同去污,变废为宝,为处理工业废水提供了新思路。永固电镀厂产生大量含FeSO4、CuSO4的电镀废液,水光皮革厂产生大量含K2Cr2O7的废液。两厂联合处理废水,回收Cu并生产铁红和媒染剂Cr2(SO4)3•6H2O,工艺流程如图:
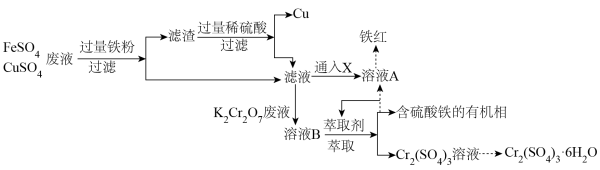
(1)K2Cr2O7中Cr元素的化合价为_______ 。
(2)处理滤渣时,要保持通风,并严禁烟火,其原因是_______ 。
(3)滤液可以通入X一步转化为溶液A,检验溶液A中金属阳离子的试剂是______ ,X可以是下列选项中的哪些物质_______ 。
A.CO2 B.O2 C.Cl2 D.SO2
(4)滤液与含K2Cr2O7的废液反应的离子方程式为_______ 。
(5)从Cr2(SO4)3溶液制取Cr2(SO4)3•6H2O晶体的实验操作方法为_______ 、_______ 、过滤、洗涤、干燥。
(6)已知Cr(OH)3化学性质与Al(OH)3类似,选择合适的化学试剂,将流程中的Cr2(SO4)3溶液转化为可用于陶瓷和搪瓷的着色剂Cr2O3(绿色粉末,广泛用于陶瓷和搪瓷的着色剂),转化过程中发生的主要的化学方程式为:_______ 、_______ 。

(1)K2Cr2O7中Cr元素的化合价为
(2)处理滤渣时,要保持通风,并严禁烟火,其原因是
(3)滤液可以通入X一步转化为溶液A,检验溶液A中金属阳离子的试剂是
A.CO2 B.O2 C.Cl2 D.SO2
(4)滤液与含K2Cr2O7的废液反应的离子方程式为
(5)从Cr2(SO4)3溶液制取Cr2(SO4)3•6H2O晶体的实验操作方法为
(6)已知Cr(OH)3化学性质与Al(OH)3类似,选择合适的化学试剂,将流程中的Cr2(SO4)3溶液转化为可用于陶瓷和搪瓷的着色剂Cr2O3(绿色粉末,广泛用于陶瓷和搪瓷的着色剂),转化过程中发生的主要的化学方程式为:
您最近一年使用:0次
5 . 某电子厂腐蚀废液含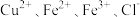 ,为了减少污染并变废为宝,工厂计划从废液中回收金属铜,并重新获得
,为了减少污染并变废为宝,工厂计划从废液中回收金属铜,并重新获得 溶液,请根据以下流程图,回答下列问题。
溶液,请根据以下流程图,回答下列问题。
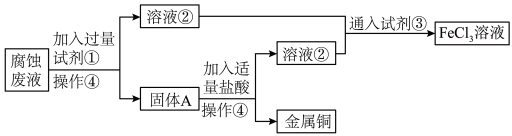
(1)②_______ (化学式)、③_______ (化学式)、④_______ (操作)。
(2)腐蚀废液中加入过量试剂①,写出发生反应的离子方程式_______ 。
(3)证明溶液②中不含 ,可往溶液中滴加
,可往溶液中滴加_______ (化学式)溶液。
(4)若已知处理前原腐蚀废液中 的质量
的质量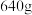 ,固体A的质量
,固体A的质量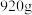 ,则流程图中加入适量盐酸(浓度
,则流程图中加入适量盐酸(浓度 )的体积至少
)的体积至少_______ L。
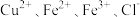 ,为了减少污染并变废为宝,工厂计划从废液中回收金属铜,并重新获得
,为了减少污染并变废为宝,工厂计划从废液中回收金属铜,并重新获得 溶液,请根据以下流程图,回答下列问题。
溶液,请根据以下流程图,回答下列问题。
(1)②
(2)腐蚀废液中加入过量试剂①,写出发生反应的离子方程式
(3)证明溶液②中不含
 ,可往溶液中滴加
,可往溶液中滴加(4)若已知处理前原腐蚀废液中
 的质量
的质量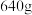 ,固体A的质量
,固体A的质量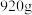 ,则流程图中加入适量盐酸(浓度
,则流程图中加入适量盐酸(浓度 )的体积至少
)的体积至少
您最近一年使用:0次
2023-02-10更新
|
240次组卷
|
2卷引用:广东省江门市2022-2023学年高一上学期调研测试(一)期末考试化学试题
名校
6 . 向仅含有 、
、 、
、 的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示。
的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示。

提示:①不考虑 、
、 与水的反应;
与水的反应;
②不考虑气体的逸出;
③不考虑水电离出的 和
和 。
。
④产物只有 、
、 和
和 。
。
回答下列问题:
(1)
_______ ,曲线I对应的离子方程式为_______ 。
(2)b点溶液中,共含有_______ 种离子,分别为_______ (填离子符号)。
(3)
_______ ,曲线II对应的离子方程式为_______ 。
(4)c点溶液中,阳离子的总物质的量与阴离子的总物质的量之比为_______ 。
 、
、 、
、 的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示。
的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示。
提示:①不考虑
 、
、 与水的反应;
与水的反应;②不考虑气体的逸出;
③不考虑水电离出的
 和
和 。
。④产物只有
 、
、 和
和 。
。回答下列问题:
(1)

(2)b点溶液中,共含有
(3)

(4)c点溶液中,阳离子的总物质的量与阴离子的总物质的量之比为
您最近一年使用:0次
2023-02-08更新
|
519次组卷
|
4卷引用:河北省保定市定州市第二中学2022-2023学年高一下学期开学考试化学试题
名校
解题方法
7 . 填空。
(1)共沉淀法制备磁性纳米Fe3O4微粒的工业流程如下:

①“共沉”制备的 粒子
粒子离子方程式 为:_______ 。
② 对
对 粒子制备有较大的影响。
粒子制备有较大的影响。
若 过量,过量的
过量,过量的 会生成副产物
会生成副产物 ,生成副产物
,生成副产物 的
的离子方程式 为:_______ 。实际投料时, 略小于理论反应的比值,这是因为部分
略小于理论反应的比值,这是因为部分 会直接生成
会直接生成 粒子,该反应的
粒子,该反应的离子方程式 为:_______ 。
(2)一化学研究性学习小组对某工厂生产印刷电路板后所得废液进行探究,要确定废液的组成及各金属离子的浓度。
取几滴废液于试管中加水稀释后,滴加KSCN溶液出现血红色,可知废液中除含有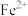 、
、 外,还含有
外,还含有 。甲同学取10 mL废液,向其中加入足量的
。甲同学取10 mL废液,向其中加入足量的 溶液,得到的沉淀经过滤、洗涤、干燥,称重8.61 g。乙同学另取10 mL废液,加入某试剂将pH调至4.0,使其中
溶液,得到的沉淀经过滤、洗涤、干燥,称重8.61 g。乙同学另取10 mL废液,加入某试剂将pH调至4.0,使其中 转化为
转化为 沉淀,而
沉淀,而 、
、 仍留在废液中,沉淀经过滤、洗涤、灼烧,冷却后称重得0.32g。
仍留在废液中,沉淀经过滤、洗涤、灼烧,冷却后称重得0.32g。
通过计算可知废液中:
_______ mol·L ,
,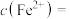
_______ mol·L ,
,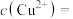
_______ mol·L 。
。
(1)共沉淀法制备磁性纳米Fe3O4微粒的工业流程如下:

①“共沉”制备的
 粒子
粒子②
 对
对 粒子制备有较大的影响。
粒子制备有较大的影响。若
 过量,过量的
过量,过量的 会生成副产物
会生成副产物 ,生成副产物
,生成副产物 的
的 略小于理论反应的比值,这是因为部分
略小于理论反应的比值,这是因为部分 会直接生成
会直接生成 粒子,该反应的
粒子,该反应的(2)一化学研究性学习小组对某工厂生产印刷电路板后所得废液进行探究,要确定废液的组成及各金属离子的浓度。
取几滴废液于试管中加水稀释后,滴加KSCN溶液出现血红色,可知废液中除含有
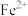 、
、 外,还含有
外,还含有 。甲同学取10 mL废液,向其中加入足量的
。甲同学取10 mL废液,向其中加入足量的 溶液,得到的沉淀经过滤、洗涤、干燥,称重8.61 g。乙同学另取10 mL废液,加入某试剂将pH调至4.0,使其中
溶液,得到的沉淀经过滤、洗涤、干燥,称重8.61 g。乙同学另取10 mL废液,加入某试剂将pH调至4.0,使其中 转化为
转化为 沉淀,而
沉淀,而 、
、 仍留在废液中,沉淀经过滤、洗涤、灼烧,冷却后称重得0.32g。
仍留在废液中,沉淀经过滤、洗涤、灼烧,冷却后称重得0.32g。通过计算可知废液中:

 ,
,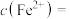
 ,
,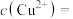
 。
。
您最近一年使用:0次
8 . 碘及其化合物广泛用于医药、染料等方面。碘酸是一种强酸,其水溶液有强氧化性。已知氧化性: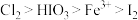 。回答下列问题:
。回答下列问题:
(1)一种以含有少量 的废液为原料制备
的废液为原料制备 的方法如图所示。
的方法如图所示。
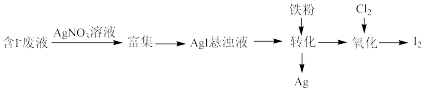
①“转化”生成的Ag溶于稀硝酸可获得硝酸银,写出Ag与稀硝酸反应的离子方程式:___________ 。
②通入 的过程中,若
的过程中,若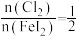 ,则反应中被氧化的元素为
,则反应中被氧化的元素为___________ (填元素符号);当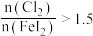 后,单质碘的产率会降低,原因是
后,单质碘的产率会降低,原因是___________ 。
(2)大量的碘由自然界的 与还原剂
与还原剂 反应制得,则该制备
反应制得,则该制备 的反应中的氧化剂和还原剂的物质的量之比为
的反应中的氧化剂和还原剂的物质的量之比为___________ 。
(3)卤素互化物 可发生水解反应,生成卤离子和卤氧离子(为非氧化还原反应),写出反应的离子方程式:
可发生水解反应,生成卤离子和卤氧离子(为非氧化还原反应),写出反应的离子方程式:___________ 。
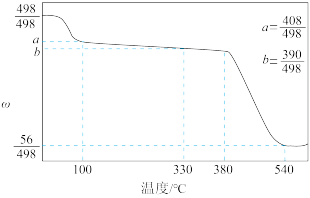
(4)碘酸钙是食品及饲料添加剂中补碘补钙的常用试剂,微溶于水。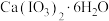 加热升温过程中剩余固体的质量分数w(
加热升温过程中剩余固体的质量分数w( )随温度变化的关系如图所示。为获得无水碘酸钙,可将
)随温度变化的关系如图所示。为获得无水碘酸钙,可将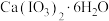 晶体
晶体___________ (填实验操作)。若将加热温度提高至540℃,则此时得到固体的主要成分为___________ (填化学式)。
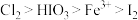 。回答下列问题:
。回答下列问题:(1)一种以含有少量
 的废液为原料制备
的废液为原料制备 的方法如图所示。
的方法如图所示。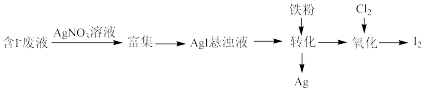
①“转化”生成的Ag溶于稀硝酸可获得硝酸银,写出Ag与稀硝酸反应的离子方程式:
②通入
 的过程中,若
的过程中,若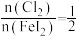 ,则反应中被氧化的元素为
,则反应中被氧化的元素为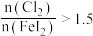 后,单质碘的产率会降低,原因是
后,单质碘的产率会降低,原因是(2)大量的碘由自然界的
 与还原剂
与还原剂 反应制得,则该制备
反应制得,则该制备 的反应中的氧化剂和还原剂的物质的量之比为
的反应中的氧化剂和还原剂的物质的量之比为(3)卤素互化物
 可发生水解反应,生成卤离子和卤氧离子(为非氧化还原反应),写出反应的离子方程式:
可发生水解反应,生成卤离子和卤氧离子(为非氧化还原反应),写出反应的离子方程式:(4)碘酸钙是食品及饲料添加剂中补碘补钙的常用试剂,微溶于水。
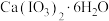 加热升温过程中剩余固体的质量分数w(
加热升温过程中剩余固体的质量分数w( )随温度变化的关系如图所示。为获得无水碘酸钙,可将
)随温度变化的关系如图所示。为获得无水碘酸钙,可将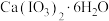 晶体
晶体
您最近一年使用:0次
2022-09-26更新
|
369次组卷
|
4卷引用:贵州省2022-2023学年高三上学期联考化学试题
9 . 化合物X由4种元素组成,按如下流程进行探究:

已知混合气体E与G的成分及成分之间比例相同,且G的质量是E的1.5倍。
请回答:
(1)组成X的四种元素_______ (填元素符号),X的化学式_______ 。
(2)写出固体B使酸性高锰酸钾溶液褪色的离子方程式_______ 。
(3)X分解成A、B、C的化学方程式_______ 。
(4)探究固体D时把 溶液改为氯水,逐滴加入氯水至过量的过程中,溶液先变血红色后褪色,褪色的原因可能是
溶液改为氯水,逐滴加入氯水至过量的过程中,溶液先变血红色后褪色,褪色的原因可能是_______ 。请设计实验证明_______ 。

已知混合气体E与G的成分及成分之间比例相同,且G的质量是E的1.5倍。
请回答:
(1)组成X的四种元素
(2)写出固体B使酸性高锰酸钾溶液褪色的离子方程式
(3)X分解成A、B、C的化学方程式
(4)探究固体D时把
 溶液改为氯水,逐滴加入氯水至过量的过程中,溶液先变血红色后褪色,褪色的原因可能是
溶液改为氯水,逐滴加入氯水至过量的过程中,溶液先变血红色后褪色,褪色的原因可能是
您最近一年使用:0次
名校
10 . 某实验小组测定铁的氧化物FexOy的化学式,已知该氧化物中铁元素只有+2和+3两种价态,实验步骤如图,下列说法正确的是
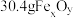

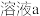
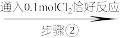
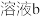
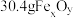

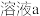
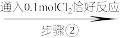
| A.步骤①和步骤②都发生了氧化还原反应 | B.溶液a中阳离子只有Fe3+和Fe2+ |
| C.溶液b中n(Fe3+):n(Cl-)=1:3 | D.通过计算可得该氧化物的化学式为:Fe4O5 |
您最近一年使用:0次
2022-03-03更新
|
635次组卷
|
3卷引用:河南省信阳市2021-2022学年高一上学期期末考试化学试题
河南省信阳市2021-2022学年高一上学期期末考试化学试题(已下线)第13讲 铁和铁的氧化物-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)江西省南昌市第二中学2023-2024学年高一上学期12月月考考试化学试题



