1 . 根据要求回答下列问题。
(1)在标准状况下,①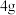
 ②
②
 ③
③
 中,含原子数最多的是
中,含原子数最多的是_______ (填序号),体积最小的是_______ (填序号)。
(2)现有由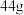
 和
和
 组成的混合气体,该混合气体中的
组成的混合气体,该混合气体中的 和
和 物质的量之比为
物质的量之比为_______ ,该混合气体的平均摩尔质量为_______ (保留一位小数)。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打受热分解的化学方程式:_______ 。
(4)84消毒液(主要成分是 )和洁厕灵(主要成分是
)和洁厕灵(主要成分是 )同时使用时生成有毒气体,用离子方程式表示该反应
)同时使用时生成有毒气体,用离子方程式表示该反应_______ 。
(5)某溶液中有 、
、 、
、 、
、 等离子,向其中加入足量的
等离子,向其中加入足量的 后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。
后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。
(1)在标准状况下,①
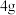
 ②
②
 ③
③
 中,含原子数最多的是
中,含原子数最多的是(2)现有由
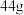
 和
和
 组成的混合气体,该混合气体中的
组成的混合气体,该混合气体中的 和
和 物质的量之比为
物质的量之比为(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打受热分解的化学方程式:
(4)84消毒液(主要成分是
 )和洁厕灵(主要成分是
)和洁厕灵(主要成分是 )同时使用时生成有毒气体,用离子方程式表示该反应
)同时使用时生成有毒气体,用离子方程式表示该反应(5)某溶液中有
 、
、 、
、 、
、 等离子,向其中加入足量的
等离子,向其中加入足量的 后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。
后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。A. | B. | C. 和 和 | D. |
您最近一年使用:0次
2 . 三氯化铁是一种很重要的铁盐,主要用于污水处理,具有效果好、价格便宜等优点。一定量的已生锈的铁屑,恰好溶解于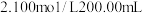 的盐酸中;充分反应后过滤,经检测所得的滤液中
的盐酸中;充分反应后过滤,经检测所得的滤液中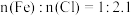 。往滤液中再通入足量
。往滤液中再通入足量 制得
制得 溶液(假设废铁屑中的杂质不与盐酸反应,氧化后制得的
溶液(假设废铁屑中的杂质不与盐酸反应,氧化后制得的 溶液仍为
溶液仍为 )。
)。
(1)滤液中
____  ,
, 和
和 的物质的量之比为
的物质的量之比为______ 。
(2)要将滤液中 恰好转化为
恰好转化为 ,理论上需通入
,理论上需通入____ L标准状况的氯气。
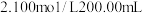 的盐酸中;充分反应后过滤,经检测所得的滤液中
的盐酸中;充分反应后过滤,经检测所得的滤液中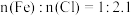 。往滤液中再通入足量
。往滤液中再通入足量 制得
制得 溶液(假设废铁屑中的杂质不与盐酸反应,氧化后制得的
溶液(假设废铁屑中的杂质不与盐酸反应,氧化后制得的 溶液仍为
溶液仍为 )。
)。(1)滤液中

 ,
, 和
和 的物质的量之比为
的物质的量之比为(2)要将滤液中
 恰好转化为
恰好转化为 ,理论上需通入
,理论上需通入
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
3 . 向100mLFeBr2溶液中通入0.1mol氯气,发现溶液中有一半溴离子被氧化为溴单质,求FeBr2溶液的物质的量的浓度__________ 。
提示:把xmolFeBr2分开,为xmolFe2+和2xmolBr-,Cl2先氧化Fe2+,再氧化Br-。
提示:把xmolFeBr2分开,为xmolFe2+和2xmolBr-,Cl2先氧化Fe2+,再氧化Br-。
您最近一年使用:0次
4 . 实验室有一瓶部分被氧化的硫酸亚铁,为测定其被氧化程度,取10.0g样品溶于水配成100mL溶液。取两份溶液各10.0mL,第一份加入14.0mL0.500mol•L-1BaCl2溶液恰好完全反应;第二份恰好与8.0mL0.100mol•L-1的酸性KMnO4溶液完全反应。
(1)100mL溶液中SO 的物质的量浓度是
的物质的量浓度是____ mol•L-1。
(2)该样品中硫酸亚铁的质量分数是____ 。
(1)100mL溶液中SO
 的物质的量浓度是
的物质的量浓度是(2)该样品中硫酸亚铁的质量分数是
您最近一年使用:0次
2021-06-25更新
|
825次组卷
|
3卷引用:浙江省杭州市余杭、临平、萧山2020-2021学年高一下学期期末学业水平测试化学试题
5 . 医学上经常用硫酸亚铁糖衣片给这种贫血病人补铁。现取20粒糖衣片,质量为10g,溶于40g水中,向所配溶液中滴加氢氧化钠溶液至略过量过滤、洗涤、干燥,然后进行灼烧到固体质量不再发生改变,质量为0.8g。试计算:
(1)该糖衣片中硫酸亚铁的质量分数______ 。
(2)1粒糖衣片中含铁元素的质量______ 。
(1)该糖衣片中硫酸亚铁的质量分数
(2)1粒糖衣片中含铁元素的质量
您最近一年使用:0次
解题方法
6 . 把2.0mol/L CuSO4溶液和2.0mol/L H2SO4溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和)。则:
(1)混合溶液中H+、Cu2+、 的物质的量浓度分别为:
的物质的量浓度分别为:____________ ;
(2)向溶液中加入铁粉,足够长的时间后,铁粉有剩余,过滤,此时滤液中的Fe2+的物质的量浓度为___________ ;
(3)取100mL该滤液,向其中加入适量硝酸,再加入足量氢氧化钠溶液,有红褐色沉淀生成。过滤,加热沉淀物至质量不再变化,得到红棕色的残渣。写出残渣的化学式______ ,并计算残渣的质量__________ (不计操作带来的损失)。
(1)混合溶液中H+、Cu2+、
 的物质的量浓度分别为:
的物质的量浓度分别为:(2)向溶液中加入铁粉,足够长的时间后,铁粉有剩余,过滤,此时滤液中的Fe2+的物质的量浓度为
(3)取100mL该滤液,向其中加入适量硝酸,再加入足量氢氧化钠溶液,有红褐色沉淀生成。过滤,加热沉淀物至质量不再变化,得到红棕色的残渣。写出残渣的化学式
您最近一年使用:0次
7 . 3.84gFe和Fe2O3的混合物溶于过量盐酸中,生成0.03molH2,向反应后的溶液中加入KSCN检验,溶液无明显现象.求原混合物中Fe2O3的质量.
您最近一年使用:0次
解题方法
8 . 铁是应用最广泛的金属,铁的卤化物、氧化物等均为重要化合物。
(1)要确定铁的某氯化物FeClx的化学式,可用实验的方法。实验中称取0.54 g的FeClx样品,溶解后加入足量硝酸银溶液,得沉淀1.435g。求出FeClx中x值 (列出计算过程);
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(C1)=1:2.1,则该样品中FeCl3的物质的量分数为__________。在实验室中,FeCl2可用铁粉和__________反应制备
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为____________;
(1)要确定铁的某氯化物FeClx的化学式,可用实验的方法。实验中称取0.54 g的FeClx样品,溶解后加入足量硝酸银溶液,得沉淀1.435g。求出FeClx中x值 (列出计算过程);
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(C1)=1:2.1,则该样品中FeCl3的物质的量分数为__________。在实验室中,FeCl2可用铁粉和__________反应制备
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为____________;
您最近一年使用:0次



