解题方法
1 . 填空
(1)Fe3+被铁粉还原成Fe2+的离子方程式:
(2)Fe2+被Cl2氧化成Fe3+的离子方程式:
您最近一年使用:0次
解题方法
2 . 下列关于铁及其化合物性质的叙述中不正确的是
| A.铁能被磁铁吸引,可用于制作磁性材料 |
| B.缺铁性贫血患者的补血剂中含有正三价铁元素 |
| C.三氧化二铁常用于制造红色油漆和涂料 |
| D.保存氯化亚铁溶液时,应加少量铁粉 |
您最近一年使用:0次
名校
解题方法
3 . 如图所示是铁及其化合物的“价类”二维图:

(1)X、Y分别代表_________ 、__________ ;(各1分)Z在空气中转化为W的化学方程式为__________ ,现象_________________________
(2)某小组研究 性质,预测
性质,预测 能与
能与___________ 发生氧化还原反应(填序号)
① 溶液 ②氯水 ③稀盐酸 ④酸性
溶液 ②氯水 ③稀盐酸 ④酸性 溶液 ⑤
溶液 ⑤ 溶液 ⑥碳酸钠
溶液 ⑥碳酸钠
(3)铁盐溶液可用于金属刻蚀,如何检验某溶液中存在
_________________________________ (写出两种检验手段);如用 溶液刻蚀铜制电路板,
溶液刻蚀铜制电路板, 被
被_________ (填“还原”或“氧化”)为 ,该反应的离子方程式为
,该反应的离子方程式为_____________________________ 。

(1)X、Y分别代表
(2)某小组研究
 性质,预测
性质,预测 能与
能与①
 溶液 ②氯水 ③稀盐酸 ④酸性
溶液 ②氯水 ③稀盐酸 ④酸性 溶液 ⑤
溶液 ⑤ 溶液 ⑥碳酸钠
溶液 ⑥碳酸钠(3)铁盐溶液可用于金属刻蚀,如何检验某溶液中存在

 溶液刻蚀铜制电路板,
溶液刻蚀铜制电路板, 被
被 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
名校
4 . 下列关于离子检验的说法正确的是
| A.检验溶液中是否含有Ba2+;取少量待测液,向其中加入少量稀硫酸,若有白色沉淀产生,则溶液中含有Ba2+ |
| B.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是酸性KMnO4溶液 |
C.检验溶液中是否含有CO :取少量待测液,向其中加入适量稀盐酸,观察是否有大量气泡产生 :取少量待测液,向其中加入适量稀盐酸,观察是否有大量气泡产生 |
| D.在未知溶液中滴加稀盐酸出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液有Ag+ |
您最近一年使用:0次
名校
解题方法
5 . 磷酸亚铁[ ]是生产锂电池的原料,能溶于强酸,不溶于水。实验室可以
]是生产锂电池的原料,能溶于强酸,不溶于水。实验室可以 、
、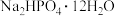 及
及 为原料制备磷酸亚铁,主要反应为
为原料制备磷酸亚铁,主要反应为
 。合成磷酸亚铁的装置如图。
。合成磷酸亚铁的装置如图。

回答下列问题:
(1)仪器A的名称为___________ 。
(2)实验中需要210 0.1
0.1
 溶液,配制该浓度的溶液需要的玻璃仪器除了烧杯、玻璃棒、量筒外,还有
溶液,配制该浓度的溶液需要的玻璃仪器除了烧杯、玻璃棒、量筒外,还有___________ ,需要称量的绿矾( )的质量为
)的质量为___________ g。
(3)实验中应使用煮沸并冷却的蒸馏水配制酸性 溶液,若蒸馏水未经煮沸直接配制,则可能发生反应的离子方程式为
溶液,若蒸馏水未经煮沸直接配制,则可能发生反应的离子方程式为___________ 。
(4)实验时,在仪器A中先加入抗坏血酸(维生素C)稀溶液作底液,然后向烧瓶中滴入 与
与 混合溶液至
混合溶液至 ,再滴入
,再滴入 溶液,最终维持
溶液,最终维持 。用抗坏血酸稀溶液作底液的作用是
。用抗坏血酸稀溶液作底液的作用是___________ 。
(5)生成的 沉淀需充分洗涤,检验洗涤是否完全的方法是
沉淀需充分洗涤,检验洗涤是否完全的方法是___________ 。
(6)某研究性学习小组的同学拟用工业品十二水合磷酸氢二钠(含 、重金属盐及有色杂质等)提纯得到
、重金属盐及有色杂质等)提纯得到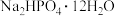 晶体。已知:
晶体。已知: 溶液的
溶液的 在8.2~8.4之间,重金属硫化物不溶于水。请补充实验步骤:将工业品溶于热水;
在8.2~8.4之间,重金属硫化物不溶于水。请补充实验步骤:将工业品溶于热水;___________ ,冷却结晶,过滤、洗涤及干燥。[实验中可选用的试剂: 溶液、0.1
溶液、0.1
 溶液、0.1
溶液、0.1
 溶液、活性炭]
溶液、活性炭]
 ]是生产锂电池的原料,能溶于强酸,不溶于水。实验室可以
]是生产锂电池的原料,能溶于强酸,不溶于水。实验室可以 、
、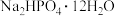 及
及 为原料制备磷酸亚铁,主要反应为
为原料制备磷酸亚铁,主要反应为
 。合成磷酸亚铁的装置如图。
。合成磷酸亚铁的装置如图。
回答下列问题:
(1)仪器A的名称为
(2)实验中需要210
 0.1
0.1
 溶液,配制该浓度的溶液需要的玻璃仪器除了烧杯、玻璃棒、量筒外,还有
溶液,配制该浓度的溶液需要的玻璃仪器除了烧杯、玻璃棒、量筒外,还有 )的质量为
)的质量为(3)实验中应使用煮沸并冷却的蒸馏水配制酸性
 溶液,若蒸馏水未经煮沸直接配制,则可能发生反应的离子方程式为
溶液,若蒸馏水未经煮沸直接配制,则可能发生反应的离子方程式为(4)实验时,在仪器A中先加入抗坏血酸(维生素C)稀溶液作底液,然后向烧瓶中滴入
 与
与 混合溶液至
混合溶液至 ,再滴入
,再滴入 溶液,最终维持
溶液,最终维持 。用抗坏血酸稀溶液作底液的作用是
。用抗坏血酸稀溶液作底液的作用是(5)生成的
 沉淀需充分洗涤,检验洗涤是否完全的方法是
沉淀需充分洗涤,检验洗涤是否完全的方法是(6)某研究性学习小组的同学拟用工业品十二水合磷酸氢二钠(含
 、重金属盐及有色杂质等)提纯得到
、重金属盐及有色杂质等)提纯得到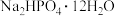 晶体。已知:
晶体。已知: 溶液的
溶液的 在8.2~8.4之间,重金属硫化物不溶于水。请补充实验步骤:将工业品溶于热水;
在8.2~8.4之间,重金属硫化物不溶于水。请补充实验步骤:将工业品溶于热水; 溶液、0.1
溶液、0.1
 溶液、0.1
溶液、0.1
 溶液、活性炭]
溶液、活性炭]
您最近一年使用:0次
2023-10-22更新
|
321次组卷
|
3卷引用:新疆生产建设兵团第二中学(新疆兵团地州学校)2023-2024学年高三上学期期中联考化学试题
名校
6 . 下列实验操作与实验现象及结论对应且正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向某溶液逐滴加入NaOH溶液 | 先有白色胶状沉淀产生,后来沉淀逐渐消失 | 溶液中可能含有 |
| B | 向某溶液中滴加氯水,然后再滴加KSCN溶液 | 溶液显红色 | 溶液中含有 |
| C | SO2分别通入酸性KMnO4和品红溶液 | 溶液均褪色 | SO2均表现漂白性 |
| D | 向Fe(NO3)2溶液中滴入2滴浓H2SO4 | 溶液变为黄色 | 氧化性:浓H2SO4>Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 下列离子方程式书写正确的是
A.向碳酸氢铵溶液中加入过量的 溶液: 溶液: |
B.过量铁粉加入稀硝酸中: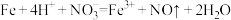 |
C.用过量氨水吸收工业尾气中的 : : |
D.氢氧化亚铁溶于过量稀硝酸: |
您最近一年使用:0次
解题方法
8 . 铁元素是人体内一种微量元素,主要以Fe2+的形式存在。请回答下列问题:
(1)下列微粒中,既有氧化性又有还原性的是______ (填字母)。
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中______ 是还原剂
(3)某种麦片中含有微量的细小铁粉,食用该麦片后,铁粉与胃酸反应的离子方程式是___________ 。
(4)含硫酸亚铁的药片可治疗缺铁性贫血,其表面有糖衣,糖衣的作用是___________ 。可用___________ 溶液检验该硫酸亚铁药片是否变质。
(1)下列微粒中,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中
(3)某种麦片中含有微量的细小铁粉,食用该麦片后,铁粉与胃酸反应的离子方程式是
(4)含硫酸亚铁的药片可治疗缺铁性贫血,其表面有糖衣,糖衣的作用是
您最近一年使用:0次
名校
解题方法
9 . 下列各组离子在指定溶液中能大量共存的是
①无色溶液中:K+、Na+、Cu2+、OH-
②pH=11的溶液中: 、Na+、[Al(OH)4]-、
、Na+、[Al(OH)4]-、
③加入Al能放出H2的溶液中:Cl-、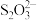 、
、 、
、
④由水电离出的c(OH-)=10-13 mol·L-1的溶液中:Na+、Ba2+、Cl-、Br-
⑤有较多Fe3+的溶液中:Na+、 、SCN-、
、SCN-、
⑥酸性溶液中:Fe2+、Al3+、NO 、I-、Cl-
、I-、Cl-
①无色溶液中:K+、Na+、Cu2+、OH-
②pH=11的溶液中:
 、Na+、[Al(OH)4]-、
、Na+、[Al(OH)4]-、
③加入Al能放出H2的溶液中:Cl-、
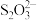 、
、 、
、
④由水电离出的c(OH-)=10-13 mol·L-1的溶液中:Na+、Ba2+、Cl-、Br-
⑤有较多Fe3+的溶液中:Na+、
 、SCN-、
、SCN-、
⑥酸性溶液中:Fe2+、Al3+、NO
 、I-、Cl-
、I-、Cl-| A.①② | B.③⑥ | C.②④ | D.③⑤ |
您最近一年使用:0次
2023-08-26更新
|
1315次组卷
|
3卷引用:新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题
解题方法
10 . 化合价和物质类别是整理元素及化合物知识的两个要素,可表示为“价—类”二维图。铁元素的“价—类”二维图如图所示,下列说法正确的是

| A.工业上用CO还原Fe2O3炼铁,该反应为置换反应 |
| B.Fe3O4中铁元素为+4价 |
| C.要除去FeCl2溶液中少量的FeCl3,可加入适量铁粉并过滤 |
| D.Fe(OH)2浊液露置于空气中,由白色立即变为红褐色 |
您最近一年使用:0次



