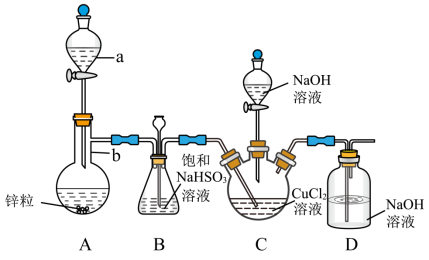
1 . CuCl是一种难溶于水和乙醇的白色固体,可溶于浓盐酸或者浓氨水(形成络合物),易被氧化为高价绿色铜盐,见光受热易分解。在催化领域广泛应用,纺织工业中常作脱色剂,可利用如图装置(夹持装置略去)将SO2通入新制氢氧化铜悬浊液中制备CuCl。
①向C中先加入10.00mL0.5mol•L-1CuCl2溶液,再加入30mL0.6mol•L-1NaOH溶液;
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO2气体至过量,直至C中出现较多的白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO3)2。
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二者为竞争关系。检验淡绿色溶液中含有 的操作方法是
的操作方法是_______ 。
①向C中先加入10.00mL0.5mol•L-1CuCl2溶液,再加入30mL0.6mol•L-1NaOH溶液;
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO2气体至过量,直至C中出现较多的白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO3)2。
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二者为竞争关系。检验淡绿色溶液中含有
 的操作方法是
的操作方法是
您最近一年使用:0次
2 . I.利用下图装置制备 ,并研究
,并研究 的性质。
的性质。
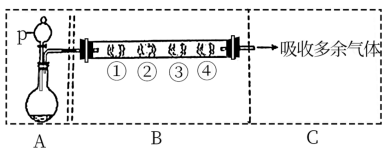
(1)A装置利用亚硫酸钠和硫酸反应制备 ,写出化学方程式
,写出化学方程式_______ 。
(2)填写下表
(3) 和氯气按照体积比
和氯气按照体积比 通入水中,溶液的漂白性
通入水中,溶液的漂白性_______ (填“增强”“减弱”“不变”)原因是_______ (用化学方程式表示)。
II.“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
,得到亚硫酸钠(Na2SO3)粗品。其流程如下:

(4)上述流程中,加入 后,发生反应的化学方程式为
后,发生反应的化学方程式为_______ 。
(5)亚硫酸钠粗品中含有少量 ,原因是
,原因是_______ 。
 ,并研究
,并研究 的性质。
的性质。
(1)A装置利用亚硫酸钠和硫酸反应制备
 ,写出化学方程式
,写出化学方程式(2)填写下表
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | 褪色 | 浅黄色 | ||
体现 的性质 的性质 |
(3)
 和氯气按照体积比
和氯气按照体积比 通入水中,溶液的漂白性
通入水中,溶液的漂白性II.“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为
 )吸收烟气中的
)吸收烟气中的 ,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
(4)上述流程中,加入
 后,发生反应的化学方程式为
后,发生反应的化学方程式为(5)亚硫酸钠粗品中含有少量
 ,原因是
,原因是
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
3 . 纯ClO2遇热易发生分解,工业上通常制成NaClO2固体以便运输和储存。制备NaClO2的实验装置如图所示(夹持装置省略),其中A装置制备ClO2,C装置用于制备NaClO2。回答下列问题:_______ 。
(2)装置A中发生反应的离子方程式为_______ 。向装置A中通入空气的目的是_______ 。
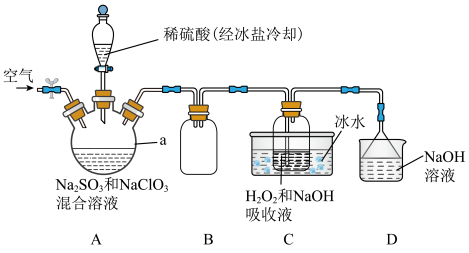
(2)装置A中发生反应的离子方程式为
您最近一年使用:0次
4 . 某化学学习小组利用 溶液氧化环己醇(
溶液氧化环己醇( 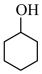 )制备环己酮(
)制备环己酮( 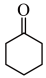 )的装置如图所示。
)的装置如图所示。
操作步骤如下:
ⅰ.向三颈烧瓶内加入环己醇、冰醋酸,逐滴加入NaClO溶液, 条件下反应30分钟后冷却。
条件下反应30分钟后冷却。
ⅱ.向三颈烧瓶内加入适量饱和NaHSO3溶液,用NaOH调节溶液显中性后加入饱和氯化钠溶液,然后经分液、干燥、蒸馏得到环己酮。
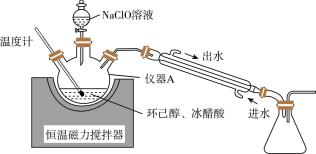
下列叙述错误的是
 溶液氧化环己醇(
溶液氧化环己醇(  )制备环己酮(
)制备环己酮(  )的装置如图所示。
)的装置如图所示。操作步骤如下:
ⅰ.向三颈烧瓶内加入环己醇、冰醋酸,逐滴加入NaClO溶液,
 条件下反应30分钟后冷却。
条件下反应30分钟后冷却。ⅱ.向三颈烧瓶内加入适量饱和NaHSO3溶液,用NaOH调节溶液显中性后加入饱和氯化钠溶液,然后经分液、干燥、蒸馏得到环己酮。

下列叙述错误的是
A.冰醋酸既作为溶剂,同时可增强 溶液的还原性 溶液的还原性 |
B.若 溶液滴加过快,三颈烧瓶中会产生少量黄绿色气体 溶液滴加过快,三颈烧瓶中会产生少量黄绿色气体 |
C.饱和亚硫酸氢钠的主要作用是除去 |
| D.饱和氯化钠可促进有机相和无机相分层 |
您最近一年使用:0次
名校
5 . 某实验小组将SO2通入Na2S和Na2SO3的混合溶液中制备硫代硫酸钠(Na2S2O3),其装置如图所示(省略夹持装置),下列说法错误的是( )
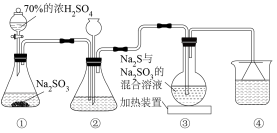

| A.装置②的作用之一是观察SO2的生成速率,其中的液体可以是饱和NaHSO3溶液 |
B.为提高产品纯度,使烧瓶中Na2S和Na2SO3恰好完全反应,则 |
| C.装置④的作用是吸收尾气,防止污染环境,同时防倒吸 |
| D.装置①也可用于高锰酸钾与浓盐酸反应制备氯气 |
您最近一年使用:0次
2020-10-09更新
|
266次组卷
|
7卷引用:【全国市级联考】山东省临沂市2018届高三第三次高考模拟考试理科综合化学试题2
21-22高一下·安徽·阶段练习
6 . 探究亚硫酸(溶液中存在大量 分子)的性质,进行如下实验。
分子)的性质,进行如下实验。
由上述实验所得亚硫酸性质及对应的解释错误的是
 分子)的性质,进行如下实验。
分子)的性质,进行如下实验。| 实验 | 装置 | 试剂a | 现象 |
| ① |  | 氯水 | 氯水褪色 |
| ② |  溶液(含酚酥) 溶液(含酚酥) | 溶液褪色,产生白色沉淀 | |
| ③ |  、 、 溶液 溶液 | 产生白色沉淀 | |
| ④ |  溶液 溶液 | 溶液出现乳白色浑浊 |
A.H2SO3溶液使氯水褪色: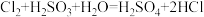 |
B.H2SO3有酸性: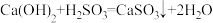 |
C.H2SO3有还原性: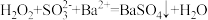 |
D.H2SO3有氧化性: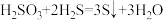 |
您最近一年使用:0次
2022-05-15更新
|
159次组卷
|
3卷引用:第15练 实验综合题与无机综合题-2022年【暑假分层作业】高一化学(人教版2019必修第二册)
(已下线)第15练 实验综合题与无机综合题-2022年【暑假分层作业】高一化学(人教版2019必修第二册)安徽省示范高中培优联盟2021-2022学年高一下学期春季联赛考试化学试题云南省楚雄天人中学2021-2022学年高二6月月考化学(A)试题



