9. 锌锰干电池的负极是作为电池壳体的金属锌,正极是被二氧化锰和碳粉包围的石墨电极,电解质是氯化锌和氯化铵的糊状物,该电池放电过程中产生MnOOH。废旧电池中的Zn、Mn元素的回收,对环境保护有重要的意义。
Ⅰ.回收锌元素,制备ZnCl
2步骤一:向除去壳体及石墨电极的黑色糊状物中加水,搅拌,充分溶解,经过滤分离得固体和滤液。
步骤二:处理滤液,得到ZnCl
2·xH
2O晶体。
步骤三:将SOCl
2与ZnCl
2·xH
2O晶体混合制取无水ZnCl
2。
制取无水ZnCl
2,回收剩余的SOCl
2并验证生成物中含有SO
2(夹持及加热装置略)的装置如图:
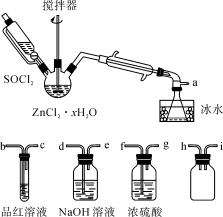
(已知:SOCl
2是一种常用的脱水剂,熔点-105℃,沸点79℃,140℃以上时易分解,与水剧烈反应生成两种气体。)
(1)写出SOCl
2与水反应的化学方程式:
__。
(2)接口的连接顺序为a→
__→
__→h→i→
__→
__→
__→e。
Ⅱ.回收锰元素,制备MnO
2(3)洗涤步骤一得到的固体,判断固体洗涤干净的方法:
__。
(4)洗涤后的固体经初步蒸干后进行灼烧,灼烧的目的:
__。
Ⅲ.二氧化锰纯度的测定
称取1.40g灼烧后的产品,加入2.68g草酸钠(Na
2C
2O
4)固体,再加入足量的稀硫酸并加热(杂质不参与反应),充分反应后冷却,将所得溶液转移到100mL容量瓶中用蒸馏水稀释至刻线,从中取出20.00mL,用0.0200mol/L高锰酸钾溶液进行滴定,滴定三次,消耗高锰酸钾溶液体积的平均值为17.30mL。
(5)写出MnO
2溶解反应的离子方程式
__。
(6)产品的纯度为
__。
(7)若灼烧不充分,滴定时消耗高锰酸钾溶液体积
__(填“偏大”“偏小”“不变”)。