1 . “价—类”二维图是研究物质性质的一种方法,图中a~f表示的均是含硫物质。下列说法正确的是

| A.a可用硫化亚铁与稀硝酸反应制取 |
B.可发生反应: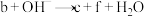 (未配平) (未配平) |
| C.c能使溴水褪色,证明c有漂白性 |
| D.f既有氧化性又有还原性 |
您最近半年使用:0次
2024-02-14更新
|
614次组卷
|
8卷引用:重庆市璧山来凤中学校2023-2024学年高一下学期3月月考化学试题
重庆市璧山来凤中学校2023-2024学年高一下学期3月月考化学试题河北省承德市2023-2024学年高一上学期期末考试化学试题(已下线)专题01 硫及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)河北省石家庄市第二十三中学2023-2024学年高一下学期第一次月考(3月)化学试题安徽省淮南市第二中2023-2024学年高一下学期第一次月考化学试题河南省新乡市原阳县实验高级中学2023-2024学年高一下学期3月月考化学试题河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题江苏省南宁市第三十三中学2023-2024学年高一下学期3月月考化学试题
解题方法
2 . 下列离子方程式的书写正确的是
A.向Na2SO3溶液中加入稀HNO3: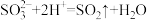 |
B.向水垢中滴加足量醋酸: |
C.用Na2SO3溶液吸收少量Cl2: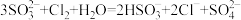 |
D.少量Fe与足量稀HNO3: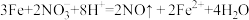 |
您最近半年使用:0次
名校
解题方法
3 . 下列离子能大量共存的是
A.使无色酚酞试液呈红色的溶液中:Na+、K+、 、 、 |
B.无色透明的溶液中:Cu2+、K+、 、 、 |
C.含有大量Ba(NO3)2的溶液中:Mg2+、 、 、 、Cl- 、Cl- |
D.使紫色石蕊试液呈红色的溶液中:Na+、K+、 、 、 |
您最近半年使用:0次
2023-05-09更新
|
300次组卷
|
3卷引用:重庆市黔江中学校2023-2024学年高一上学期11月月考化学试题
4 . 有一瓶 溶液,它可能部分被氧化。某同学取少量该溶液,滴加
溶液,它可能部分被氧化。某同学取少量该溶液,滴加 溶液,产生白色沉淀,再加入足量稀硫酸,充分振荡后仍然有白色沉淀,下列叙述正确的是
溶液,产生白色沉淀,再加入足量稀硫酸,充分振荡后仍然有白色沉淀,下列叙述正确的是
 溶液,它可能部分被氧化。某同学取少量该溶液,滴加
溶液,它可能部分被氧化。某同学取少量该溶液,滴加 溶液,产生白色沉淀,再加入足量稀硫酸,充分振荡后仍然有白色沉淀,下列叙述正确的是
溶液,产生白色沉淀,再加入足量稀硫酸,充分振荡后仍然有白色沉淀,下列叙述正确的是| A.亚硫酸钠已部分被空气中的氧气氧化 |
B.加入 溶液后,产生的沉淀中一定含有硫酸钡 溶液后,产生的沉淀中一定含有硫酸钡 |
| C.加入稀硫酸后,不溶的沉淀一定是硫酸钡和亚硫酸钡 |
D.将稀硫酸换成稀盐酸后观察沉淀变化量可以确定 溶液是否部分被氧化 溶液是否部分被氧化 |
您最近半年使用:0次
解题方法
5 . 下列物质能使高锰酸钾溶液褪色,且褪色原理相同的是
①活性炭 ② 溶液 ③
溶液 ③ ④稀硫酸 ⑤
④稀硫酸 ⑤ 溶液
溶液
①活性炭 ②
 溶液 ③
溶液 ③ ④稀硫酸 ⑤
④稀硫酸 ⑤ 溶液
溶液| A.②③⑤ | B.②③④ | C.①②④ | D.①③⑤ |
您最近半年使用:0次
名校
解题方法
6 . 对于下列实验,能正确描述的离子方程式是
A.用Na2SO3溶液吸收少量Cl2: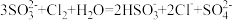 |
| B.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+ |
| C.向氯化钡溶液中通入CO2:CO2+H2O+Ba2+=BaCO3↓+2H+ |
D.同浓度同体积NH4HSO4溶液与NaOH溶液混合: |
您最近半年使用:0次
7 . 下图的实验装置可用于研究SO2转化为SO3的转化率。
已知:SO3的熔点是16.8℃,沸点是44.8℃。

完成下列填空:
(1)A装置中发生的化学反应方程式为_______ 。
(2)根据实验需要,应该在D、E处连接合适的装置。请从下图中选择,将所选装置的序号填入相应的空格,D:_______ ,E:_______ 。
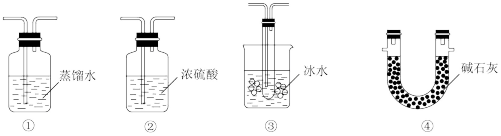
装置F的作用为_______ 。
(3)用a mol Na2SO3粉末与足量浓硫酸进行此实验,当A处反应结束时,再继续通入一段时间O2,最后测得E处装置增重b g,则此时SO2的转化率为_______ (用含a、b的代数式表示)。
(4)现欲检验Na2SO3样品在空气中是否变质,其方法是_______ 。(简述实验操作及现象)
(5)实验结束后,不慎将收集了SO3的装置露置于空气中,可观察到装置出口处产生大量白雾,简述其原因_______ 。
已知:SO3的熔点是16.8℃,沸点是44.8℃。

完成下列填空:
(1)A装置中发生的化学反应方程式为
(2)根据实验需要,应该在D、E处连接合适的装置。请从下图中选择,将所选装置的序号填入相应的空格,D:

装置F的作用为
(3)用a mol Na2SO3粉末与足量浓硫酸进行此实验,当A处反应结束时,再继续通入一段时间O2,最后测得E处装置增重b g,则此时SO2的转化率为
(4)现欲检验Na2SO3样品在空气中是否变质,其方法是
(5)实验结束后,不慎将收集了SO3的装置露置于空气中,可观察到装置出口处产生大量白雾,简述其原因
您最近半年使用:0次
名校
解题方法
8 . 下列实验与结论相匹配的是
| 实验 | 结论 | |
| A. | 用FeCl3溶液刻蚀铜电路板 | 还原性:Fe>Cu |
| B. | 向某溶液中加入淀粉KI溶液,溶液呈蓝色 | 溶液中一定含Fe3+ |
| C. | 将彩色鲜花放入干燥氯气中,发现彩色鲜花褪色 | 氯气具有漂白性 |
| D. | 向久置的Na2SO3溶液中加入足量BaCl2溶液,出现白色沉淀;再加入稀盐酸,沉淀部分溶解 | Na2SO3部分被氧化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
9 . 甲、乙两组同学用不同的方法制备SO2并探究其性质。(夹持装置已略去)
Ⅰ.甲组同学设计的实验装置如图所示,回答下列问题:
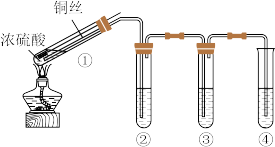
(1)试管①中反应的化学方程式为_______ 。
(2)试管②中的品红溶液褪色。欲证明品红褪色的原因是SO2,需要补充的实验操作及应出现的实验现象是_______ 。
(3)试管③中的溴水褪色,体现SO2具有_______ 性(填“还原”、“氧化”或“漂白”)。
(4)试管④中的试剂是NaOH溶液,反应的离子方程式为_______ 。
Ⅱ.乙组同学设计的实验装置如下图所示,回答下列问题:
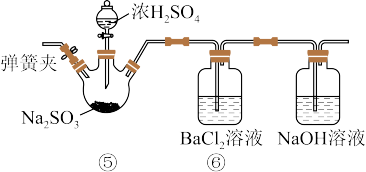
已知:BaSO3是白色难溶于水的物质,但可溶于盐酸。
(5)⑤中反应的化学方程式为_______ 。
(6)⑥中产生了不溶于盐酸的白色沉淀,该沉淀是_______ 。
(7)请你推测⑥中出现白色沉淀的原因可能是_______ 。
Ⅰ.甲组同学设计的实验装置如图所示,回答下列问题:

(1)试管①中反应的化学方程式为
(2)试管②中的品红溶液褪色。欲证明品红褪色的原因是SO2,需要补充的实验操作及应出现的实验现象是
(3)试管③中的溴水褪色,体现SO2具有
(4)试管④中的试剂是NaOH溶液,反应的离子方程式为
Ⅱ.乙组同学设计的实验装置如下图所示,回答下列问题:

已知:BaSO3是白色难溶于水的物质,但可溶于盐酸。
(5)⑤中反应的化学方程式为
(6)⑥中产生了不溶于盐酸的白色沉淀,该沉淀是
(7)请你推测⑥中出现白色沉淀的原因可能是
您最近半年使用:0次
名校
解题方法
10 . 某溶液中可能含有浓度均为0.5mol/L的K+、Na+、Fe2+、Fe3+、SO 、SO
、SO 中的几种离子。根据下列实验操作与现象,推测合理的是
中的几种离子。根据下列实验操作与现象,推测合理的是
 、SO
、SO 中的几种离子。根据下列实验操作与现象,推测合理的是
中的几种离子。根据下列实验操作与现象,推测合理的是| 实验步骤 | 实验现象 | |
| Ⅰ | 向该溶液中加酸性高锰酸钾溶液 | 紫色褪去 |
| Ⅱ | 向该溶液中加氯化钡溶液 | 产生难溶于水的沉淀 |
A.若溶液中有SO ,则有Fe2+ ,则有Fe2+ | B.溶液中可能有Fe3+ |
C.若溶液中有SO ,则一定有Fe3+ ,则一定有Fe3+ | D.SO 、SO 、SO 可能同时存在于溶液中 可能同时存在于溶液中 |
您最近半年使用:0次



