解题方法
1 . 下列实验目的、方案设计和现象、结论都正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 为验证某固体是 还是 还是 ,室温下取少量固体于试管中,插入温度计,加几滴水。 ,室温下取少量固体于试管中,插入温度计,加几滴水。 | 温度降低 | 该固体是 |
| B | 常温下,用pH计分别测定等体积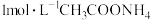 溶液和 溶液和 溶液的pH 溶液的pH | pH均为7 | 同温下,不同浓度的 溶液中水的电离程度相同 溶液中水的电离程度相同 |
| C | 向盛有少量蒸馏水的试管里滴加2滴 溶液,然后再滴加2滴硫氰化钾溶液 溶液,然后再滴加2滴硫氰化钾溶液 | 无明显现象 |  与 与 的配位能力强于 的配位能力强于 |
| D | 在某待检溶液中,滴加NaOH溶液,加热,用湿润的红色石蕊试纸检验产生的气体 | 试纸变蓝色 | 该待检溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 乙酰苯胺是一种无色有闪光的小叶状固体或白色晶性粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂。乙酰苯胺的一种制备原理为:
实验步骤:
【步骤1】如图所示,在圆底烧瓶中加入无水苯胺 、冰醋酸
、冰醋酸 、锌粉
、锌粉 ,安装仪器,加入沸石,调节加热温度,使温度计温度控制在
,安装仪器,加入沸石,调节加热温度,使温度计温度控制在 左右,反应约
左右,反应约 ,当反应基本完成时,停止加热。
,当反应基本完成时,停止加热。 水,搅拌加热至沸腾,使粗品完全溶解。
水,搅拌加热至沸腾,使粗品完全溶解。
【步骤3】稍冷后,加入 活性炭,并煮沸
活性炭,并煮沸 ,趁热抽滤除去活性炭。
,趁热抽滤除去活性炭。
【步骤4】将滤液倒入烧杯中,自然冷却,析出晶体。抽滤、洗涤、干燥得产品,称其质量。
回答下列问题:
(1)仪器a的名称_____ 。
(2)【步骤1】加热可用_____ (填“水浴”或“油浴”)。
(3)制备过程中加入锌粉的作用为_____ 。
(4)从化学平衡的角度分析,使用刺形分馏柱并控制分馏柱上端的温度在 左右的原因:
左右的原因:_____ 。
(5)乙酰苯胺粗品因含杂质而显色,【步骤3】中加入活性炭吸附有色杂质,加入活性炭需要待沸腾的溶液稍冷却后再加入,其目的是_____ 。
(6)该实验最终得到纯品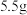 ,则乙酰苯胺的产率为
,则乙酰苯胺的产率为_____ (保留一位小数)。
(7)乙酰苯胺可以在 热溶液中发生水解,写出其反应方程式:
热溶液中发生水解,写出其反应方程式:_____ 。
(8)当制备少量乙酰苯胺时,常用图所示的微型仪器组装成实验装置制备。当观察到_____ 现象时,反应基本结束。
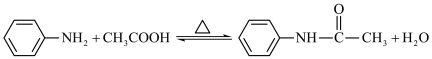
| 名称 | 相对分子质量 | 性状 | 密度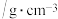 | 沸点/℃ | 溶解度 | 备注 |
| 苯胺 | 93 | 无色油状液体 | 1.02 | 184.4 | 微溶于水,易溶于乙醇、乙醚 | 易被氧化 |
| 乙酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水,易溶于乙醇、乙醚 | |
| 乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水,溶于热水,易溶于乙醇、乙醚 |
【步骤1】如图所示,在圆底烧瓶中加入无水苯胺
 、冰醋酸
、冰醋酸 、锌粉
、锌粉 ,安装仪器,加入沸石,调节加热温度,使温度计温度控制在
,安装仪器,加入沸石,调节加热温度,使温度计温度控制在 左右,反应约
左右,反应约 ,当反应基本完成时,停止加热。
,当反应基本完成时,停止加热。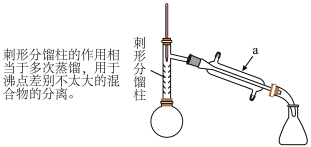
 水,搅拌加热至沸腾,使粗品完全溶解。
水,搅拌加热至沸腾,使粗品完全溶解。【步骤3】稍冷后,加入
 活性炭,并煮沸
活性炭,并煮沸 ,趁热抽滤除去活性炭。
,趁热抽滤除去活性炭。【步骤4】将滤液倒入烧杯中,自然冷却,析出晶体。抽滤、洗涤、干燥得产品,称其质量。
回答下列问题:
(1)仪器a的名称
(2)【步骤1】加热可用
(3)制备过程中加入锌粉的作用为
(4)从化学平衡的角度分析,使用刺形分馏柱并控制分馏柱上端的温度在
 左右的原因:
左右的原因:(5)乙酰苯胺粗品因含杂质而显色,【步骤3】中加入活性炭吸附有色杂质,加入活性炭需要待沸腾的溶液稍冷却后再加入,其目的是
(6)该实验最终得到纯品
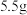 ,则乙酰苯胺的产率为
,则乙酰苯胺的产率为(7)乙酰苯胺可以在
 热溶液中发生水解,写出其反应方程式:
热溶液中发生水解,写出其反应方程式:(8)当制备少量乙酰苯胺时,常用图所示的微型仪器组装成实验装置制备。当观察到

您最近一年使用:0次
名校
解题方法
3 . 乙酰苯胺是生产磺胺类药物的重要中间体。实验室制取乙酰苯胺的一种方法如下:
 +CH3COOH
+CH3COOH
 +H2O
+H2O
乙酸、苯胺、乙酰苯胺的部分物理性质如下表
实验过程:①在50mL蒸馏瓶中加入沸石、乙酸7.4mL(过量),苯胺5mL,实验装置如下图所示(加热装置略去),先小火加热10分钟,再控制分馏柱温度为105℃,加热至反应完成。
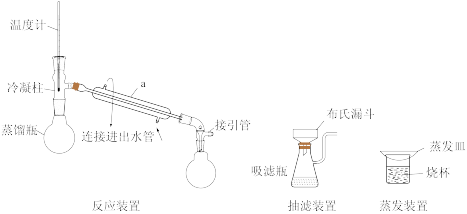
②趁热将反应后的混合物倒入装有100mL冷水的烧杯中,快速搅拌,用布氏漏斗抽滤。
③洗涤沉淀、再抽滤得固体,检验乙酰苯胺中的乙酸是否被除尽。
④将沉淀转移到表面皿上,加热蒸发,除去水。
回答下列问题:
(1)a仪器的名称是____ 。
(2)本实验为了提高苯胺的转化率,采取的措施是____ (填字母标号)。
A.用冷凝柱回流 B.加入过量的乙酸 C.分离出水 D.加入沸石
(3)控制分馏柱温度为105℃的目的是____ 。
(4)持续控制分馏柱温度为105℃,直至____ (填现象)说明反应结束。
(5)抽滤时,多次用冷水润洗沉淀、可以除去乙酰苯胺中的乙酸。检验乙酸是否除尽的方法是___ 。
(6)蒸发装置烧杯中加入的液体为_____ 。
(7)某同学实验的产率为75.3%,导致产量不高的因素可能是___ (填字母标号)。
A.没有等生成的水分馏完就停止反应 B.在抽滤时,有产物残留在烧杯壁
C.乙酰苯胺中的乙酸未除干净 D.抽滤时乙酰苯胺有部分溶于水中
 +CH3COOH
+CH3COOH
 +H2O
+H2O乙酸、苯胺、乙酰苯胺的部分物理性质如下表
| 乙酸 | 苯胺 | 乙酰苯胺 | |
| 沸点 | 118 | 184 | 304 |
| 状态 | 无色液体 | 无色液体 | 白色固体 |
| 在水中的溶解度 | 易溶于水 | 易溶于水20℃溶解度3.6g | 20℃溶解度0.46g;80℃溶解度3.5g;100C溶解度18g |

②趁热将反应后的混合物倒入装有100mL冷水的烧杯中,快速搅拌,用布氏漏斗抽滤。
③洗涤沉淀、再抽滤得固体,检验乙酰苯胺中的乙酸是否被除尽。
④将沉淀转移到表面皿上,加热蒸发,除去水。
回答下列问题:
(1)a仪器的名称是
(2)本实验为了提高苯胺的转化率,采取的措施是
A.用冷凝柱回流 B.加入过量的乙酸 C.分离出水 D.加入沸石
(3)控制分馏柱温度为105℃的目的是
(4)持续控制分馏柱温度为105℃,直至
(5)抽滤时,多次用冷水润洗沉淀、可以除去乙酰苯胺中的乙酸。检验乙酸是否除尽的方法是
(6)蒸发装置烧杯中加入的液体为
(7)某同学实验的产率为75.3%,导致产量不高的因素可能是
A.没有等生成的水分馏完就停止反应 B.在抽滤时,有产物残留在烧杯壁
C.乙酰苯胺中的乙酸未除干净 D.抽滤时乙酰苯胺有部分溶于水中
您最近一年使用:0次
2021-03-18更新
|
807次组卷
|
4卷引用:广西壮族自治区南宁市2021届高三下学期第一次适应性测试理科综合化学试题
广西壮族自治区南宁市2021届高三下学期第一次适应性测试理科综合化学试题(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点34 物质的制备与合成-备战2022年高考化学一轮复习考点帮(浙江专用)辽宁省沈阳市回民中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
4 . 实验室利用苯甲腈( ,
, )和三氟乙醇(
)和三氟乙醇( ,
, )制备苯甲亚胺三氟乙酯的装置(加热及夹持装置略)如图所示。
)制备苯甲亚胺三氟乙酯的装置(加热及夹持装置略)如图所示。
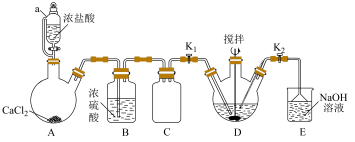
已知:Ⅰ.制备原理: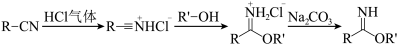 (R、R'=烃基);
(R、R'=烃基);
Ⅱ.苯甲腈、三氟乙醇、苯甲亚胺三氟乙酯均为液体,苯甲亚胺三氟乙酯受热易分解。
回答下列问题:
(1)组装好装置并检查装置气密性,再向A中加入足量无水 ,D中加入20.6g苯甲腈和21.6g三氟乙醇并用冰浴降温至0℃,仪器a的名称为
,D中加入20.6g苯甲腈和21.6g三氟乙醇并用冰浴降温至0℃,仪器a的名称为___________ ,装置C的作用是___________ 。
(2)向D中持续通入 一段时间后关闭
一段时间后关闭 、
、 ,继续搅拌反应液使充分反应,冷却至0℃,抽滤得白色固体,用乙腈洗涤2~3次,白色固体主要成分的结构简式为
,继续搅拌反应液使充分反应,冷却至0℃,抽滤得白色固体,用乙腈洗涤2~3次,白色固体主要成分的结构简式为___________ ,洗涤的方法是___________ 。
(3)将洗涤后的白色固体加入饱和 溶液中,低温下反应,有机溶剂萃取3次,合并有机相,向有机相中加入无水
溶液中,低温下反应,有机溶剂萃取3次,合并有机相,向有机相中加入无水 ,过滤,与溶剂分离后得产品20.3g。
,过滤,与溶剂分离后得产品20.3g。
①萃取时可选用的有机溶剂是___________ (填标号)。
a.甲醇 b.乙酸 c.乙酸乙酯 d.丙酮
②无水 的作用是
的作用是___________ ,产品与溶剂分离的操作的名称是___________ ,本实验的产率为___________ 。
 ,
, )和三氟乙醇(
)和三氟乙醇( ,
, )制备苯甲亚胺三氟乙酯的装置(加热及夹持装置略)如图所示。
)制备苯甲亚胺三氟乙酯的装置(加热及夹持装置略)如图所示。
已知:Ⅰ.制备原理:
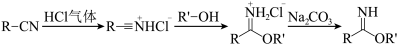 (R、R'=烃基);
(R、R'=烃基);Ⅱ.苯甲腈、三氟乙醇、苯甲亚胺三氟乙酯均为液体,苯甲亚胺三氟乙酯受热易分解。
回答下列问题:
(1)组装好装置并检查装置气密性,再向A中加入足量无水
 ,D中加入20.6g苯甲腈和21.6g三氟乙醇并用冰浴降温至0℃,仪器a的名称为
,D中加入20.6g苯甲腈和21.6g三氟乙醇并用冰浴降温至0℃,仪器a的名称为(2)向D中持续通入
 一段时间后关闭
一段时间后关闭 、
、 ,继续搅拌反应液使充分反应,冷却至0℃,抽滤得白色固体,用乙腈洗涤2~3次,白色固体主要成分的结构简式为
,继续搅拌反应液使充分反应,冷却至0℃,抽滤得白色固体,用乙腈洗涤2~3次,白色固体主要成分的结构简式为(3)将洗涤后的白色固体加入饱和
 溶液中,低温下反应,有机溶剂萃取3次,合并有机相,向有机相中加入无水
溶液中,低温下反应,有机溶剂萃取3次,合并有机相,向有机相中加入无水 ,过滤,与溶剂分离后得产品20.3g。
,过滤,与溶剂分离后得产品20.3g。①萃取时可选用的有机溶剂是
a.甲醇 b.乙酸 c.乙酸乙酯 d.丙酮
②无水
 的作用是
的作用是
您最近一年使用:0次
名校
解题方法
5 . 对硝基乙酰苯胺常用作合成药物和染料的中间体,用乙酰苯胺制备对硝基乙酰苯胺的反应为:
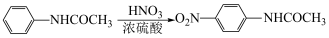
实验参数:
副反应:

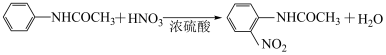
乙酰苯胺与混酸在5℃下反应主要产物是对硝基乙酰苯胺,在40℃下反应则生成约25%的邻硝基乙酰苯胺。
步骤1.在三颈烧瓶内放入新制备的乙酰苯胺4.5g和4.5 冰醋酸。在冷水浴冷却下搅拌,慢慢加入9
冰醋酸。在冷水浴冷却下搅拌,慢慢加入9 浓硫酸。乙酰苯胺逐渐溶解。将所得溶液放在冰水浴中冷却到0~2℃。
浓硫酸。乙酰苯胺逐渐溶解。将所得溶液放在冰水浴中冷却到0~2℃。
步骤2.用2 浓硫酸和2.3
浓硫酸和2.3 浓硝酸在冰水浴中配制混酸。
浓硝酸在冰水浴中配制混酸。
步骤3.向三颈烧瓶中滴加混酸,保持反应温度不超过5℃。滴加完毕,在室温下搅拌1h后,将反应混合物缓慢倒入装有20 水和30g碎冰的烧杯,并不断搅拌,立即析出淡黄色沉淀。
水和30g碎冰的烧杯,并不断搅拌,立即析出淡黄色沉淀。
步骤4.待碎冰全部融化后抽滤,洗涤,抽干得粗品。
步骤5.将该粗品纯化,得对硝基乙酰苯胺3.2g

回答下列问题:
(1)装置图中,冷凝管的出水口是_______ (填字母),仪器A中a的作用是_______ 。
(2)步骤1加冰醋酸有两个作用:①作溶剂,加速溶解,②_______ 。
(3)步骤3滴加混酸时不能过快,控制每10s滴加1~2滴,原因是_______ 。
(4)步骤5中洗涤粗品时_______(填标号)。
(5)本实验的产率为_______ 。

实验参数:
| 化合物名称 | 分子量 | 性状 | 熔点/℃ | 沸点/℃ | 溶解度 |
| 乙酰苯胺 | 135 | 白色晶体 | 114.3 | 304 | 溶于沸水,微溶于冷水,溶于乙醇和乙醚 |
| 对硝基乙酰苯胺 | 180 | 白色晶体 | 215.6 | 100(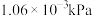 ) ) | 溶于热水,几乎不溶于冷水,溶于乙醇和乙醚 |
| 邻硝基乙酰苯胺 | 180 | 淡黄色片状或棱状晶体 | 94.0 | 100(0.13 ) ) | 溶于沸水,微溶于冷水,溶于乙醇和乙醚 |


乙酰苯胺与混酸在5℃下反应主要产物是对硝基乙酰苯胺,在40℃下反应则生成约25%的邻硝基乙酰苯胺。
步骤1.在三颈烧瓶内放入新制备的乙酰苯胺4.5g和4.5
 冰醋酸。在冷水浴冷却下搅拌,慢慢加入9
冰醋酸。在冷水浴冷却下搅拌,慢慢加入9 浓硫酸。乙酰苯胺逐渐溶解。将所得溶液放在冰水浴中冷却到0~2℃。
浓硫酸。乙酰苯胺逐渐溶解。将所得溶液放在冰水浴中冷却到0~2℃。步骤2.用2
 浓硫酸和2.3
浓硫酸和2.3 浓硝酸在冰水浴中配制混酸。
浓硝酸在冰水浴中配制混酸。步骤3.向三颈烧瓶中滴加混酸,保持反应温度不超过5℃。滴加完毕,在室温下搅拌1h后,将反应混合物缓慢倒入装有20
 水和30g碎冰的烧杯,并不断搅拌,立即析出淡黄色沉淀。
水和30g碎冰的烧杯,并不断搅拌,立即析出淡黄色沉淀。步骤4.待碎冰全部融化后抽滤,洗涤,抽干得粗品。
步骤5.将该粗品纯化,得对硝基乙酰苯胺3.2g

回答下列问题:
(1)装置图中,冷凝管的出水口是
(2)步骤1加冰醋酸有两个作用:①作溶剂,加速溶解,②
(3)步骤3滴加混酸时不能过快,控制每10s滴加1~2滴,原因是
(4)步骤5中洗涤粗品时_______(填标号)。
| A.用冷水洗 | B.用热水洗 | C.用乙醇洗 | D.先用冷水再用乙醇洗 |
(5)本实验的产率为
您最近一年使用:0次
6 . 邻苯二甲酰亚胺(PIMD)是一种重要的亚胺,是Gabriel合成法制备胺的原料。某实验室模拟氨水法以邻苯二甲酸酐为原料制备PIMD。
反应原理:
实验装置如图:
相关物质的物理性质如表:
实验步骤:
I.向250mL三颈烧瓶中加入74.0g邻苯二甲酸酐,边搅拌边滴入50.0mL浓氨水(稍过量),加热至80℃-95℃,待固体完全溶解后停止加热。将三颈烧瓶右端口所连装置取下改为蒸馏装置,继续加热,将溶液中的水及过量的氨蒸馏回收,此时烧瓶中有白色固体析出。
Ⅱ.继续升温至235℃-240℃,固体熔化,反应60分钟后,停止加热。冷却至室温,热水洗涤固体、抽滤、烘干,得到粗品白色粉末72.2g。
Ⅲ.向白色粉末中加入适量乙醇,加热回流使固体恰好溶解, ,将滤液降温冷却,有白色晶体析出,抽滤、洗涤、烘干后得白色晶体59.2g。
请回答下列问题:
(1)仪器A的名称为______ ,仪器A中盛装的试剂是______ 。(填标号)
a.碱石灰 b.五氧化二磷 c.浓硫酸
(2)步骤Ⅱ所得粗品中的杂质主要为________ 。
(3)邻苯二甲酸酐的熔沸点远低于邻苯二甲酰亚胺,原因可能是________ 。
(4)步骤Ⅲ的目的是利用重结晶进一步提纯邻苯二甲酰亚胺,该步骤中划线部分应补全的操作是______ 。选择乙醇作为提纯溶剂的主要原因是_______ 。
(5)本实验中邻苯二甲酰亚胺的产率最接近于______ 。(填标号)
a.85% b.80% c.75% d.70%
(6)邻苯二甲酰亚胺还可以用由邻二甲苯与氨气、氧气在加热条件下催化反应一步制得,写出该反应的化学方程式:________ 。
反应原理:

实验装置如图:

相关物质的物理性质如表:
| 物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 邻苯二甲酸酐 | 148 | 131~134 | 284 | 不溶于冷水,微溶于热水,稍溶于乙醇 |
| 邻苯二甲酰亚胺 | 147 | 232~235 | 366 | 微溶于热水,易溶于乙醇,易溶于碱溶液 |
I.向250mL三颈烧瓶中加入74.0g邻苯二甲酸酐,边搅拌边滴入50.0mL浓氨水(稍过量),加热至80℃-95℃,待固体完全溶解后停止加热。将三颈烧瓶右端口所连装置取下改为蒸馏装置,继续加热,将溶液中的水及过量的氨蒸馏回收,此时烧瓶中有白色固体析出。
Ⅱ.继续升温至235℃-240℃,固体熔化,反应60分钟后,停止加热。冷却至室温,热水洗涤固体、抽滤、烘干,得到粗品白色粉末72.2g。
Ⅲ.向白色粉末中加入适量乙醇,加热回流使固体恰好溶解, ,将滤液降温冷却,有白色晶体析出,抽滤、洗涤、烘干后得白色晶体59.2g。
请回答下列问题:
(1)仪器A的名称为
a.碱石灰 b.五氧化二磷 c.浓硫酸
(2)步骤Ⅱ所得粗品中的杂质主要为
(3)邻苯二甲酸酐的熔沸点远低于邻苯二甲酰亚胺,原因可能是
(4)步骤Ⅲ的目的是利用重结晶进一步提纯邻苯二甲酰亚胺,该步骤中划线部分应补全的操作是
(5)本实验中邻苯二甲酰亚胺的产率最接近于
a.85% b.80% c.75% d.70%
(6)邻苯二甲酰亚胺还可以用由邻二甲苯与氨气、氧气在加热条件下催化反应一步制得,写出该反应的化学方程式:
您最近一年使用:0次
7 . 氯乙酸( )是医药工业中重要的合成中间体。用氯乙酸制取镇静药巴比妥(K)的合成路线如下:
)是医药工业中重要的合成中间体。用氯乙酸制取镇静药巴比妥(K)的合成路线如下:

(1)A中非含氧官能团的名称___________ 。
(2)A与足量NaOH水溶液反应的化学方程式为___________ 。
已知:
(3)实验室利用该反应制备F时,最适合的装置是___________ (选填编号);选择该装置的理由是___________ 。
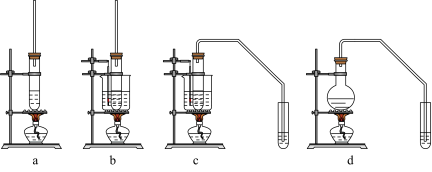
(4)最后一步反应为: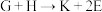 ,则H的结构简式为
,则H的结构简式为___________ 。
(5)能水解产生丁二酸(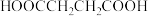 )的F的同分异构体有
)的F的同分异构体有___________ 种。
(6)结合题中流程信息,以乙烯为原料设计合成丁二酸的路线。合成路线常用的表示方式为: ,
,___________ 。
 )是医药工业中重要的合成中间体。用氯乙酸制取镇静药巴比妥(K)的合成路线如下:
)是医药工业中重要的合成中间体。用氯乙酸制取镇静药巴比妥(K)的合成路线如下:
(1)A中非含氧官能团的名称
(2)A与足量NaOH水溶液反应的化学方程式为
已知:
| 物质 | D | E | F |
| 熔点 | 135.6℃ | -117.3℃ | -50℃ |
| 沸点 | - (140℃分解) | 78℃ | 199.3℃ |

(4)最后一步反应为:
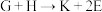 ,则H的结构简式为
,则H的结构简式为(5)能水解产生丁二酸(
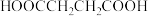 )的F的同分异构体有
)的F的同分异构体有(6)结合题中流程信息,以乙烯为原料设计合成丁二酸的路线。合成路线常用的表示方式为:
 ,
,
您最近一年使用:0次
名校
解题方法
8 . 乙酰苯胺是一种白色结晶粉末,可用作止痛剂、退热剂、防腐剂和染料中间体。
已知:
Ⅰ.粗乙酰苯胺的制备:
制备原理: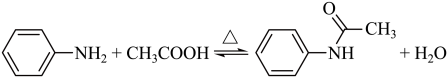
实验装置:如图所示(加热、夹持装置略)

实验步骤:
①向仪器a中加入11.4mL(约0.2mol)冰醋酸、9.1mL(约0.1mol)无水苯胺、0.1g锌粉;
②组装好仪器,对仪器a加热,当温度计读数达到100℃左右时有液体馏出,维持温度在100~105℃之间反应60min;
③反应结束后,在搅拌下趁热将反应液倒入盛有冷水的烧杯中,析出固体,将混合物抽滤得到乙酰苯胺粗品。
(1)仪器a的名称是___________ 。仪器a的最适宜规格为___________ (填标号)。
a.25mL b.50mL c.150mL d.200mL
(2)步骤②中锥形瓶中的馏出液主要成分是___________ (填物质名称),锥形瓶中实际收集的液体远多于理论量,可能的原因为___________ 。
(3)为探究锌粉用量对乙酰苯胺产率的影响,实验小组做了对比实验,实验数据如下表,试合理推测加入锌粉的作用是___________ ,第二组实验中锌粉用量最多但乙酰苯胺产率反而降低的原因可能是___________ 。
Ⅱ.乙酰苯胺的提纯:
将上述制得的粗乙酰苯胺粗产品移入500mL烧杯中,加入100mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,趁热过滤。待滤液冷却至室温,有晶体析出,称量产品为10.8g。
(4)上述提纯乙酰苯胺的方法是___________ 。
(5)该实验中乙酰苯胺的产率是___________ (保留两位有效数字)。
已知:
| 物质 | 苯胺 | 冰醋酸 | 乙酰苯胺 |
| 熔点 | -6.2℃ | 16.6℃ | 113℃ |
| 沸点 | 184℃ | 117.9℃ | 304℃ |
| 其他性质 | 微溶于水,易被氧化而变色 | — | 白色晶体,难溶于水,易溶于乙醇等有机溶剂 |
制备原理:
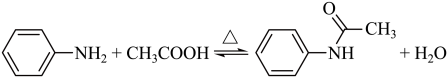
实验装置:如图所示(加热、夹持装置略)

实验步骤:
①向仪器a中加入11.4mL(约0.2mol)冰醋酸、9.1mL(约0.1mol)无水苯胺、0.1g锌粉;
②组装好仪器,对仪器a加热,当温度计读数达到100℃左右时有液体馏出,维持温度在100~105℃之间反应60min;
③反应结束后,在搅拌下趁热将反应液倒入盛有冷水的烧杯中,析出固体,将混合物抽滤得到乙酰苯胺粗品。
(1)仪器a的名称是
a.25mL b.50mL c.150mL d.200mL
(2)步骤②中锥形瓶中的馏出液主要成分是
(3)为探究锌粉用量对乙酰苯胺产率的影响,实验小组做了对比实验,实验数据如下表,试合理推测加入锌粉的作用是
| 组别 | 第一组 | 第二组 | 第三组 |
| 苯胺(mL) | 9.1 | 9.1 | 9.1 |
| 冰醋酸(mL) | 15.6 | 15.6 | 15.6 |
| 锌粉(g) | 1.625 | 3.25 | 0 |
| 产量(g) | 3.4 | 2.26 | 1.27 |
| 产率(%) | 41 | 30.1 | 17.1 |
Ⅱ.乙酰苯胺的提纯:
将上述制得的粗乙酰苯胺粗产品移入500mL烧杯中,加入100mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,趁热过滤。待滤液冷却至室温,有晶体析出,称量产品为10.8g。
(4)上述提纯乙酰苯胺的方法是
(5)该实验中乙酰苯胺的产率是
您最近一年使用:0次
2024-01-13更新
|
273次组卷
|
3卷引用:湖南省长沙市第一中学2023-2024学年高三上学期月考(五)化学试题
9 . 乙酰苯胺(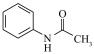 )具有退热镇痛作用,在OTC药物中占有重要地位。乙酰苯胺可通过苯胺(
)具有退热镇痛作用,在OTC药物中占有重要地位。乙酰苯胺可通过苯胺( )和乙酸反应制得,该反应是放热的可逆反应,其制备流程如下:
)和乙酸反应制得,该反应是放热的可逆反应,其制备流程如下:

已知:①苯胺在空气中易被氧化。
②可能用到的有关性质如下:
回答下列问题:
Ⅰ.乙酰苯胺的制备
(1)制备乙酰苯胺的化学方程式为_______ 。
(2)加入锌粉的原因是_______ 。
(3)“加热回流”的装置如图所示,a处使用的仪器为_______ (填“A”“B”或“C”),该仪器的名称是_______ 。
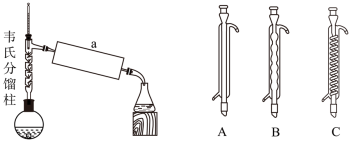
(4)“加热回流”的反应温度应控制在_______ (填标号)。
A.85-100℃ B.100-115℃ C.115-130℃
Ⅱ.乙酰苯胺的提纯
将上述制得的粗乙酰苯胺固体移入500mL烧杯中,加入100mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,趁热过滤。待滤液冷却至室温,有晶体析出,称量产品为10.0g。
(5)趁热过滤的目的是_______ ;这种提纯乙酰苯胺的方法叫_______ 。
(6)该实验中乙酰苯胺的产率是_______ (保留三位有效数字)。
 )具有退热镇痛作用,在OTC药物中占有重要地位。乙酰苯胺可通过苯胺(
)具有退热镇痛作用,在OTC药物中占有重要地位。乙酰苯胺可通过苯胺( )和乙酸反应制得,该反应是放热的可逆反应,其制备流程如下:
)和乙酸反应制得,该反应是放热的可逆反应,其制备流程如下:
已知:①苯胺在空气中易被氧化。
②可能用到的有关性质如下:
| 名称 | 相对分子质量 | 性状 | 密度 | 熔点/℃ | 沸点/℃ | 溶解度 | |
| g/100g水 | g/100g乙醇 | ||||||
| 苯胺 | 93 | 棕黄色液体 | 1.02 | -6.3 | 184 | 微溶 | ∞ |
| 冰醋酸 | 60 | 无色透明液体 | 1.05 | 16.6 | 117.9 | ∞ | ∞ |
| 乙酰苯胺 | 135 | 无色片状晶体 | 1.21 | 155~156 | 280~290 | 温度高,溶解度大 | 较水中大 |
Ⅰ.乙酰苯胺的制备
(1)制备乙酰苯胺的化学方程式为
(2)加入锌粉的原因是
(3)“加热回流”的装置如图所示,a处使用的仪器为

(4)“加热回流”的反应温度应控制在
A.85-100℃ B.100-115℃ C.115-130℃
Ⅱ.乙酰苯胺的提纯
将上述制得的粗乙酰苯胺固体移入500mL烧杯中,加入100mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,趁热过滤。待滤液冷却至室温,有晶体析出,称量产品为10.0g。
(5)趁热过滤的目的是
(6)该实验中乙酰苯胺的产率是
您最近一年使用:0次
10 . 乙酰苯胺( )有止痛、退热的功能,在实验室按以下流程进行制备。
)有止痛、退热的功能,在实验室按以下流程进行制备。
I.查阅资料:苯胺易被氧化,乙酰苯胺在碱性条件下水解,其他物质的有关性质如下表。
Ⅱ.制备过程:
(1)原理与装置。
实验装置如图。在三颈烧瓶中先加入 锌粒和
锌粒和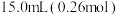 冰醋酸,然后用恒压滴液漏斗滴加
冰醋酸,然后用恒压滴液漏斗滴加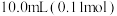 苯胺。
苯胺。
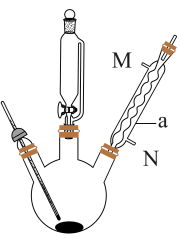
①球形冷凝管 的作用是
的作用是___________ ,冷凝水的进水口为___________ (填“M”或“N”)。
②加入锌粒,除了防止暴沸外,还能起到的作用是___________ 。
③写出该制备方法的主要反应方程式___________ 。
④制备过程中温度计控制示数在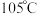 左右的原因是
左右的原因是___________ 。
(2)制得粗产品。
实验流程包括: ,其中最合适的“洗涤”是
,其中最合适的“洗涤”是___________ (填标号)。
a. 的乙醇溶液 b.
的乙醇溶液 b. 溶液 c.冰水 d.热水
溶液 c.冰水 d.热水
(3)重结晶提纯。
粗产品溶于沸水中配成饱和溶液 再加入少量蒸馏水
再加入少量蒸馏水 加入活性炭脱色
加入活性炭脱色 加热煮沸
加热煮沸
___________  冷却结晶
冷却结晶 过滤一洗涤
过滤一洗涤 干燥,得到
干燥,得到 产品。
产品。
Ⅲ.计算产率。
(4)已知:产率= ,本实验中乙酰苯胺的产率为
,本实验中乙酰苯胺的产率为___________ (保留两位有效数字)。
 )有止痛、退热的功能,在实验室按以下流程进行制备。
)有止痛、退热的功能,在实验室按以下流程进行制备。I.查阅资料:苯胺易被氧化,乙酰苯胺在碱性条件下水解,其他物质的有关性质如下表。
| 名称 | 熔点/℃ | 沸点/℃ | 溶解度/g(20℃) | |
| 水 | 乙醇 | |||
| 苯胺 | -6.3 | 184 | 3.4 | 任意比混溶 |
| 冰醋酸 | 16.6 | 118 | 任意比混溶 | 任意比混溶 |
| 乙酰苯胺 | 114.3 | 304 | 0.46(温度越高,溶解度越大) | 36.9 |
(1)原理与装置。
实验装置如图。在三颈烧瓶中先加入
 锌粒和
锌粒和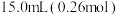 冰醋酸,然后用恒压滴液漏斗滴加
冰醋酸,然后用恒压滴液漏斗滴加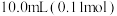 苯胺。
苯胺。
①球形冷凝管
 的作用是
的作用是②加入锌粒,除了防止暴沸外,还能起到的作用是
③写出该制备方法的主要反应方程式
④制备过程中温度计控制示数在
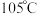 左右的原因是
左右的原因是(2)制得粗产品。
实验流程包括:
 ,其中最合适的“洗涤”是
,其中最合适的“洗涤”是a.
 的乙醇溶液 b.
的乙醇溶液 b. 溶液 c.冰水 d.热水
溶液 c.冰水 d.热水(3)重结晶提纯。
粗产品溶于沸水中配成饱和溶液
 再加入少量蒸馏水
再加入少量蒸馏水 加入活性炭脱色
加入活性炭脱色 加热煮沸
加热煮沸
 冷却结晶
冷却结晶 过滤一洗涤
过滤一洗涤 干燥,得到
干燥,得到 产品。
产品。Ⅲ.计算产率。
(4)已知:产率=
 ,本实验中乙酰苯胺的产率为
,本实验中乙酰苯胺的产率为
您最近一年使用:0次



