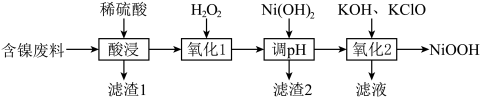
1 . NiOOH可用作碱性镍镉电池的电极材料,用含镍废料(主要成分是Ni,杂质有Al、Fe、SiO2)制取NiOOH的流程如图。
已知:ⅰ.Ni2+的性质较稳定;
ⅱ.有关金属离子沉淀的相关pH见下表
回答下列问题:
(1)Ni位于元素周期表第_______ 周期,第_______ 族。
(2)实际生产中发现H2O2的实际用量比理论用量多,原因是_______ 。
(3)“调pH”时pH的范围是_______ ,当溶液中离子浓度 时认为该离子沉淀完全,则常温下
时认为该离子沉淀完全,则常温下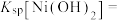
_______ 。
(4)“氧化2”中反应的离子方程式为_______ 。
(5)锌镍电池是一种可充电电池,其充电时总反应为: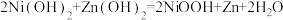 ,则放电时正极的电极反应式为
,则放电时正极的电极反应式为_______ ,充电时阴极周围溶液pH_______ (填“增大”“减小”或“不变”)。

已知:ⅰ.Ni2+的性质较稳定;
ⅱ.有关金属离子沉淀的相关pH见下表
| 沉淀物 |  |  |  |  |
| 开始沉淀时pH | 3.0 | 1.5 | 5.9 | 7.1 |
| 完全沉淀时pH | 4.7 | 3.2 | 9.0 | 9.2 |
(1)Ni位于元素周期表第
(2)实际生产中发现H2O2的实际用量比理论用量多,原因是
(3)“调pH”时pH的范围是
 时认为该离子沉淀完全,则常温下
时认为该离子沉淀完全,则常温下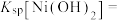
(4)“氧化2”中反应的离子方程式为
(5)锌镍电池是一种可充电电池,其充电时总反应为:
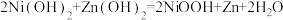 ,则放电时正极的电极反应式为
,则放电时正极的电极反应式为
您最近一年使用:0次
2023-09-08更新
|
191次组卷
|
3卷引用:湖北宜荆荆恩2023-2024学年高三上学期9月联考化学试题
名校
2 . 第IIB族元素(Zn、Cd、Hg)和第VIA族元素(S、Se、Te)组成的某些二元化合物常用作半导体材料,应用十分广泛。
(1)基态Se原子价电子排布式为_______ ,有_______ 种空间运动状态。
(2)碲酸(H6TeO6)是白色固体,经X射线衍射研究证明在碲酸分子内的6个羟基排列在碲原子的周围成八面体结构,碲酸中碲原子的价层电子对数为_______ 。
(3)CdTe可用作太阳能电池的吸收层,研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的流程如图:

①碲化镉吸收层中的CdTe参与反应的化学方程式为_______ ,该反应需要控制温度为50℃的原因为_______ ;滤渣1含有的一种单质是_______ 。
②常温下,向含Cd2+、Te4+滤液中加入NaOH溶液调节pH,当pH=10时,溶液中c(Cd2+)=_______ 。(已知Ksp[Cd(OH)2]=5.3×10-15)。
(1)基态Se原子价电子排布式为
(2)碲酸(H6TeO6)是白色固体,经X射线衍射研究证明在碲酸分子内的6个羟基排列在碲原子的周围成八面体结构,碲酸中碲原子的价层电子对数为
(3)CdTe可用作太阳能电池的吸收层,研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的流程如图:

①碲化镉吸收层中的CdTe参与反应的化学方程式为
②常温下,向含Cd2+、Te4+滤液中加入NaOH溶液调节pH,当pH=10时,溶液中c(Cd2+)=
您最近一年使用:0次
解题方法
3 . 2Zn(OH)2·ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2·ZnCO3的工艺流程如下:

(1)用(NH4)2SO4与NH3·H2O的混合溶液浸取锌焙砂生成[Zn(NH3)4]2+的过程中加入H2O2的目的是________ 。
(2)加入(NH4)2S除杂过程中的主要离子方程式为________ 。
(3)过滤3所得滤液可循环使用,其主要成分的化学式是_______ 。
(4)检验2Zn(OH)2·ZnCO3沉淀是否洗涤干净的方法是________ 。
(5)写出沉锌步骤中发生反应的化学方程式________ 。

(1)用(NH4)2SO4与NH3·H2O的混合溶液浸取锌焙砂生成[Zn(NH3)4]2+的过程中加入H2O2的目的是
(2)加入(NH4)2S除杂过程中的主要离子方程式为
(3)过滤3所得滤液可循环使用,其主要成分的化学式是
(4)检验2Zn(OH)2·ZnCO3沉淀是否洗涤干净的方法是
(5)写出沉锌步骤中发生反应的化学方程式
您最近一年使用:0次



