名校
1 . 新型除草剂丙炔氟草胺H(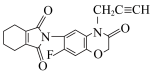 )的合成路线如图所示:
)的合成路线如图所示:

(1)物质A的结构简式为
(2)B→C为可逆反应,推测
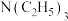 (一种有机碱)的作用是
(一种有机碱)的作用是(3)物质D中含氧官能团的名称为
(4)F→G的反应类型为
(5)D→E转化所需的无机试剂和反应条件为
(6)G→H的化学方程式为
(7)与B具有相同官能团且属于芳香族化合物的同分异构体数目为
您最近一年使用:0次
名校
解题方法
2 . 科学家成功制得新型可循环高分子材料,其合成路线如图所示。下列说法正确的是

| A.反应①中,标记*的碳原子被氧化 |
| B.反应②的类型为缩聚反应 |
| C.聚合物Ⅰ可以通过水解反应降解为小分子 |
| D.聚合物Ⅰ与聚合物Ⅱ均可通过适当的化学反应形成网状结构的高分子材料 |
您最近一年使用:0次
名校
解题方法
3 . 聚肉桂酸乙烯酯(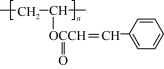 )是我国电子工业制造集成电路和半导体器件不可缺少的产品,其合成路线如图1所示:
)是我国电子工业制造集成电路和半导体器件不可缺少的产品,其合成路线如图1所示:
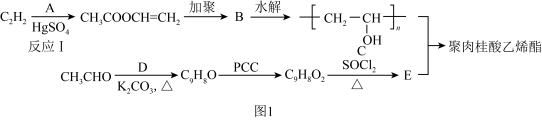
②
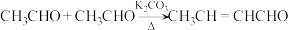 ;
;③
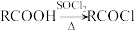 ;
;④
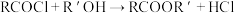 。
。回答下列问题:
(1)有机物A的名称为
(2)B的链节为
(3)C与E反应生成聚肉桂酸乙烯酯的化学方程式为
(4)工业上合成
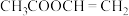 采用反应Ⅰ而不是利用相应的醇与羧酸酯化的原因是
采用反应Ⅰ而不是利用相应的醇与羧酸酯化的原因是(5)如图2所示是实验室中合成
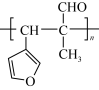 的路线,回答下列问题:
的路线,回答下列问题: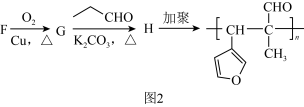
①呋喃( )与苯类似具有芳香性,分子中所有原子均共面且具有
)与苯类似具有芳香性,分子中所有原子均共面且具有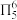 (5中心6电子大
(5中心6电子大 键),则呋喃中氧原子的杂化方式为
键),则呋喃中氧原子的杂化方式为
您最近一年使用:0次
4 . 汽车尾气是空气中碳氢化合物和氮氧化合物的主要来源之一,它们在特定的条件下可形成光化学烟雾。
Ⅰ.汽车尾气净化器中的主要反应:2NO+2CO 2CO2+N2。
2CO2+N2。
(1)汽车尾气中NO生成过程的能量变化如下图所示。1 mol N2和1 mol O2完全反应生成NO会______ (填“吸收”或“放出”)____ kJ能量。_____ 。
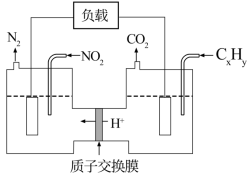
Ⅱ.一种利用烃(CxHy)来消除氮氧化物污染的工作原理如下图所示,装置中电极均为惰性电极,两侧电解质为同浓度的盐酸。___________ 。
Ⅲ.一种新型催化剂能使NO和CO发生反应2NO+2CO 2CO2+N2,已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
2CO2+N2,已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
(4)表中a=______ 。
(5)能验证温度对化学反应速率影响规律的是实验_______ (填实验编号)。
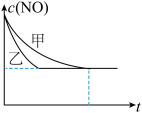
(6)实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线_____ (填“甲”或“乙”)。 2CO2(g)+N2(g),不能说明该反应已达到平衡状态的是______(填字母)。
2CO2(g)+N2(g),不能说明该反应已达到平衡状态的是______(填字母)。
Ⅰ.汽车尾气净化器中的主要反应:2NO+2CO
 2CO2+N2。
2CO2+N2。(1)汽车尾气中NO生成过程的能量变化如下图所示。1 mol N2和1 mol O2完全反应生成NO会

Ⅱ.一种利用烃(CxHy)来消除氮氧化物污染的工作原理如下图所示,装置中电极均为惰性电极,两侧电解质为同浓度的盐酸。
Ⅲ.一种新型催化剂能使NO和CO发生反应2NO+2CO
 2CO2+N2,已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
2CO2+N2,已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。| 实验 编号 | t/℃ | NO初始浓度 (mol·L-1) | CO初始浓度 (mol·L-1) | 催化剂的比表面积 (m2·g-1) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
| Ⅲ | 350 | a | 5.80×10-3 | 82 |
(4)表中a=
(5)能验证温度对化学反应速率影响规律的是实验
(6)实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线
 2CO2(g)+N2(g),不能说明该反应已达到平衡状态的是______(填字母)。
2CO2(g)+N2(g),不能说明该反应已达到平衡状态的是______(填字母)。| A.容器内温度不再变化 | B.容器内混合气体的平均相对分子质量保持不变 |
| C.2v逆(NO)=v正(N2) | D.容器内混合气体的密度保持不变 |
您最近一年使用:0次
5 . 某实验小组设计提取橘精油(主要成分为柠檬烯,沸点为176.0℃)的实验流程如图所示,下列说法正确的是

| A.利用如图所示装置对橘皮进行反复滴萃可提高柠檬烯的提取率 |
| B.有机试剂X可选用正己烷,分液时有机层从下口放出 |
| C.无水硫酸钠的作用是除去乙醇 |
| D.蒸馏获得柠檬烯时,为了受热均匀可以选择水浴加热 |
您最近一年使用:0次
6 . “绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。硫酸工业排出的尾气(主要含SO2)有多种处理方式。
Ⅰ.以黄铁矿(主要成分FeS2)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如图所示。
(1)由炉渣制备还原铁粉的化学方程式为_______ 。
(2)工业生产硫酸过程中,将SO2氧化为SO3时通常使用五氧化二钒(V2O5)作催化剂,并加热到400~500℃,采取该反应条件的目的是________ 。
(3)焦亚硫酸钠(Na2S2O5)中硫元素的化合价为_______ ,具有还原性,导致商品Na2S2O5中不可避免地存在Na2SO4杂质,检验其中含有 的方法是
的方法是_______ 。
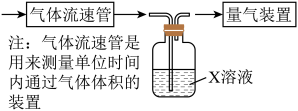
Ⅱ.有学者提出利用Fe2+、Fe3+等离子的催化作用,常温下将SO2氧化成 而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成
而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成 的转化率。
的转化率。
(5)若上述实验是在标准状况下进行的,欲测定转化器中SO2氧化成 的转化率,已知气体流速a mL·min-1,还需测定的数据有
的转化率,已知气体流速a mL·min-1,还需测定的数据有_____ 、______ 。
Ⅰ.以黄铁矿(主要成分FeS2)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如图所示。
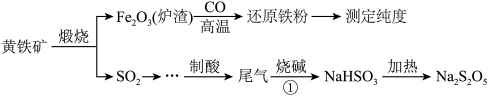
(1)由炉渣制备还原铁粉的化学方程式为
(2)工业生产硫酸过程中,将SO2氧化为SO3时通常使用五氧化二钒(V2O5)作催化剂,并加热到400~500℃,采取该反应条件的目的是
(3)焦亚硫酸钠(Na2S2O5)中硫元素的化合价为
 的方法是
的方法是Ⅱ.有学者提出利用Fe2+、Fe3+等离子的催化作用,常温下将SO2氧化成
 而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成
而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成 的转化率。
的转化率。
| A.碘的淀粉溶液 | B.酸性高锰酸钾溶液 |
| C.氢氧化钠溶液 | D.氯化钡溶液 |
(5)若上述实验是在标准状况下进行的,欲测定转化器中SO2氧化成
 的转化率,已知气体流速a mL·min-1,还需测定的数据有
的转化率,已知气体流速a mL·min-1,还需测定的数据有
您最近一年使用:0次
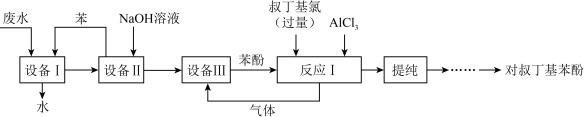
7 . 含酚废水被列为重点控制污染物。某实验小组设计如图所示流程处理含苯酚的废水,并用分离的苯酚制备对叔丁基苯酚:
请回答下列问题:
(1)设备Ⅰ、Ⅱ、Ⅲ中均采用了相同的操作方法,该操作的名称是_______ ;若在实验室进行该操作,用到的玻璃仪器为_______ 。
(2)设备Ⅲ中发生反应的离子方程式为_______ 。
(3)该流程循环利用的物质是________ 。
(4) 是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为
是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为________ 。
(5)提纯过程中,为除去 ,需将反应所得粗产品倒入适当浓度盐酸与碎冰组成的混合物中,这样操作的目的是
,需将反应所得粗产品倒入适当浓度盐酸与碎冰组成的混合物中,这样操作的目的是_______ 。
(6)用重结晶法提纯粗对叔丁基苯酚的操作顺序是:向粗产品中加入过量石油醚→加入活性炭脱色→ⅰ→ⅱ→ⅲ→ⅳ→挥发溶剂并保存,ⅰ~ⅳ处对应操作步骤分别为______ (填代号,可重复)。
a.用蒸馏水洗涤 b.过滤 c.冷却结晶 d.蒸发浓缩 e.蒸馏浓缩
(7)对叔丁基苯酚可作为抗氧化剂,其原理是________ 。
| 结构简式 | 部分物理性质 | |
| 叔丁基氯 |  | \ |
| 对叔丁基苯酚 |
| 溶于石油醚(一种由低沸点烃类物质组成的有机溶剂),难溶于冷水,微溶于热水 |
(1)设备Ⅰ、Ⅱ、Ⅲ中均采用了相同的操作方法,该操作的名称是
(2)设备Ⅲ中发生反应的离子方程式为
(3)该流程循环利用的物质是
(4)
 是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为
是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为(5)提纯过程中,为除去
 ,需将反应所得粗产品倒入适当浓度盐酸与碎冰组成的混合物中,这样操作的目的是
,需将反应所得粗产品倒入适当浓度盐酸与碎冰组成的混合物中,这样操作的目的是(6)用重结晶法提纯粗对叔丁基苯酚的操作顺序是:向粗产品中加入过量石油醚→加入活性炭脱色→ⅰ→ⅱ→ⅲ→ⅳ→挥发溶剂并保存,ⅰ~ⅳ处对应操作步骤分别为
a.用蒸馏水洗涤 b.过滤 c.冷却结晶 d.蒸发浓缩 e.蒸馏浓缩
(7)对叔丁基苯酚可作为抗氧化剂,其原理是
您最近一年使用:0次
名校
解题方法
8 . 甲壳质是由乙酰氨基葡萄糖相互结合形成的,其结构如图所示,下列关于甲壳质的说法正确的是

| A.能发生消去反应和取代反应 | B.分子中含有1个酰胺基 |
| C.适宜条件下水解能生成葡萄糖和氨基酸 | D.与淀粉和蔗糖均属于多糖 |
您最近一年使用:0次
9 . 香草醛( )存在于甜菜、香草豆中,具有抗惊厥、抗癫痫等作用。其质谱中分子离子峰的质荷比为152,核磁共振氢谱如图所示。下列有关说法错误的是
)存在于甜菜、香草豆中,具有抗惊厥、抗癫痫等作用。其质谱中分子离子峰的质荷比为152,核磁共振氢谱如图所示。下列有关说法错误的是

| A.香草醛苯环上的一卤代物有3种 |
| B.结构简式中“—Me”代表甲基 |
| C.1mol香草醛与足量浓溴水作用,消耗溴单质的物质的量超过1mol |
D.香草醛与足量酸性 溶液共热,可制得香草酸( 溶液共热,可制得香草酸(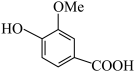 ) ) |
您最近一年使用:0次
10 . 丙酮是重要的化工试剂,某实验小组利用2-丙醇氧化法合成丙酮,实验步骤如下:(已知丙酮的沸点为56℃,不与水形成恒沸物,能被强氧化剂氧化成乙酸)
步骤一:制备氧化剂
称取6.00 g CrO3 (过量)充分溶解于80 mL水中,小心加入3 mL浓硫酸,得到橙红色溶液。
(1)溶液中显橙红色的离子为_______ (填离子符号)。
步骤二:制备丙酮
组装如图1所示的实验装置,将3.00 g异丙醇注入仪器X,向仪器Y中加入步骤一制备的溶液,控制滴速5~6 s每滴慢慢将溶液滴入到仪器X中,当仪器X中溶液变成棕黄色,且长时间搅拌后依然保持棕黄色时,停止滴加。________ 。
(3)使用仪器Y相较于普通分液漏斗的优点是_______ 。
(4)仪器Y中溶液刚滴入X中的实验现象为_______ 。
(5)能否将X、Y中的药品互换位置?____ (填“能”或“否”),原因是____ 。
步骤三:提纯
取少量一水合次磷酸钠(NaH2PO2·H2O)配成硫酸酸化溶液,加入仪器X中,待其中溶液呈现绿色时,将原制备装置改成蒸馏装置(如图2),收集55~56℃馏分。
(6)NaH2PO2·H2O的作用是_______ 。
(7)图2装置空白处使用的仪器为____ (填代号)。______ 。
步骤一:制备氧化剂
称取6.00 g CrO3 (过量)充分溶解于80 mL水中,小心加入3 mL浓硫酸,得到橙红色溶液。
(1)溶液中显橙红色的离子为
步骤二:制备丙酮
组装如图1所示的实验装置,将3.00 g异丙醇注入仪器X,向仪器Y中加入步骤一制备的溶液,控制滴速5~6 s每滴慢慢将溶液滴入到仪器X中,当仪器X中溶液变成棕黄色,且长时间搅拌后依然保持棕黄色时,停止滴加。
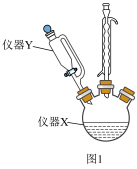
(3)使用仪器Y相较于普通分液漏斗的优点是
(4)仪器Y中溶液刚滴入X中的实验现象为
(5)能否将X、Y中的药品互换位置?
步骤三:提纯
取少量一水合次磷酸钠(NaH2PO2·H2O)配成硫酸酸化溶液,加入仪器X中,待其中溶液呈现绿色时,将原制备装置改成蒸馏装置(如图2),收集55~56℃馏分。
(6)NaH2PO2·H2O的作用是
(7)图2装置空白处使用的仪器为

A.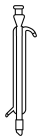 B.
B.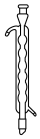 C.
C.
您最近一年使用:0次