1 . 四氮化四硫(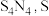 为
为 价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与
价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与 反应制备,反应装置如图所示(夹持和加热装置已省略)。
反应制备,反应装置如图所示(夹持和加热装置已省略)。
已知: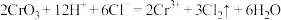 ;
;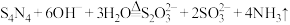
步骤如下: ,打开
,打开 和
和 ,先向装置C中通入干燥纯净的
,先向装置C中通入干燥纯净的 ,待装置C中充满黄绿色气体时,开始加热C,使
,待装置C中充满黄绿色气体时,开始加热C,使 与
与 在
在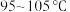 下反应生成
下反应生成 ;
;
②待装置C中的 全部反应后,关闭止水夹
全部反应后,关闭止水夹 ,撤掉装置A、B;
,撤掉装置A、B;
③ 处连接制
处连接制 的装置,关闭止水夹
的装置,关闭止水夹 ,打开
,打开 和
和 ,通入干燥纯净的
,通入干燥纯净的 ,反应制得
,反应制得 。
。
回答下列问题:
(1)装置A用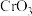 粉末与浓盐酸反应制取
粉末与浓盐酸反应制取 ,发生装置A可以选用
,发生装置A可以选用_________ 。(填选项) 时为使装置C受热均匀,可采用的最佳加热方式为
时为使装置C受热均匀,可采用的最佳加热方式为____________ ;
(3)制取 的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式
的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式_____________ ;
(4)装置E的作用是____________ 、_________ ;
(5)测定 的纯度:称取
的纯度:称取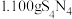 样品(杂质不参与反应),加入
样品(杂质不参与反应),加入 溶液,并加热,释放出的氨气用足量
溶液,并加热,释放出的氨气用足量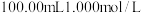 硼酸吸收[假定溶液体积不变,反应为:
硼酸吸收[假定溶液体积不变,反应为: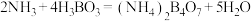 ].反应后的溶液再用
].反应后的溶液再用 的盐酸进行滴定[滴定反应为:
的盐酸进行滴定[滴定反应为: ],重复三次实验.实验数据记录如下表所示:
],重复三次实验.实验数据记录如下表所示:
____________ .(填选项)
A.滴定时应先快后慢滴入盐酸,且眼睛注视滴定管中液面变化
B.滴加最后半滴方法是:将旋塞稍稍转动,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁,使溶液流入锥形瓶,振荡摇匀
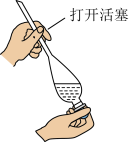
C.滴定终点装盐酸的滴定管液面如图所示,则读数为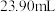
D.滴定管在滴定前有气泡,滴定后气泡消失,导致测定的结果偏高
②制得的 的纯度为
的纯度为____________ 。(保留四位有效数字)
(6)副产物 溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)
溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)
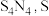 为
为 价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与
价)为橙黄色固体,易被氧化,难溶于水,易溶于四氯化碳,可用氨气与 反应制备,反应装置如图所示(夹持和加热装置已省略)。
反应制备,反应装置如图所示(夹持和加热装置已省略)。已知:
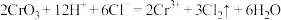 ;
;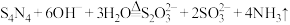
步骤如下:

 ,打开
,打开 和
和 ,先向装置C中通入干燥纯净的
,先向装置C中通入干燥纯净的 ,待装置C中充满黄绿色气体时,开始加热C,使
,待装置C中充满黄绿色气体时,开始加热C,使 与
与 在
在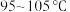 下反应生成
下反应生成 ;
;②待装置C中的
 全部反应后,关闭止水夹
全部反应后,关闭止水夹 ,撤掉装置A、B;
,撤掉装置A、B;③
 处连接制
处连接制 的装置,关闭止水夹
的装置,关闭止水夹 ,打开
,打开 和
和 ,通入干燥纯净的
,通入干燥纯净的 ,反应制得
,反应制得 。
。回答下列问题:
(1)装置A用
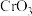 粉末与浓盐酸反应制取
粉末与浓盐酸反应制取 ,发生装置A可以选用
,发生装置A可以选用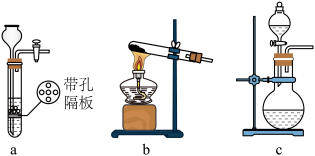
 时为使装置C受热均匀,可采用的最佳加热方式为
时为使装置C受热均匀,可采用的最佳加热方式为(3)制取
 的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式
的同时装置C中还生成一种常见固体单质和一种盐,写出反应的化学方程式(4)装置E的作用是
(5)测定
 的纯度:称取
的纯度:称取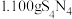 样品(杂质不参与反应),加入
样品(杂质不参与反应),加入 溶液,并加热,释放出的氨气用足量
溶液,并加热,释放出的氨气用足量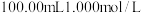 硼酸吸收[假定溶液体积不变,反应为:
硼酸吸收[假定溶液体积不变,反应为: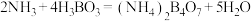 ].反应后的溶液再用
].反应后的溶液再用 的盐酸进行滴定[滴定反应为:
的盐酸进行滴定[滴定反应为: ],重复三次实验.实验数据记录如下表所示:
],重复三次实验.实验数据记录如下表所示:实验序号 | 初始读数 | 最终读数 |
Ⅰ | 0.20 | 20.42 |
Ⅱ | 0.40 | 24.85 |
Ⅲ | 1.00 | 21.18 |

A.滴定时应先快后慢滴入盐酸,且眼睛注视滴定管中液面变化
B.滴加最后半滴方法是:将旋塞稍稍转动,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁,使溶液流入锥形瓶,振荡摇匀
C.滴定终点装盐酸的滴定管液面如图所示,则读数为
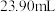
D.滴定管在滴定前有气泡,滴定后气泡消失,导致测定的结果偏高
②制得的
 的纯度为
的纯度为(6)副产物
 溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)
溶于水加入硫酸铜溶液中先沉淀后溶解,再向溶解后的深蓝色溶液中加入乙醇后,析出深蓝色晶体,下列叙述正确的是____________.(填选项)A.析出的深蓝色晶体为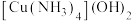 |
| B.深蓝色晶体中的阴阳离子构型都为正四面体形 |
C. 与 与 形成的配位键比 形成的配位键比 与 与 形成的配位键更稳定 形成的配位键更稳定 |
D.由配体 形成配离子 形成配离子 的过程中 的过程中 键角变大 键角变大 |
您最近一年使用:0次
2 . 有机物X是一种瞬干胶,在常温常压下受水的引发可快速聚合实现黏合,其原理如图所示。下列说法错误的是
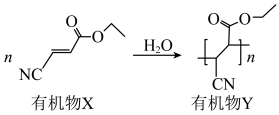
| A.有机物X中所有碳原子可能共平面 |
| B.有机物X中碳原子的杂化方式有两种 |
| C.X转化为Y的反应原子利用率为100% |
D.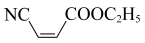 与有机物X互为顺反异构体 与有机物X互为顺反异构体 |
您最近一年使用:0次
解题方法
3 . 氮化铬的晶胞结构如图所示,A点原子坐标 ,密度为
,密度为 ,摩尔质量为
,摩尔质量为 ,晶胞参数为
,晶胞参数为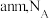 代表阿伏加德罗常数的值.下列说法错误的是
代表阿伏加德罗常数的值.下列说法错误的是
 ,密度为
,密度为 ,摩尔质量为
,摩尔质量为 ,晶胞参数为
,晶胞参数为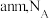 代表阿伏加德罗常数的值.下列说法错误的是
代表阿伏加德罗常数的值.下列说法错误的是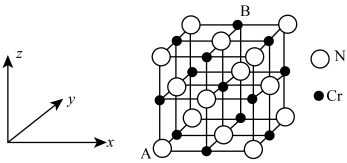
A.该晶体的化学式为 | B.B点原子坐标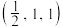 |
C. 原子位于N原子构成的四面体空隙中 原子位于N原子构成的四面体空隙中 | D.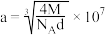 |
您最近一年使用:0次
4 . 实验装置为实验提供必要条件和测量手段。如图装置不能达到实验目的的是
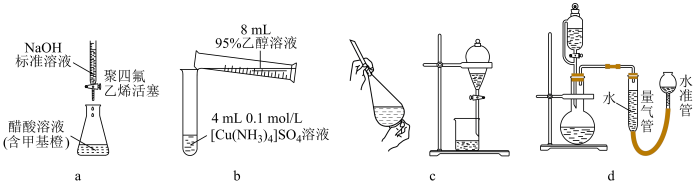
| A.图a测定醋酸溶液的浓度 |
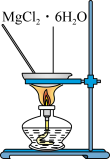
| B.图b制备[Cu(NH3)4]SO4•H2O晶体 |
| C.图c用NaOH溶液除去溴苯中的溴单质 |
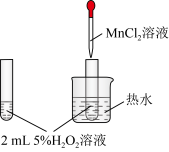
| D.图d测定一定质量的Na2O2和Na2O混合物中Na2O2的含量 |
您最近一年使用:0次
昨日更新
|
316次组卷
|
2卷引用:辽宁省重点高中协作校2024届高三下学期第二次模拟考试化学试题
5 . 尼达尼布用于治疗特发性肺纤维化,其结构简式如图所示,下列说法正确的是
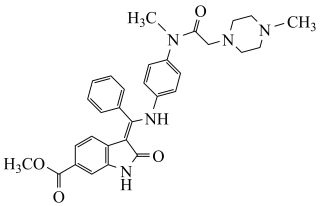
| A.分子中H原子的个数为偶数 |
| B.分子中存在手性碳原子 |
| C.1mol该物质与足量NaOH溶液反应,最多可消耗2molNaOH |
| D.可以发生取代反应、氧化反应、还原反应和聚合反应 |
您最近一年使用:0次
解题方法
6 . 下列实验方案设计、操作或结论均正确的是
| A | B |
|
|
| 分液漏斗放气操作 | 制取无水 |
| C | D |
|
|
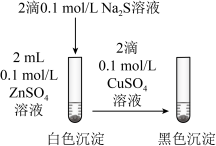
判断溶度积: | 验证 对 对 的分解有催化作用 的分解有催化作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 己二酸(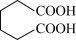 ,其相对分子质量为146)是一种重要的化工原料和合成中间体。某实验小组以钨磷酸为催化剂,开展己二酸的合成及性质探究实验。
,其相对分子质量为146)是一种重要的化工原料和合成中间体。某实验小组以钨磷酸为催化剂,开展己二酸的合成及性质探究实验。
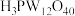 )的制备实验流程如图:
)的制备实验流程如图: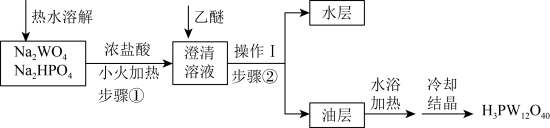
(2)水层中的物质有大量
 和少量
和少量 ,步骤①中发生反应的化学方程式为
,步骤①中发生反应的化学方程式为Ⅱ.己二酸的合成
向三颈烧瓶中加入
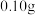 钨磷酸催化剂和
钨磷酸催化剂和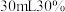 双氧水,在室温下搅拌
双氧水,在室温下搅拌 ,然后加入
,然后加入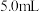 试剂X,得到溶液A。
试剂X,得到溶液A。(3)环己烯、环己醇、环己酮均可被双氧水氧化成己二酸。仅从所需双氧水理论用量的角度看,试剂X的最佳选择是
A.环己烯(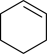 ) B.环己醇()
) B.环己醇()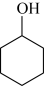 C.环己酮(
C.环己酮(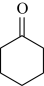 )
)
 从溶液A获取己二酸晶体,对应的实验操作为:
从溶液A获取己二酸晶体,对应的实验操作为: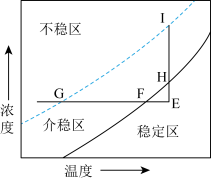
将
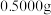 己二酸样品配制成
己二酸样品配制成 溶液,每次取
溶液,每次取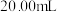 试样溶液于锥形瓶中,滴入几滴酚酞试液,用
试样溶液于锥形瓶中,滴入几滴酚酞试液,用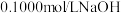 溶液滴定至终点,平均消耗
溶液滴定至终点,平均消耗 溶液
溶液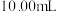 (己二酸被完全中和)。
(己二酸被完全中和)。(5)①下列说法错误的是
A.用
 容量瓶配制成溶液后,最好用
容量瓶配制成溶液后,最好用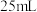 规格的量筒量取待测液于锥形瓶中
规格的量筒量取待测液于锥形瓶中B.滴定时,未用待测液润洗锥形瓶,则测定结果偏低
C.接近滴定终点时,应控制活塞,改为滴加半滴标准液,直至溶液由无色变为浅红色,且半分钟内不变色
D.若滴定前滴定管尖嘴部分无气泡,滴定后产生气泡,则测定结果偏高
②己二酸的纯度为
 。
。(6)若要得到纯度更高的己二酸,可通过
您最近一年使用:0次
8 . 对锂盐进行掺杂和改进所获得的一种离子液体,能显著提高锂离子电池传输电荷的能力,其结构如图所示。已知A、B、C、D、E为短周期元素,且A、B原子的电子数之和等于C、D原子价电子数之和。下列说法中正确的是
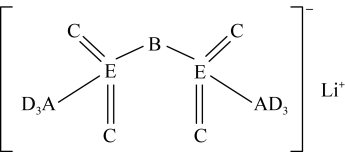
| A.A的简单氢化物是极性分子 | B.第一电离能: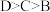 |
C. 中E原子为 中E原子为 杂化 杂化 | D.该锂盐的熔点高于 |
您最近一年使用:0次
名校
9 . 氢能源是最具应用前景的能源之一。甲烷-水蒸气催化重整制氢(SMR)是一种制高纯氢的方法之一,其涉及的主要反应如下:
反应Ⅰ: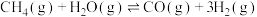
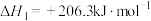
反应Ⅱ: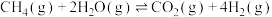

反应Ⅲ: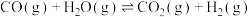
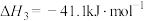
回答下列问题:
(1)反应Ⅱ能自发进行的条件是_______ 。
(2)一定温度下,向某容积为1L的恒容容器中按照水碳比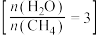 充入amolCH4(g)和3amolH2O(g),tmin后反应达到平衡。达到平衡时,容器中CO为mmol,CO2为nmol。
充入amolCH4(g)和3amolH2O(g),tmin后反应达到平衡。达到平衡时,容器中CO为mmol,CO2为nmol。
①下列说法不正确 的是_______ 。
A.为防止催化剂中毒和安全事故发生,需对原料气进行脱硫等净化处理
B.提高水碳比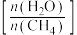 ,有利于提高H2的产率
,有利于提高H2的产率
C.其他条件不变,压缩容器体积,反应Ⅱ的平衡不发生移动
D.以Ni/γ-Al2O3作催化剂,降低反应活化能,提高反应速率和原料平衡利用率
②反应Ⅲ的平衡常数K=_______ (用含a,m,n的代数式表示)。
(3)650((局部温度过高会造成积碳)、按照一定流速通入原料气,当水碳比[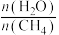 ]一定时,催化剂中无添加吸附剂和添加P-Li4SiO4吸附((吸收CO2),各气体组分反应的平衡含量与时间的关系如图所示:
]一定时,催化剂中无添加吸附剂和添加P-Li4SiO4吸附((吸收CO2),各气体组分反应的平衡含量与时间的关系如图所示:_______ 。
②实验时发现t1min后CO2的平衡含量低于理论平衡值,CO的平衡含量高于理论平衡值,可能的原因是_______ (用化学反应方程式表示)。
(4)该反应常采用钯膜分离技(可选择性地让某气体通过而离开体系),其机理如图所示,其中过程2: ,其活化能E((正)<E((逆);过程3:H*在钯膜内的迁移速率是决速步(*表示物质吸附在催化剂表面),下列说法
,其活化能E((正)<E((逆);过程3:H*在钯膜内的迁移速率是决速步(*表示物质吸附在催化剂表面),下列说法不正确 的是_______。
反应Ⅰ:
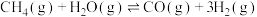
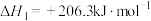
反应Ⅱ:
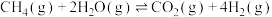

反应Ⅲ:
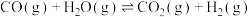
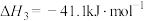
回答下列问题:
(1)反应Ⅱ能自发进行的条件是
(2)一定温度下,向某容积为1L的恒容容器中按照水碳比
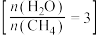 充入amolCH4(g)和3amolH2O(g),tmin后反应达到平衡。达到平衡时,容器中CO为mmol,CO2为nmol。
充入amolCH4(g)和3amolH2O(g),tmin后反应达到平衡。达到平衡时,容器中CO为mmol,CO2为nmol。①下列说法
A.为防止催化剂中毒和安全事故发生,需对原料气进行脱硫等净化处理
B.提高水碳比
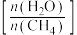 ,有利于提高H2的产率
,有利于提高H2的产率C.其他条件不变,压缩容器体积,反应Ⅱ的平衡不发生移动
D.以Ni/γ-Al2O3作催化剂,降低反应活化能,提高反应速率和原料平衡利用率
②反应Ⅲ的平衡常数K=
(3)650((局部温度过高会造成积碳)、按照一定流速通入原料气,当水碳比[
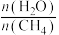 ]一定时,催化剂中无添加吸附剂和添加P-Li4SiO4吸附((吸收CO2),各气体组分反应的平衡含量与时间的关系如图所示:
]一定时,催化剂中无添加吸附剂和添加P-Li4SiO4吸附((吸收CO2),各气体组分反应的平衡含量与时间的关系如图所示: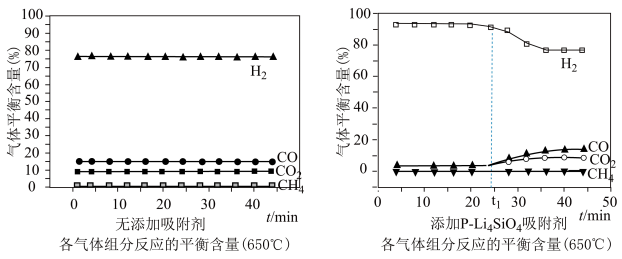
②实验时发现t1min后CO2的平衡含量低于理论平衡值,CO的平衡含量高于理论平衡值,可能的原因是
(4)该反应常采用钯膜分离技(可选择性地让某气体通过而离开体系),其机理如图所示,其中过程2:
 ,其活化能E((正)<E((逆);过程3:H*在钯膜内的迁移速率是决速步(*表示物质吸附在催化剂表面),下列说法
,其活化能E((正)<E((逆);过程3:H*在钯膜内的迁移速率是决速步(*表示物质吸附在催化剂表面),下列说法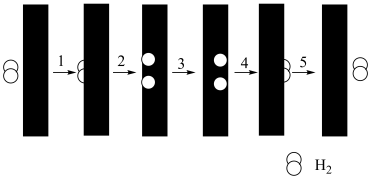
| A.钯膜对H2分子的透过具有选择性 |
B.过程4的 |
| C.采用钯膜分离技术可以提高原料的利用率 |
| D.常用N2将过程5中的H2吹扫出反应器而促进反应 |
您最近一年使用:0次
10 .  代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.标准状况下,22.4L  和44.8L 和44.8L  在光照下充分反应后分子数仍为 在光照下充分反应后分子数仍为 |
B.电解精炼粗铜时,阳极质量减少6.4g,外电路中通过电子的数目为 |
C.1mol Na在空气中受热完全转化成 ,转移电子的数目为 ,转移电子的数目为 |
D.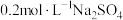 溶液中含有 溶液中含有 和 和 的总物质的量为0.6mol 的总物质的量为0.6mol |
您最近一年使用:0次