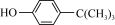
1 . 含酚废水被列为重点控制污染物。某实验小组设计如图所示流程处理含苯酚的废水,并用分离的苯酚制备对叔丁基苯酚:
请回答下列问题:
(1)设备Ⅰ、Ⅱ、Ⅲ中均采用了相同的操作方法,该操作的名称是_______ ;若在实验室进行该操作,用到的玻璃仪器为_______ 。
(2)设备Ⅲ中发生反应的离子方程式为_______ 。
(3)该流程循环利用的物质是________ 。
(4) 是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为
是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为________ 。
(5)提纯过程中,为除去 ,需将反应所得粗产品倒入适当浓度盐酸与碎冰组成的混合物中,这样操作的目的是
,需将反应所得粗产品倒入适当浓度盐酸与碎冰组成的混合物中,这样操作的目的是_______ 。
(6)用重结晶法提纯粗对叔丁基苯酚的操作顺序是:向粗产品中加入过量石油醚→加入活性炭脱色→ⅰ→ⅱ→ⅲ→ⅳ→挥发溶剂并保存,ⅰ~ⅳ处对应操作步骤分别为______ (填代号,可重复)。
a.用蒸馏水洗涤 b.过滤 c.冷却结晶 d.蒸发浓缩 e.蒸馏浓缩
(7)对叔丁基苯酚可作为抗氧化剂,其原理是________ 。
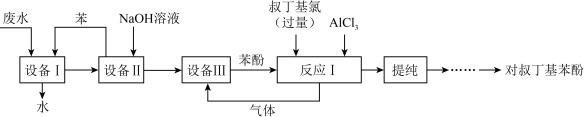
| 结构简式 | 部分物理性质 | |
| 叔丁基氯 |  | \ |
| 对叔丁基苯酚 |
| 溶于石油醚(一种由低沸点烃类物质组成的有机溶剂),难溶于冷水,微溶于热水 |
(1)设备Ⅰ、Ⅱ、Ⅲ中均采用了相同的操作方法,该操作的名称是
(2)设备Ⅲ中发生反应的离子方程式为
(3)该流程循环利用的物质是
(4)
 是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为
是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为(5)提纯过程中,为除去
 ,需将反应所得粗产品倒入适当浓度盐酸与碎冰组成的混合物中,这样操作的目的是
,需将反应所得粗产品倒入适当浓度盐酸与碎冰组成的混合物中,这样操作的目的是(6)用重结晶法提纯粗对叔丁基苯酚的操作顺序是:向粗产品中加入过量石油醚→加入活性炭脱色→ⅰ→ⅱ→ⅲ→ⅳ→挥发溶剂并保存,ⅰ~ⅳ处对应操作步骤分别为
a.用蒸馏水洗涤 b.过滤 c.冷却结晶 d.蒸发浓缩 e.蒸馏浓缩
(7)对叔丁基苯酚可作为抗氧化剂,其原理是
您最近一年使用:0次
名校
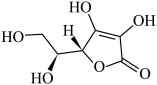
2 . 维生素C的结构简式如图所示,下列关于维生素C的说法错误的是
| A.维生素C又称抗坏血酸,因此它属于羧酸类物质 |
B.维生素C在 较大的溶液中无法稳定存在 较大的溶液中无法稳定存在 |
| C.向碘和淀粉的混合溶液中加足量维生素C可观察到溶液蓝色褪去 |
| D.维生素C是人体所需的营养物质之一 |
您最近一年使用:0次
3 . 请按要求回答下列问题:
Ⅰ.按性质可把烃分为饱和烃(烷烃)和不饱和烃。
(1)已知某链状烷烃分子中电子数为42,该烷烃的分子式为________ ,其同分异构体共有______ 种。该链状烷烃中沸点最低的是_______ (写结构简式),其二氯代物有____ 种同分异构体。
(2)在常温常压下,有CH4、C2H4、C3H8和C4H8四种气态烃。取等质量的四种气态烃,分别在足量的氧气中完全燃烧,消耗氧气的量最多的是______ (填分子式,下同)。这四种烃中,一定能使酸性KMnO4溶液褪色的是_______ 。
(4)反应①的化学方程式为_______ ,反应类型为______ ;反应③的化学方程式为______ ,反应类型为_______ 。
Ⅰ.按性质可把烃分为饱和烃(烷烃)和不饱和烃。
(1)已知某链状烷烃分子中电子数为42,该烷烃的分子式为
(2)在常温常压下,有CH4、C2H4、C3H8和C4H8四种气态烃。取等质量的四种气态烃,分别在足量的氧气中完全燃烧,消耗氧气的量最多的是
Ⅱ.聚氯乙烯( )简称PVC,是当今世界上产量最大、应用最广的塑料之一、工业上用乙烯和氯气为原料经下列各步合成PVC:
)简称PVC,是当今世界上产量最大、应用最广的塑料之一、工业上用乙烯和氯气为原料经下列各步合成PVC:

| A.PVC的单体是CH3CH2Cl | B.PVC是高分子化合物 |
| C.PVC能够使溴的四氯化碳溶液褪色 | D.PVC易降解 |
(4)反应①的化学方程式为
您最近一年使用:0次
4 . 氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨催化氧化制硝酸的流程示意图。请回答下列问题。(已知NO与 在高温时不易反应)
在高温时不易反应)___________ (填化学式)常用作保护气(如填充灯泡、焊接保护等),实验室制取氨气的化学方程式___________ ,液氨常用作___________ 。
(2)氧化炉中发生反应的方程式为___________ 。
(3)A是什么物质___________ ,向吸收塔中持续通入A的作用为___________ 。
(4)在实验室中硝酸要保存在棕色试剂瓶中避光保存,请用化学方程式表示其原因___________ 。
(5)为避免硝酸工业尾气中氮的氧化物(以 为例)污染环境,可在“尾气处理装置”中使用具有碱性的
为例)污染环境,可在“尾气处理装置”中使用具有碱性的 溶液等吸收尾气,写出相关反应的化学方程式:
溶液等吸收尾气,写出相关反应的化学方程式:___________ 。
(6)联氨( )是氮元素与氢元素形成的另一种化合物,可由
)是氮元素与氢元素形成的另一种化合物,可由 与NaClO溶液反应制得,请写出相应反应的离子方程式
与NaClO溶液反应制得,请写出相应反应的离子方程式___________ 。已知联氨与氨性质类似,可看成一种二元弱碱(反应的实质是N原子提供孤电子对,与 形成一种特殊的共价键),则向联氨溶液中加入过量硫酸生成的酸式盐的化学式为
形成一种特殊的共价键),则向联氨溶液中加入过量硫酸生成的酸式盐的化学式为___________ 。
 在高温时不易反应)
在高温时不易反应)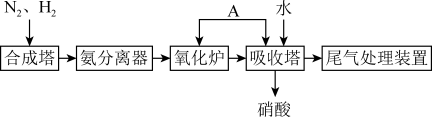
(2)氧化炉中发生反应的方程式为
(3)A是什么物质
(4)在实验室中硝酸要保存在棕色试剂瓶中避光保存,请用化学方程式表示其原因
(5)为避免硝酸工业尾气中氮的氧化物(以
 为例)污染环境,可在“尾气处理装置”中使用具有碱性的
为例)污染环境,可在“尾气处理装置”中使用具有碱性的 溶液等吸收尾气,写出相关反应的化学方程式:
溶液等吸收尾气,写出相关反应的化学方程式:(6)联氨(
 )是氮元素与氢元素形成的另一种化合物,可由
)是氮元素与氢元素形成的另一种化合物,可由 与NaClO溶液反应制得,请写出相应反应的离子方程式
与NaClO溶液反应制得,请写出相应反应的离子方程式 形成一种特殊的共价键),则向联氨溶液中加入过量硫酸生成的酸式盐的化学式为
形成一种特殊的共价键),则向联氨溶液中加入过量硫酸生成的酸式盐的化学式为
您最近一年使用:0次
5 . NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用。下列说法不正确的是

A.放电时, 向石墨Ⅰ电极迁移 向石墨Ⅰ电极迁移 |
| B.石墨Ⅰ电极电势高于石墨Ⅱ电极 |
| C.电池总反应式为4NO2+O2=2N2O5 |
| D.当外电路通过4 mol e-,负极上共产生4 mol N2O5 |
您最近一年使用:0次
解题方法
6 . 下列分子中,所有原子不可能在同一平面内的是
| A.CH2=CHCl | B.CH2=CHCH3 |
| C.CF2=CF2 | D.CO2 |
您最近一年使用:0次
解题方法
7 . 把在空气中久置的铝片5.0 g投入盛有50 mL 0.1 mol·L-1盐酸的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系可用如图所示的坐标曲线来表示,下列推论错误的是
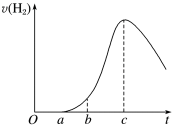
| A.O→a不产生氢气是因为表面的氧化物隔离了铝和稀盐酸 |
| B.b→c段产生氢气的速率增加较快的主要原因之一是溶液温度升高 |
| C.Cl-的浓度对该反应的速率一定没有影响 |
| D.t>c时,产生氢气的速率降低的主要原因是溶液中H+浓度下降 |
您最近一年使用:0次
名校
解题方法
8 . 贝诺酯是由阿司匹林、扑热息痛经化学法制备的解热镇痛抗炎药,其合成反应式(反应条件略去)如下,下列叙述错误的是
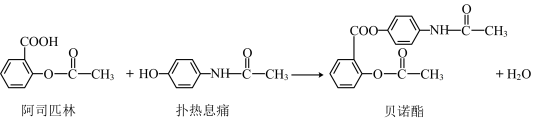
| A.FeCl3溶液可鉴别阿司匹林和扑热息痛 |
| B.贝诺酯与足量NaOH溶液共热后再酸化,最终生成阿司匹林和扑热息痛 |
| C.1 mol阿司匹林最多可消耗3 mol NaOH |
| D.常温下贝诺酯在水中的溶解度小于扑热息痛 |
您最近一年使用:0次
名校
9 . 在 密闭容器中,800℃时,反应
密闭容器中,800℃时,反应 体系中,
体系中,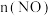 随时间的变化如下表所示,各物质的浓度一时间曲线如图所示。
随时间的变化如下表所示,各物质的浓度一时间曲线如图所示。
(1) 用
用 表示的化学反应速率
表示的化学反应速率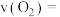
_______ 。从表中可以看出,该反应化学反应速率逐渐减慢,原因是_______ 。
(2)图中 点处反应
点处反应_______ (填“已达到”或“未达到”)平衡状态,A点处v(正)_______ (填“>”或“<”)v(逆)。
(3)若要加快该反应速率,可以采取的措施是_______ (任写两点)。
(4)下列能够说明反应已达到平衡状态的是_______(填字母)。
(5)已知该反应为放热反应,若生成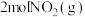 放出热量为
放出热量为 ,则通入
,则通入 与足量
与足量 充分反应生成
充分反应生成 放出的热量
放出的热量_______ (填“>”“<”或“=”)Q。
 密闭容器中,800℃时,反应
密闭容器中,800℃时,反应 体系中,
体系中,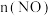 随时间的变化如下表所示,各物质的浓度一时间曲线如图所示。
随时间的变化如下表所示,各物质的浓度一时间曲线如图所示。时间 | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

(1)
 用
用 表示的化学反应速率
表示的化学反应速率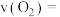
(2)图中
 点处反应
点处反应(3)若要加快该反应速率,可以采取的措施是
(4)下列能够说明反应已达到平衡状态的是_______(填字母)。
| A.混合气体的颜色不再变化 | B.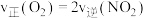 |
| C.混合气体平均摩尔质量保持不变 | D. 发生反应同时生成 发生反应同时生成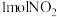 |
(5)已知该反应为放热反应,若生成
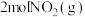 放出热量为
放出热量为 ,则通入
,则通入 与足量
与足量 充分反应生成
充分反应生成 放出的热量
放出的热量
您最近一年使用:0次
名校
解题方法
10 . 反应热可分为燃烧热、生成热等,由稳定单质化合生成1mol纯物质的反应热称为生成热 。下图分别表示
。下图分别表示 和
和 分解时的能量变化情况(单位:kJ)。下列说法错误的是
分解时的能量变化情况(单位:kJ)。下列说法错误的是
 。下图分别表示
。下图分别表示 和
和 分解时的能量变化情况(单位:kJ)。下列说法错误的是
分解时的能量变化情况(单位:kJ)。下列说法错误的是
A.CO的燃烧热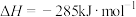 |
B.O=O的键能(气态分子中1mol化学键解离成气态原子所吸收的能量)为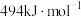 |
C. 的生成热: 的生成热: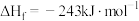 |
D. 燃烧热的热化学方程式为: 燃烧热的热化学方程式为: 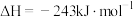 |
您最近一年使用:0次