解题方法
1 . 四水甲酸铜(II)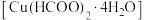 常用作催化剂、化学试剂,应用于电镀等领域。实验室可以用碱式碳酸铜
常用作催化剂、化学试剂,应用于电镀等领域。实验室可以用碱式碳酸铜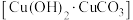 与甲酸反应来制备。
与甲酸反应来制备。
已知:①四水甲酸铜(II)为蓝色晶体,易溶于水,难溶于醇及大多数有机物。
②碱式碳酸铜和碳酸氢钠在水溶液中比固态时更易分解。
实验室制备四水甲酸铜(II)的步骤如下:
I.称取一定量 和
和 ,充分研细并混合均匀。
,充分研细并混合均匀。
II.将I中所得混合物加入到100mL接近沸腾的蒸馏水中,继续加热至接近沸腾状态数分钟。
III.静置溶液澄清后,用倾析法分离得到沉淀,用蒸馏水洗涤,干燥。
IV.将III中所得产品放入如图装置的三颈烧瓶中,加入约20mL蒸馏水,加热搅拌至50℃左右。
V.向三颈烧瓶中加入甲酸,反应结束后趁热过滤。
VI.经过一系列操作得到四水甲酸铜(II)产品。
回答下列问题:___________ 。
(2)步骤II中发生反应的化学方程式为___________ 。
实际取用的硫酸铜和碳酸氢钠的物质的量之比小于1:2,原因一是过量的碳酸氢钠用于保持溶液呈碱性,二是___________ 。
(3)步骤III中检验沉淀已洗净的方法是___________ 。
(4)步骤VI中的一系列操作中减压过滤的优点是___________ 。
(5)测定产品中四水甲酸铜(II)(M=226g/mol)的含量:准确称取ag产品配成100mL溶液,取25.00mL于锥形瓶中,消除干扰离子后,用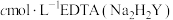 标准溶液滴定至终点,平均消耗EDTA溶液bmL。(已知滴定反应为:
标准溶液滴定至终点,平均消耗EDTA溶液bmL。(已知滴定反应为: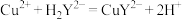 )则产品中四水甲酸铜(II)的质量分数为
)则产品中四水甲酸铜(II)的质量分数为___________ (用含a、b、c的代数式表示)。
(6)如果将甲酸铜(II) 、对苯二甲酸(
、对苯二甲酸(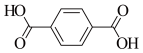 )、乙醇混合溶液长时间放置,将析出一种晶体X(晶胞结构如图),甲酸根全部被交换到溶液中。
)、乙醇混合溶液长时间放置,将析出一种晶体X(晶胞结构如图),甲酸根全部被交换到溶液中。___________ ;若1molX晶胞的质量为456g,实验表明,91.2mg晶体X可吸收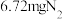 ,所得晶体中Cu:N个数比为1:
,所得晶体中Cu:N个数比为1:___________ 。
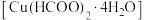 常用作催化剂、化学试剂,应用于电镀等领域。实验室可以用碱式碳酸铜
常用作催化剂、化学试剂,应用于电镀等领域。实验室可以用碱式碳酸铜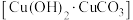 与甲酸反应来制备。
与甲酸反应来制备。已知:①四水甲酸铜(II)为蓝色晶体,易溶于水,难溶于醇及大多数有机物。
②碱式碳酸铜和碳酸氢钠在水溶液中比固态时更易分解。
实验室制备四水甲酸铜(II)的步骤如下:
I.称取一定量
 和
和 ,充分研细并混合均匀。
,充分研细并混合均匀。II.将I中所得混合物加入到100mL接近沸腾的蒸馏水中,继续加热至接近沸腾状态数分钟。
III.静置溶液澄清后,用倾析法分离得到沉淀,用蒸馏水洗涤,干燥。
IV.将III中所得产品放入如图装置的三颈烧瓶中,加入约20mL蒸馏水,加热搅拌至50℃左右。
V.向三颈烧瓶中加入甲酸,反应结束后趁热过滤。
VI.经过一系列操作得到四水甲酸铜(II)产品。
回答下列问题:

(2)步骤II中发生反应的化学方程式为
实际取用的硫酸铜和碳酸氢钠的物质的量之比小于1:2,原因一是过量的碳酸氢钠用于保持溶液呈碱性,二是
(3)步骤III中检验沉淀已洗净的方法是
(4)步骤VI中的一系列操作中减压过滤的优点是
(5)测定产品中四水甲酸铜(II)(M=226g/mol)的含量:准确称取ag产品配成100mL溶液,取25.00mL于锥形瓶中,消除干扰离子后,用
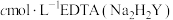 标准溶液滴定至终点,平均消耗EDTA溶液bmL。(已知滴定反应为:
标准溶液滴定至终点,平均消耗EDTA溶液bmL。(已知滴定反应为: )则产品中四水甲酸铜(II)的质量分数为
)则产品中四水甲酸铜(II)的质量分数为(6)如果将甲酸铜(II)
 、对苯二甲酸(
、对苯二甲酸( )、乙醇混合溶液长时间放置,将析出一种晶体X(晶胞结构如图),甲酸根全部被交换到溶液中。
)、乙醇混合溶液长时间放置,将析出一种晶体X(晶胞结构如图),甲酸根全部被交换到溶液中。
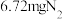 ,所得晶体中Cu:N个数比为1:
,所得晶体中Cu:N个数比为1:
您最近一年使用:0次
2024-03-27更新
|
551次组卷
|
3卷引用:2024届辽宁省协作校高三下学期一模大联考化学试题
解题方法
2 . 实验室制备三氯化六氨合钴(Ⅲ){[ Co(NH3)6]Cl3 }的装置如图1所示。
实验步骤:在三颈烧瓶中加入活性炭(作催化剂)、CoCl2和NH4Cl混合溶液,滴入浓氨水,充分反应后,再滴入双氧水,且水浴控温在55℃左右,反应结束后,将反应混合物趁热过滤,待滤液冷却后加入适量浓盐酸,冰水冷却抽滤、乙醇洗涤、干燥,得到[ Co(NH3)6]Cl3晶体。已知:[ Co(NH3)6]2+具有CoCl2和NH4Cl较强还原性,Co2+不易被氧化, 。
。
(1)仪器a的名称是_______________ ,仪器c中无水CaCl2的作用是_______________ 。
(2)先加入浓氨水的目的是_______________ ,水浴控制温度为55℃的原因是_______________ 。
(3)CoCl2制备[ Co(NH3)6]Cl3的化学方程式为_______________ 。
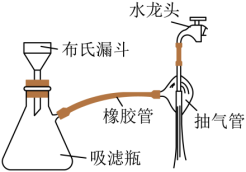
(4)待滤液冷却后加入适量浓盐酸的作用是_______________ ,抽滤采用如图2的装置,抽滤的优点是_______________ 。
(5)为测定产品中钴的含量,进行下列实验:
I.称取4.0g产品,加入足量NaOH溶液蒸出NH3,再加入稀硫酸,使[ Co(NH3)6]Cl3全部转化为Co3+,然后将溶液配制成250mL,取25.00mL于锥形瓶,加入过量KI溶液(将Co3+还原成Co2+),用0.1000mol.L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液13.10mL。(已知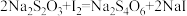 )
)
Ⅱ.另取与步骤I中等量的KI溶液于锥形瓶中,用上述标准溶液进行滴定,消耗Na2S2O3标准溶液1.10mL。
①样品中钴元素的质量分数为_______________ %。
②若步骤Ⅱ滴定前读数准确,滴定后的俯视读数,测定结果将_______________ (填“偏大”“偏小”或“不变”)。
实验步骤:在三颈烧瓶中加入活性炭(作催化剂)、CoCl2和NH4Cl混合溶液,滴入浓氨水,充分反应后,再滴入双氧水,且水浴控温在55℃左右,反应结束后,将反应混合物趁热过滤,待滤液冷却后加入适量浓盐酸,冰水冷却抽滤、乙醇洗涤、干燥,得到[ Co(NH3)6]Cl3晶体。已知:[ Co(NH3)6]2+具有CoCl2和NH4Cl较强还原性,Co2+不易被氧化,
 。
。
(1)仪器a的名称是
(2)先加入浓氨水的目的是
(3)CoCl2制备[ Co(NH3)6]Cl3的化学方程式为
(4)待滤液冷却后加入适量浓盐酸的作用是
(5)为测定产品中钴的含量,进行下列实验:
I.称取4.0g产品,加入足量NaOH溶液蒸出NH3,再加入稀硫酸,使[ Co(NH3)6]Cl3全部转化为Co3+,然后将溶液配制成250mL,取25.00mL于锥形瓶,加入过量KI溶液(将Co3+还原成Co2+),用0.1000mol.L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液13.10mL。(已知
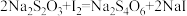 )
)Ⅱ.另取与步骤I中等量的KI溶液于锥形瓶中,用上述标准溶液进行滴定,消耗Na2S2O3标准溶液1.10mL。
①样品中钴元素的质量分数为
②若步骤Ⅱ滴定前读数准确,滴定后的俯视读数,测定结果将
您最近一年使用:0次
名校
3 . 某同学为测定 和
和 混合粉末中
混合粉末中 的含量。将
的含量。将 和
和 混合粉末加入
混合粉末加入 的稀硝酸中,得到
的稀硝酸中,得到 气体
气体 (标准状况下),忽略溶液体积的变化。下列有关说法正确的是
(标准状况下),忽略溶液体积的变化。下列有关说法正确的是
 和
和 混合粉末中
混合粉末中 的含量。将
的含量。将 和
和 混合粉末加入
混合粉末加入 的稀硝酸中,得到
的稀硝酸中,得到 气体
气体 (标准状况下),忽略溶液体积的变化。下列有关说法正确的是
(标准状况下),忽略溶液体积的变化。下列有关说法正确的是| A.反应后有固体剩余 | B.反应后的溶液中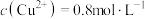 |
C. 单质在混合粉末中的质量分数约为 单质在混合粉末中的质量分数约为 | D.在反应后的溶液中加入足量铁粉,可置换出 |
您最近一年使用:0次
2024-04-11更新
|
172次组卷
|
4卷引用:辽宁省部分高中2023-2024学年高一下学期4月月考化学试题
辽宁省部分高中2023-2024学年高一下学期4月月考化学试题吉林省白山市抚松县第一中学2023-2024学年高一下学期4月月考化学试题(已下线)第二章 化学计量及应用(测试)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)山东省烟台市龙口第一中学东校2023-2024学年高二下学期6月月考化学试题
名校
解题方法
4 . 氧钒(Ⅳ)碱式碳酸铵晶体{(NH4)5[(VO)6(CO3)4(OH)9]•10H2O}是制备多种含钒产品和催化剂的基础原料和前驱体。已知:①氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇;②VO2+有较强还原性,易被氧化。实验室以V2O5为原料制备该晶体的流程如图:
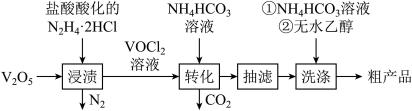
请回答下列问题:
(1)“浸渍”时反应的化学方程式为_______ 。
(2)“转化”时需要在CO2氛围中进行的原因是_______ 。
(3)“转化”可在下图装置中进行:
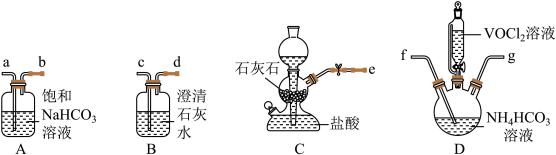
①上述装置连接的合理顺序为e→_______ (按气流方向,用小写字母表示)。
②写出装置D中生成氧钒(Ⅳ)碱式碳酸铵晶体的化学方程式_______ 。
(4)“洗涤”时用饱和NH4HCO3溶液洗涤晶体,检验晶体已洗涤干净的操作是_______ 。
(5)为测定粗产品中钒元素的含量,称取1.0g粗产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后加入0.01mol/LKMnO4溶液至稍过量,充分反应后继续滴加2%的NaNO2溶液至稍过量,再用尿素除去过量的NaNO2,滴入几滴铁氰化钾K3[Fe(CN)6]溶液,最后用0.2mol/L(NH4)2Fe(SO4)2标准溶液滴定,滴定终点消耗标准溶液的体积为20.00mL。(已知粗产品中杂质不含钒,也不参与反应;滴定反应为VO +Fe2++2H+=VO2++Fe3++H2O)
+Fe2++2H+=VO2++Fe3++H2O)
①滴定终点时的现象为_______ 。
②粗产品中钒元素的质量分数为_______ %。

请回答下列问题:
(1)“浸渍”时反应的化学方程式为
(2)“转化”时需要在CO2氛围中进行的原因是
(3)“转化”可在下图装置中进行:

①上述装置连接的合理顺序为e→
②写出装置D中生成氧钒(Ⅳ)碱式碳酸铵晶体的化学方程式
(4)“洗涤”时用饱和NH4HCO3溶液洗涤晶体,检验晶体已洗涤干净的操作是
(5)为测定粗产品中钒元素的含量,称取1.0g粗产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后加入0.01mol/LKMnO4溶液至稍过量,充分反应后继续滴加2%的NaNO2溶液至稍过量,再用尿素除去过量的NaNO2,滴入几滴铁氰化钾K3[Fe(CN)6]溶液,最后用0.2mol/L(NH4)2Fe(SO4)2标准溶液滴定,滴定终点消耗标准溶液的体积为20.00mL。(已知粗产品中杂质不含钒,也不参与反应;滴定反应为VO
 +Fe2++2H+=VO2++Fe3++H2O)
+Fe2++2H+=VO2++Fe3++H2O)①滴定终点时的现象为
②粗产品中钒元素的质量分数为
您最近一年使用:0次
名校
解题方法
5 . 对氨基苯磺酸是制备药物的重要中间体,可用苯胺(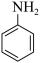 )、浓硫酸为原料合成。实验流程、装置示意图如下。
)、浓硫酸为原料合成。实验流程、装置示意图如下。
回答下列问题:
(1)仪器A的名称___________ 。
(2)写出该反应的化学方程式___________ 。
(3)步骤1中加热方式是___________ (填“水浴”、“油浴”或“直接加热”)。步骤1加入浓硫酸时,为防止温度过高致苯胺被氧化,可采取的措施有___________ 。
(4)下列有关说法正确的是________
(5)对氨基苯磺酸粗产品因含杂质而显色,可用重结晶法进行提纯。从下列选项中选择合理操作并排序:______
(___________)→(___________)→(___________)→(___________)→过滤→洗涤→干燥。
a.沸水溶解 b.过滤 c.趁热过滤 d.蒸发结晶 e.冷却结晶 f.加入活性炭
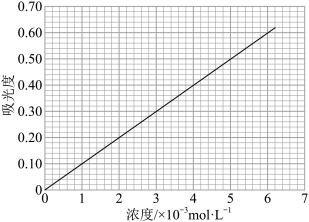
(6)对氨基苯磺酸与对二甲氨基苯甲醛在一定条件下可以发生显色反应。利用这一原理,用分光光度法可以测定对氨基苯磺酸的含量,吸光度与对氨基苯磺酸浓度关系如图所示。___________ 。
 )、浓硫酸为原料合成。实验流程、装置示意图如下。
)、浓硫酸为原料合成。实验流程、装置示意图如下。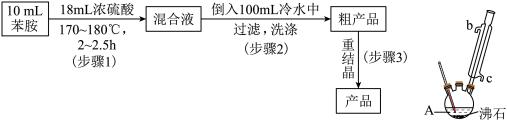
| 名称 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 苯胺 | 93 |  | 184 | 微溶于水,溶于乙醇、乙醚等有机溶剂 |
| 对氨基苯磺酸 | 173 | 288 | —— | 微溶于冷水,溶于热水,不溶于乙醇、乙醚等有机溶剂 |
(1)仪器A的名称
(2)写出该反应的化学方程式
(3)步骤1中加热方式是
(4)下列有关说法正确的是________
| A.反应产物中可能有邻氨基苯磺酸 |
| B.冷凝管进出水方向是b进a出 |
| C.如果加热后发现忘加沸石,应立刻补加 |
| D.步骤2将混合液倒入盛有冷水烧杯中,用玻璃棒摩擦器壁可促使晶体析出 |
(___________)→(___________)→(___________)→(___________)→过滤→洗涤→干燥。
a.沸水溶解 b.过滤 c.趁热过滤 d.蒸发结晶 e.冷却结晶 f.加入活性炭
(6)对氨基苯磺酸与对二甲氨基苯甲醛在一定条件下可以发生显色反应。利用这一原理,用分光光度法可以测定对氨基苯磺酸的含量,吸光度与对氨基苯磺酸浓度关系如图所示。
您最近一年使用:0次
2023-07-11更新
|
185次组卷
|
3卷引用:辽宁省实验中学2023-2024学年高二下学期第一次月考化学试题
名校
6 . 碳酸钐Sm2(CO3)3为难溶于水的白色粉末,可用于治疗高磷酸盐血症。
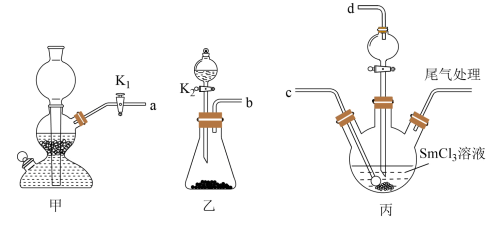
回答下列问题:
I.实验室利用NH3和CO2通入SmCl3溶液中制备水合碳酸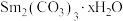 :
:
(1)装置的连接顺序是a→___________ ,___________ ←b(填接口字母)
(2)生成水合碳酸钐的化学方程式为___________ ;
(3)若氮气过量,溶液碱性太强会生成副产物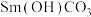 ,减少该副产物生成的操作是
,减少该副产物生成的操作是___________ 。
Ⅱ.碳酸钐质量分数的测定(已知:EDTA可以和许多金属离子形成配合物,且在不同的pH下配合物的稳定性不同):
准确称取10.00产品试样,溶于10.00ml稀盐酸中,加入10.00mlNH3-NH4Cl缓冲溶液,加入0.2g紫脲酸铵混合指示剂,用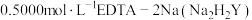 标准溶液滴定至呈蓝紫色(
标准溶液滴定至呈蓝紫色(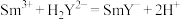 ),消耗EDTA-2Na溶液40.00mL。
),消耗EDTA-2Na溶液40.00mL。
(4)若滴定终点俯视读数,测得碳酸钐的质量分数会___________ (偏大、偏小、不影响)。滴定之前滴定管内没有气泡,滴定结束后产生气泡,则测得碳酸钐的质量分数会___________ (偏大、偏小、不影响),加入NH3-NH4Cl缓冲溶液的作用是___________ 。
Ⅲ.测定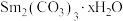 中结晶水的含量:
中结晶水的含量:
(5)将装置A称重,记为m1g。将提纯后的样品装入装置A中,再次将装置A称重,记为m2g,将装有试剂的装置C称重,记为m3g。按下图连接好装置进行实验。

①打开 、
、 和
和 ,缓缓通入
,缓缓通入 ;
;
②数分钟后关闭___________ (填写止水夹代号,下同),打开___________ ,点燃酒精喷灯,加热 中样品:
中样品:
③一段时间后,熄灭酒精灯,打开K1,通入N2数分钟后,冷却到室温,关闭K1和K2,称量装置A,重复上述操作步骤,直至装置A恒重,记为m4g(此时装置A中为Sm2O3)。称重装置C,记为m5g。则提纯后的样品中含结晶水的质量为___________ g(列出计算式)

回答下列问题:
I.实验室利用NH3和CO2通入SmCl3溶液中制备水合碳酸
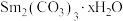 :
:(1)装置的连接顺序是a→
(2)生成水合碳酸钐的化学方程式为
(3)若氮气过量,溶液碱性太强会生成副产物
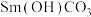 ,减少该副产物生成的操作是
,减少该副产物生成的操作是Ⅱ.碳酸钐质量分数的测定(已知:EDTA可以和许多金属离子形成配合物,且在不同的pH下配合物的稳定性不同):
准确称取10.00产品试样,溶于10.00ml稀盐酸中,加入10.00mlNH3-NH4Cl缓冲溶液,加入0.2g紫脲酸铵混合指示剂,用
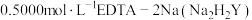 标准溶液滴定至呈蓝紫色(
标准溶液滴定至呈蓝紫色(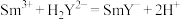 ),消耗EDTA-2Na溶液40.00mL。
),消耗EDTA-2Na溶液40.00mL。(4)若滴定终点俯视读数,测得碳酸钐的质量分数会
Ⅲ.测定
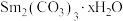 中结晶水的含量:
中结晶水的含量:(5)将装置A称重,记为m1g。将提纯后的样品装入装置A中,再次将装置A称重,记为m2g,将装有试剂的装置C称重,记为m3g。按下图连接好装置进行实验。

①打开
 、
、 和
和 ,缓缓通入
,缓缓通入 ;
;②数分钟后关闭
 中样品:
中样品:③一段时间后,熄灭酒精灯,打开K1,通入N2数分钟后,冷却到室温,关闭K1和K2,称量装置A,重复上述操作步骤,直至装置A恒重,记为m4g(此时装置A中为Sm2O3)。称重装置C,记为m5g。则提纯后的样品中含结晶水的质量为
您最近一年使用:0次
名校
解题方法
7 . 二氧化钒(VO2)是一种新型热敏材料,实验室以V2O5为原料合成用于制备VO2的氧钒(Ⅳ)碱式碳酸铵晶体{化学式为(NH4)5[(VO)6(CO3)4(OH)9]•10H2O},过程如图:
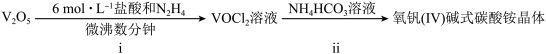
已知:+4价钒在弱酸性条件下具有还原性,VO2+能被O2氧化。
回答下列问题:
(1)步骤ⅰ中生成VOCl2同时生成N2的化学方程式为______ 。
(2)步骤ii可用如图仪器组装完成。
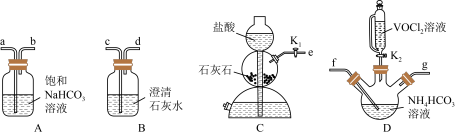
①上述装置从左到右的连接顺序为_______ (用各接口字母表示)。
②B装置的作用是_______ 。
③反应结束后,将三颈烧瓶置于CO2保护下的干燥器中,静置后可得到紫红色晶体,然后抽滤,先用饱和NH4HCO3溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。用饱和NH4HCO3溶液洗涤除去的阴离子主要是_______ (填阴离子的电子式)。
(3)测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品中钒的含量。实验步骤如图:
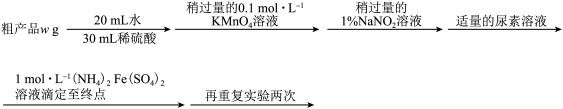
消耗滴定液的体积如表:
滴定反应为VO +Fe3++2H+=VO2++Fe2++H2O。
+Fe3++2H+=VO2++Fe2++H2O。
①滴定时,向锥形瓶中加入几滴_______ (填化学式)溶液作指示剂。
②粗产品中钒的质量分数为_______ %。
③结合上述实验步骤,分析选择尿素溶液的原因_______ 。
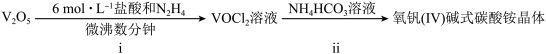
已知:+4价钒在弱酸性条件下具有还原性,VO2+能被O2氧化。
回答下列问题:
(1)步骤ⅰ中生成VOCl2同时生成N2的化学方程式为
(2)步骤ii可用如图仪器组装完成。

①上述装置从左到右的连接顺序为
②B装置的作用是
③反应结束后,将三颈烧瓶置于CO2保护下的干燥器中,静置后可得到紫红色晶体,然后抽滤,先用饱和NH4HCO3溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。用饱和NH4HCO3溶液洗涤除去的阴离子主要是
(3)测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品中钒的含量。实验步骤如图:

消耗滴定液的体积如表:
| 实验次数 | 滴定前读数/mL | 滴定后读数/mL |
| 1 | 0.00 | 19.99 |
| 2 | 1.10 | 21.10 |
| 3 | 1.56 | 21.57 |
 +Fe3++2H+=VO2++Fe2++H2O。
+Fe3++2H+=VO2++Fe2++H2O。①滴定时,向锥形瓶中加入几滴
②粗产品中钒的质量分数为
③结合上述实验步骤,分析选择尿素溶液的原因
您最近一年使用:0次
名校
8 . 钛是航空、军工、电力等领域的重要原材料。地壳中的含钛矿石之一是金红石( ),其是冶炼钛的重要原料。生产钛的工艺流程如图:
),其是冶炼钛的重要原料。生产钛的工艺流程如图:

已知:①常温下,钛既不与常见非金属单质反应,也不与强酸反应;
②加热时,钛可以和常见的非金属单质反应。
(1)在反应I中:
①下列有关CO的说法正确的是_______ (填标号)。
A.属于酸性氧化物 B.摩尔质量为28 C.为可燃性气体 D.具有还原性
②反应I的化学方程式为_______ ,该反应中氧化剂与还原剂的质量之比为_______ 。
③每转移0.2mol电子,同时生成CO的体积为_______ (标准状况下)。
(2)在反应II中:
①氩气的作用为_______ 。
②该反应的基本反应类型为_______ 。
(3)为了测定反应II制得的金属钛(杂质仅含Mg)中的钛元素含量。常温下,取mg反应II制得的金属钛置于烧杯中,往烧杯中逐滴滴入物质的量浓度为 的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:
的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:
①上述反应的离子方程式为_______ 。
②金属钛的质量分数为_______ (用含m、c、V的代数式表示)。
 ),其是冶炼钛的重要原料。生产钛的工艺流程如图:
),其是冶炼钛的重要原料。生产钛的工艺流程如图:
已知:①常温下,钛既不与常见非金属单质反应,也不与强酸反应;
②加热时,钛可以和常见的非金属单质反应。
(1)在反应I中:
①下列有关CO的说法正确的是
A.属于酸性氧化物 B.摩尔质量为28 C.为可燃性气体 D.具有还原性
②反应I的化学方程式为
③每转移0.2mol电子,同时生成CO的体积为
(2)在反应II中:
①氩气的作用为
②该反应的基本反应类型为
(3)为了测定反应II制得的金属钛(杂质仅含Mg)中的钛元素含量。常温下,取mg反应II制得的金属钛置于烧杯中,往烧杯中逐滴滴入物质的量浓度为
 的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:
的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:①上述反应的离子方程式为
②金属钛的质量分数为
您最近一年使用:0次
2023-01-11更新
|
290次组卷
|
7卷引用:辽宁省辽西联合校2023-2024学年高三上学期期中考试化学试题
名校
9 . 近年来,人们对微生物的氮转化进行了深入研究,将其归纳为如图1所示过程。请回答下列问题:
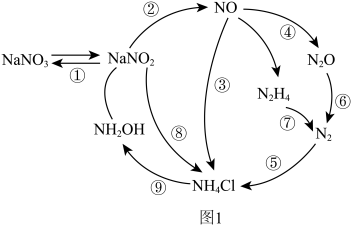
(1)N2的电子式为_____ ;羟胺(NH2OH)的结构式为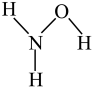 ,属于
,属于_____ (填“离子”或“共价”)化合物。
(2)笑气(N2O)可用作医用麻醉剂、制冷剂,实验室通过加热NH4NO3分解制备N2O,只有两种产物,写出该反应的化学方程式:_____ 。
(3)图1转化过程中具有固氮功能的是_____ (填标号)。
(4)实验室常用氢氧化钙和氯化铵制备氨气,反应装置如图2所示。
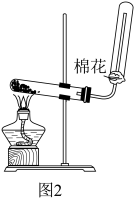
I.写出该反应的化学方程式:_____ 。
Ⅱ.棉花的作用为_____ 。
(5)NaNO2和食盐性状相似,社会上曾多次发生将NaNO2误当食盐食用的事件。可用0.1mol•L-1酸性KMnO4溶液来测定某亚硝酸钠样品中NaNO2的含量(假设杂质不与KMnO4溶液反应),进行三次实验,每次取ag样品,消耗酸性KMnO4溶液的平均体积为20.00mL。测定原理为NO +MnO
+MnO +H+→NO
+H+→NO +Mn2++H2O。
+Mn2++H2O。
I.请配平该离子方程式:_____ 。
Ⅱ.NaNO2的质量分数为_____ %。

(1)N2的电子式为
 ,属于
,属于(2)笑气(N2O)可用作医用麻醉剂、制冷剂,实验室通过加热NH4NO3分解制备N2O,只有两种产物,写出该反应的化学方程式:
(3)图1转化过程中具有固氮功能的是
(4)实验室常用氢氧化钙和氯化铵制备氨气,反应装置如图2所示。

I.写出该反应的化学方程式:
Ⅱ.棉花的作用为
(5)NaNO2和食盐性状相似,社会上曾多次发生将NaNO2误当食盐食用的事件。可用0.1mol•L-1酸性KMnO4溶液来测定某亚硝酸钠样品中NaNO2的含量(假设杂质不与KMnO4溶液反应),进行三次实验,每次取ag样品,消耗酸性KMnO4溶液的平均体积为20.00mL。测定原理为NO
 +MnO
+MnO +H+→NO
+H+→NO +Mn2++H2O。
+Mn2++H2O。I.请配平该离子方程式:
Ⅱ.NaNO2的质量分数为
您最近一年使用:0次
2023-04-18更新
|
406次组卷
|
3卷引用:辽宁省部分学校联考2022-2023学年高一下学期4月月考化学试题
名校
10 . 现有mg含有Na2O杂质的Na2O2样品,某同学在实验室用如图装置(部分夹持仪器已省略)测定其杂质含量:
(1)装置A中反应的离子方程式为_____ ;其中CaCO3属于____ (填“酸”“碱”或“盐”)。
(2)图中有一处明显错误,请指出并改正:_____ 。
(3)装置B的作用是____ ;装置D的作用是_____ ;若无装置D,样品中杂质的质量分数____ (填“偏高”“偏低”或“无影响”)。
(4)写出装置C中Na2O2和CO2反应的化学方程式:_____ 。
(5)实验结束后,装置F中水的体积为VmL,已知氧气的密度为1.43g·L-1,样品的质量分数为____ (用含m、V的代数式表示,列出计算式即可)。

(1)装置A中反应的离子方程式为
(2)图中有一处明显错误,请指出并改正:
(3)装置B的作用是
(4)写出装置C中Na2O2和CO2反应的化学方程式:
(5)实验结束后,装置F中水的体积为VmL,已知氧气的密度为1.43g·L-1,样品的质量分数为
您最近一年使用:0次
2022-09-13更新
|
556次组卷
|
3卷引用:辽宁省朝阳市凌源市2021-2022学年高一上学期期末考试化学试题



