1 . 三草酸合铁( )酸钾晶体
)酸钾晶体 是制备负载型活性铁催化剂的主要原料。实验室欲制备少量三草酸合铁(
是制备负载型活性铁催化剂的主要原料。实验室欲制备少量三草酸合铁( )酸钾晶体。
)酸钾晶体。
已知: 为翠绿色晶体,难溶于乙醇;0℃时在水中溶解度为4.7g,100℃时溶解度为117.7g。
为翠绿色晶体,难溶于乙醇;0℃时在水中溶解度为4.7g,100℃时溶解度为117.7g。
 .制备
.制备 :称取2.0g莫尔盐
:称取2.0g莫尔盐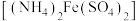 于锥形瓶中,溶于水,滴加足量
于锥形瓶中,溶于水,滴加足量 ,加热并搅拌。当变成红褐色后,再煮沸十分钟,冷却后,过滤、洗涤。
,加热并搅拌。当变成红褐色后,再煮沸十分钟,冷却后,过滤、洗涤。
 .制备草酸氢钾:称取
.制备草酸氢钾:称取 溶于20mL水中,加入
溶于20mL水中,加入 ,反应生成
,反应生成 。
。
 .制备三草酸合铁(
.制备三草酸合铁( )酸钾晶体。步骤如图:
)酸钾晶体。步骤如图:
(1) 中制备
中制备 的离子反应方程式为
的离子反应方程式为___________ 。
(2) 中制备三草酸合铁(
中制备三草酸合铁( )酸钾晶体
)酸钾晶体
①步骤1装置中仪器a的名称为___________ 。
②步骤2的操作名称是___________ ,步骤3采用冰水冷却的目的为___________ 。
③过滤后需要用乙醇溶液洗涤,其优点是___________ 。
(3)三草酸合铁( )酸钾晶体具有光敏性,在强光下分解生成
)酸钾晶体具有光敏性,在强光下分解生成 、
、 和
和 等,该反应的化学方程式为
等,该反应的化学方程式为___________ 。
(4)产品纯度的测定
称取ag晶体粗品溶于100mL水中配成溶液,取20mL溶液于锥形瓶中,用 的酸性
的酸性 ,标准溶液进行滴定(已知
,标准溶液进行滴定(已知 被还原为
被还原为 且粗品中的杂质不参与反应),进行了三次平行实验,达到滴定终点时平均消枆标准溶液VmL。
且粗品中的杂质不参与反应),进行了三次平行实验,达到滴定终点时平均消枆标准溶液VmL。
①所得粗品的纯度为___________ %(用含V、c、a的代数式表示)。
②下列情况会导致产品纯度测定结果偏高的有___________ 。
A.产品中含有
B.滴定终点读数时滴定管尖嘴有气泡(滴定前无气泡)
C.盛装酸性 溶液的滴定管未润洗
溶液的滴定管未润洗
D.产品干燥不充分
 )酸钾晶体
)酸钾晶体 是制备负载型活性铁催化剂的主要原料。实验室欲制备少量三草酸合铁(
是制备负载型活性铁催化剂的主要原料。实验室欲制备少量三草酸合铁( )酸钾晶体。
)酸钾晶体。已知:
 为翠绿色晶体,难溶于乙醇;0℃时在水中溶解度为4.7g,100℃时溶解度为117.7g。
为翠绿色晶体,难溶于乙醇;0℃时在水中溶解度为4.7g,100℃时溶解度为117.7g。 .制备
.制备 :称取2.0g莫尔盐
:称取2.0g莫尔盐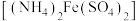 于锥形瓶中,溶于水,滴加足量
于锥形瓶中,溶于水,滴加足量 ,加热并搅拌。当变成红褐色后,再煮沸十分钟,冷却后,过滤、洗涤。
,加热并搅拌。当变成红褐色后,再煮沸十分钟,冷却后,过滤、洗涤。 .制备草酸氢钾:称取
.制备草酸氢钾:称取 溶于20mL水中,加入
溶于20mL水中,加入 ,反应生成
,反应生成 。
。 .制备三草酸合铁(
.制备三草酸合铁( )酸钾晶体。步骤如图:
)酸钾晶体。步骤如图:
(1)
 中制备
中制备 的离子反应方程式为
的离子反应方程式为(2)
 中制备三草酸合铁(
中制备三草酸合铁( )酸钾晶体
)酸钾晶体①步骤1装置中仪器a的名称为
②步骤2的操作名称是
③过滤后需要用乙醇溶液洗涤,其优点是
(3)三草酸合铁(
 )酸钾晶体具有光敏性,在强光下分解生成
)酸钾晶体具有光敏性,在强光下分解生成 、
、 和
和 等,该反应的化学方程式为
等,该反应的化学方程式为(4)产品纯度的测定
称取ag晶体粗品溶于100mL水中配成溶液,取20mL溶液于锥形瓶中,用
 的酸性
的酸性 ,标准溶液进行滴定(已知
,标准溶液进行滴定(已知 被还原为
被还原为 且粗品中的杂质不参与反应),进行了三次平行实验,达到滴定终点时平均消枆标准溶液VmL。
且粗品中的杂质不参与反应),进行了三次平行实验,达到滴定终点时平均消枆标准溶液VmL。①所得粗品的纯度为
②下列情况会导致产品纯度测定结果偏高的有
A.产品中含有

B.滴定终点读数时滴定管尖嘴有气泡(滴定前无气泡)
C.盛装酸性
 溶液的滴定管未润洗
溶液的滴定管未润洗D.产品干燥不充分
您最近一年使用:0次
2 . 以相应的卤代酸酯为原料,利用Gabriel法合成天冬氨酸,其中一种中间产物的结构如图所示,下列有关该有机物的说法正确的是

| A.存在分子中含有两个苯环且可发生银镜反应的同分异构体 |
| B.分子中不含有手性碳原子 |
C.1mol该有机物最多与7mol的 发生加成反应 发生加成反应 |
| D.分子中所有的碳原子共平面 |
您最近一年使用:0次
3 . 化合物K可用于治疗糖尿病,其合成路线如下:
回答下列问题:
(1)1mol A能与含2mol 的水溶液反应生成气体,则A的结构简式为
的水溶液反应生成气体,则A的结构简式为_______ 。
(2)由A生成B的反应类型是_______ ,H中氮原子的杂化方式为_______ 。
(3)C的化学名称是_______ ,K中官能团的名称为_______ 。
(4)E的结构简式为_______ 。
(5)反应J+F→K的化学方程式为_______ 。
(6)符合下列条件的G的同分异构体共有_______ 种。
①含有苯环;
②能发生水解反应和银镜反应;
③遇 溶液显紫色。
溶液显紫色。
其中,核磁共振氢谱显示5组峰,且峰面积比为2∶2∶2∶1∶1的同分异构体的结构简式为______________ 。
(7)邻苯二甲酰亚胺( )是合成高分子的重要材料。参照上述合成路线,写出以邻二甲苯为原料制备邻苯二甲酰亚胺的合成路线(无机试剂任选):
)是合成高分子的重要材料。参照上述合成路线,写出以邻二甲苯为原料制备邻苯二甲酰亚胺的合成路线(无机试剂任选):______________ 。

ⅰ.

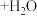 。
。
ⅱ.

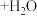 。
。
ⅲ.

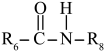
 。
。
回答下列问题:
(1)1mol A能与含2mol
 的水溶液反应生成气体,则A的结构简式为
的水溶液反应生成气体,则A的结构简式为(2)由A生成B的反应类型是
(3)C的化学名称是
(4)E的结构简式为
(5)反应J+F→K的化学方程式为
(6)符合下列条件的G的同分异构体共有
①含有苯环;
②能发生水解反应和银镜反应;
③遇
 溶液显紫色。
溶液显紫色。其中,核磁共振氢谱显示5组峰,且峰面积比为2∶2∶2∶1∶1的同分异构体的结构简式为
(7)邻苯二甲酰亚胺(
 )是合成高分子的重要材料。参照上述合成路线,写出以邻二甲苯为原料制备邻苯二甲酰亚胺的合成路线(无机试剂任选):
)是合成高分子的重要材料。参照上述合成路线,写出以邻二甲苯为原料制备邻苯二甲酰亚胺的合成路线(无机试剂任选):
您最近一年使用:0次
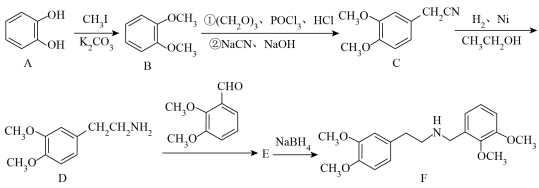
4 . 延胡索乙素具有镇痛及催眠作用,其中间体F的合成路线如图。回答下列问题: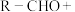 H2NR′
H2NR′ NR′(R为烃基,R′为烃基或H)
NR′(R为烃基,R′为烃基或H)_______ ,A→B的反应类型为_______ 。
(2)已知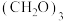 为六元环结构,核磁共振氢谱显示有1组峰,则其结构简式为
为六元环结构,核磁共振氢谱显示有1组峰,则其结构简式为_______ 。
(3)D中官能团的名称为_______ ,D中碳原子的杂化方式为_______ 。
(4)反应C→D的化学方程式为_______ 。
(5)已知化合物M是 的芳香族同分异构体,则符合下列条件的M的结构有
的芳香族同分异构体,则符合下列条件的M的结构有_____ 种。
①苯环上只有2个取代基;
②能与 溶液发生显色反应;
溶液发生显色反应;
③能发生水解反应。
(6)参照上述合成路线,以苯和乙醇为原料,设计合成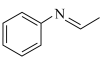 的路线:
的路线:_______ 。(无机试剂任选)
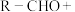 H2NR′
H2NR′ NR′(R为烃基,R′为烃基或H)
NR′(R为烃基,R′为烃基或H)②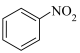


(2)已知
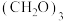 为六元环结构,核磁共振氢谱显示有1组峰,则其结构简式为
为六元环结构,核磁共振氢谱显示有1组峰,则其结构简式为(3)D中官能团的名称为
(4)反应C→D的化学方程式为
(5)已知化合物M是
 的芳香族同分异构体,则符合下列条件的M的结构有
的芳香族同分异构体,则符合下列条件的M的结构有①苯环上只有2个取代基;
②能与
 溶液发生显色反应;
溶液发生显色反应;③能发生水解反应。
(6)参照上述合成路线,以苯和乙醇为原料,设计合成
 的路线:
的路线:
您最近一年使用:0次
5 . 氧钒(Ⅳ)碱式碳酸铵晶体{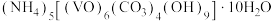 }的制备及纯度分析步骤如下。
}的制备及纯度分析步骤如下。
Ⅰ.制备氧钒(Ⅳ)碱式碳酸铵晶体的流程如下:
 碱式碳酸铵晶体
碱式碳酸铵晶体
其中,步骤ⅱ可通过如图装置完成。
实验步骤: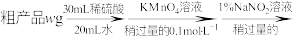
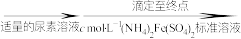 再重复实验两次。
再重复实验两次。
已知:①氧钒(Ⅳ)碱式碳酸铵晶体难溶于水,
②+4价钒在弱酸性条件下具有还原性。
③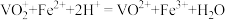 。
。
④在该实验条件下, 与尿素不反应。
与尿素不反应。
回答下列问题:
(1)从原子结构角度解释+5价钒较稳定的原因:_______ 。
(2)步骤ⅰ中 和
和 反应得到的产物之一是一种无毒无害的气体,该反应中氧化剂与还原剂的物质的量之比是
反应得到的产物之一是一种无毒无害的气体,该反应中氧化剂与还原剂的物质的量之比是_______ 。
(3)步骤ⅱ中盛装 溶液的仪器名称为
溶液的仪器名称为_______ 。
(4)步骤ⅱ中装置D的作用是_______ 。
(5)步骤ⅲ中依次用饱和 溶液无水乙醇、乙醚洗涤晶体,用饱和
溶液无水乙醇、乙醚洗涤晶体,用饱和 溶液洗涤的目的是
溶液洗涤的目的是_______ 。
(6)分析测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品纯度的流程:
①滴入 溶液的目的是除去
溶液的目的是除去 ,写出其反应的离子方程式:
,写出其反应的离子方程式:_______ 。
②若平均消耗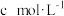
 标准溶液的体积为a mL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为
标准溶液的体积为a mL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为_______ %。
③若其他操作均正确,但 的加入量不足,会引起测定结果
的加入量不足,会引起测定结果_____ (填“偏大”“偏小”或“无影响”)。
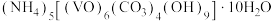 }的制备及纯度分析步骤如下。
}的制备及纯度分析步骤如下。Ⅰ.制备氧钒(Ⅳ)碱式碳酸铵晶体的流程如下:
 碱式碳酸铵晶体
碱式碳酸铵晶体其中,步骤ⅱ可通过如图装置完成。

实验步骤:
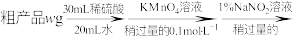
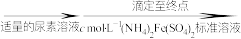 再重复实验两次。
再重复实验两次。已知:①氧钒(Ⅳ)碱式碳酸铵晶体难溶于水,

②+4价钒在弱酸性条件下具有还原性。
③
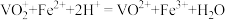 。
。④在该实验条件下,
 与尿素不反应。
与尿素不反应。回答下列问题:
(1)从原子结构角度解释+5价钒较稳定的原因:
(2)步骤ⅰ中
 和
和 反应得到的产物之一是一种无毒无害的气体,该反应中氧化剂与还原剂的物质的量之比是
反应得到的产物之一是一种无毒无害的气体,该反应中氧化剂与还原剂的物质的量之比是(3)步骤ⅱ中盛装
 溶液的仪器名称为
溶液的仪器名称为(4)步骤ⅱ中装置D的作用是
(5)步骤ⅲ中依次用饱和
 溶液无水乙醇、乙醚洗涤晶体,用饱和
溶液无水乙醇、乙醚洗涤晶体,用饱和 溶液洗涤的目的是
溶液洗涤的目的是(6)分析测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品纯度的流程:
①滴入
 溶液的目的是除去
溶液的目的是除去 ,写出其反应的离子方程式:
,写出其反应的离子方程式:②若平均消耗
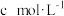
 标准溶液的体积为a mL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为
标准溶液的体积为a mL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为③若其他操作均正确,但
 的加入量不足,会引起测定结果
的加入量不足,会引起测定结果
您最近一年使用:0次
解题方法
6 . “挖掘文物价值,讲好中国故事。”下列文物在潮湿空气中易发生电化学腐蚀的是
|
|
| A.先锋煲(陶) | B.曜变天目碗(瓷) |
|
|
| C.铁足大铜鼎 | D.六棱柱形水晶穿珠 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 我国某大学科研团队通过超快电脉冲热还原法开发了一种新型碳载钌镍合金纳米催化剂(RuNi/C),并基于此催化剂制备出一种极具竞争力的高能量镍氢气( )电池,其工作原理如图所示。下列说法错误的是
)电池,其工作原理如图所示。下列说法错误的是
 )电池,其工作原理如图所示。下列说法错误的是
)电池,其工作原理如图所示。下列说法错误的是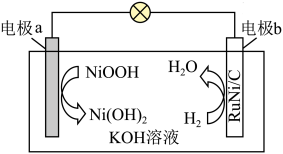
A.放电时, 向电极b移动 向电极b移动 |
| B.放电一段时间后,KOH溶液的浓度增大 |
C.放电时,电极a上的电极反应式为 |
D.外电路中每转移2mol  ,理论上电极b上消耗2g ,理论上电极b上消耗2g  |
您最近一年使用:0次
8 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1mol乙醛中含有σ键的数目为6 |
B.1L pH=3的稀 溶液中氢离子的数目为0.002 溶液中氢离子的数目为0.002 |
C.等物质的量的 和 和 气体中所含中子数均为16 气体中所含中子数均为16 |
D.标准状况下,11.2L  中含有的分子数目为0.5 中含有的分子数目为0.5 |
您最近一年使用:0次
9 . CO、 (主要指NO和
(主要指NO和 )是大气主要污染物之一。有效去除大气中的CO、
)是大气主要污染物之一。有效去除大气中的CO、 是环境保护的重要课题。
是环境保护的重要课题。
已知:
反应1:

反应2:

反应3:

反应4:

回答下列问题:
(1)计算
_______  ,反应3自发进行的条件是
,反应3自发进行的条件是_______ (填“高温”“低温”或“任意温度”)。
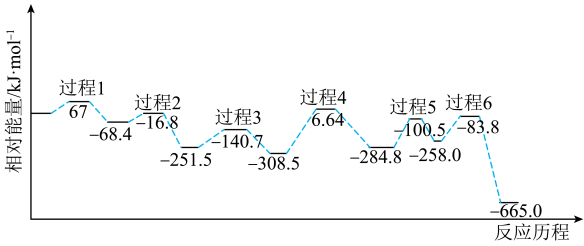
(2)已知反应4在某催化剂作用下的反应历程如图。
_______ (填“>”或“<”)0。
②该反应历程的决速步骤为过程_______ 。
③为了提高该反应的速率和NO平衡转化率,可采取的措施有_______ (填一条)。
(3)向密闭容器中充入一定量的 和
和 ,保持总压为
,保持总压为 ,发生反应4.当
,发生反应4.当 时NO的平衡转化率随温度T以及
时NO的平衡转化率随温度T以及 K下NO的平衡转化率随投料比
K下NO的平衡转化率随投料比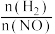 的变化关系如图。
的变化关系如图。_______ (填标号)。
A.气体的密度保持不变
B.NO的浓度不变
C.
D. 保持不变
保持不变
②表示 时NO的平衡转化率随温度T的变化关系的曲线是
时NO的平衡转化率随温度T的变化关系的曲线是_______ (填“Ⅰ”或“Ⅱ”),理由是_______ 。
③a、d两点对应的平衡常数大小比较为
_______ 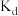 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
④b点对应条件下的压强平衡常数
_______  (
( 为用分压表示的平衡常数,分压=总压×物质的量分数,列出计算式即可)。
为用分压表示的平衡常数,分压=总压×物质的量分数,列出计算式即可)。
 (主要指NO和
(主要指NO和 )是大气主要污染物之一。有效去除大气中的CO、
)是大气主要污染物之一。有效去除大气中的CO、 是环境保护的重要课题。
是环境保护的重要课题。已知:
反应1:


反应2:


反应3:


反应4:


回答下列问题:
(1)计算

 ,反应3自发进行的条件是
,反应3自发进行的条件是(2)已知反应4在某催化剂作用下的反应历程如图。

②该反应历程的决速步骤为过程
③为了提高该反应的速率和NO平衡转化率,可采取的措施有
(3)向密闭容器中充入一定量的
 和
和 ,保持总压为
,保持总压为 ,发生反应4.当
,发生反应4.当 时NO的平衡转化率随温度T以及
时NO的平衡转化率随温度T以及 K下NO的平衡转化率随投料比
K下NO的平衡转化率随投料比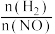 的变化关系如图。
的变化关系如图。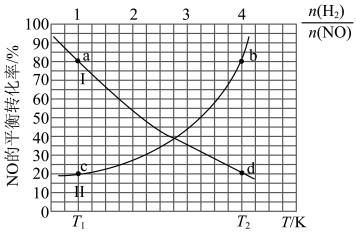
A.气体的密度保持不变
B.NO的浓度不变
C.

D.
 保持不变
保持不变②表示
 时NO的平衡转化率随温度T的变化关系的曲线是
时NO的平衡转化率随温度T的变化关系的曲线是③a、d两点对应的平衡常数大小比较为

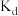 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。④b点对应条件下的压强平衡常数

 (
( 为用分压表示的平衡常数,分压=总压×物质的量分数,列出计算式即可)。
为用分压表示的平衡常数,分压=总压×物质的量分数,列出计算式即可)。
您最近一年使用:0次
10 . 钛酸亚铁常用于制备磁芯、磁盘和传感器等,它属于立方晶系,晶胞结构如图所示。下列叙述错误的是 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。

 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。A. 的分数坐标为 的分数坐标为 |
B.晶胞中 位于 位于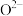 所形成的正八面体的体心 所形成的正八面体的体心 |
C. 和 和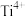 之间的最短距离为等 之间的最短距离为等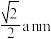 |
D.钛酸亚铁晶体密度为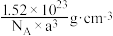 |
您最近一年使用:0次







