真题
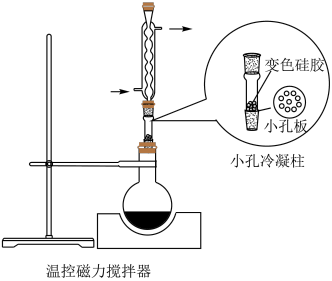
1 . 某实验小组为实现乙酸乙酯的绿色制备及反应过程可视化,设计实验方案如下: 烧瓶中分别加入
烧瓶中分别加入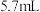 乙酸(
乙酸(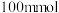 )、
)、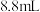 乙醇(
乙醇(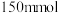 )、
)、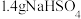 固体及4~6滴
固体及4~6滴 甲基紫的乙醇溶液。向小孔冷凝柱中装入变色硅胶。
甲基紫的乙醇溶液。向小孔冷凝柱中装入变色硅胶。
II.加热回流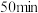 后,反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热。
后,反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热。
III.冷却后,向烧瓶中缓慢加入饱和 溶液至无
溶液至无 逸出,分离出有机相。
逸出,分离出有机相。
IV.洗涤有机相后,加入无水 ,过滤。
,过滤。
V.蒸馏滤液,收集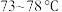 馏分,得无色液体
馏分,得无色液体 ,色谱检测纯度为
,色谱检测纯度为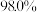 。
。
回答下列问题:
(1) 在反应中起
在反应中起_______ 作用,用其代替浓 的优点是
的优点是_______ (答出一条即可)。
(2)甲基紫和变色硅胶的颜色变化均可指示反应进程。变色硅胶吸水,除指示反应进程外,还可_______ 。
(3)使用小孔冷凝柱承载,而不向反应液中直接加入变色硅胶的优点是_______(填标号)。
(4)下列仪器中,分离有机相和洗涤有机相时均需使用的是_______ (填名称)。_______ (精确至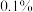 )。
)。
(6)若改用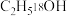 作为反应物进行反应,质谱检测目标产物分子离子峰的质荷比数值应为
作为反应物进行反应,质谱检测目标产物分子离子峰的质荷比数值应为_______ (精确至1)。
 烧瓶中分别加入
烧瓶中分别加入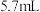 乙酸(
乙酸(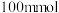 )、
)、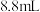 乙醇(
乙醇(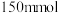 )、
)、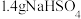 固体及4~6滴
固体及4~6滴 甲基紫的乙醇溶液。向小孔冷凝柱中装入变色硅胶。
甲基紫的乙醇溶液。向小孔冷凝柱中装入变色硅胶。II.加热回流
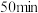 后,反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热。
后,反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热。III.冷却后,向烧瓶中缓慢加入饱和
 溶液至无
溶液至无 逸出,分离出有机相。
逸出,分离出有机相。IV.洗涤有机相后,加入无水
 ,过滤。
,过滤。V.蒸馏滤液,收集
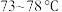 馏分,得无色液体
馏分,得无色液体 ,色谱检测纯度为
,色谱检测纯度为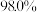 。
。回答下列问题:
(1)
 在反应中起
在反应中起 的优点是
的优点是(2)甲基紫和变色硅胶的颜色变化均可指示反应进程。变色硅胶吸水,除指示反应进程外,还可
(3)使用小孔冷凝柱承载,而不向反应液中直接加入变色硅胶的优点是_______(填标号)。
| A.无需分离 | B.增大该反应平衡常数 |
| C.起到沸石作用,防止暴沸 | D.不影响甲基紫指示反应进程 |
(4)下列仪器中,分离有机相和洗涤有机相时均需使用的是
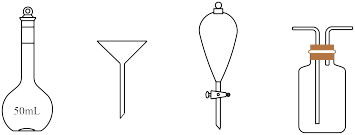
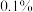 )。
)。(6)若改用
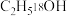 作为反应物进行反应,质谱检测目标产物分子离子峰的质荷比数值应为
作为反应物进行反应,质谱检测目标产物分子离子峰的质荷比数值应为
您最近一年使用:0次
名校
解题方法
2 . 下列反应的离子方程式书写正确的是
A.向 溶液中加入硝酸: 溶液中加入硝酸: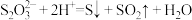 |
B.久置的 溶液中出现红褐色固体: 溶液中出现红褐色固体: |
C.电解 水溶液的离子方程式: 水溶液的离子方程式: |
D.向 溶液中加入 溶液中加入 : : |
您最近一年使用:0次
名校
解题方法
3 . 锌是一种重要的金属,锌及其化合物被广泛应用于汽车、建筑、船舶、电池等行业。现某科研小组以固体废锌催化剂(主要成分是 ,含少量
,含少量 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示: 和
和 转化为
转化为 进入溶液。
进入溶液。
② 时,
时,
③深度除杂标准:溶液中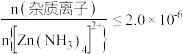 。
。
(1)“滤渣1”的主要成分为 、
、___________ 。
(2)“深度除锰”是将残留的 转化为
转化为 ,写出该过程的化学方程式
,写出该过程的化学方程式___________ 。该过程中 的加入量远大于其理论值,原因为
的加入量远大于其理论值,原因为___________ 。
(3)“深度除铜”时,锌的最终回收率、除铜效果(用反应后溶液中的铜锌比 表示)与
表示)与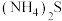 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。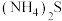 加入量最优选择
加入量最优选择___________ (填标号)。
A.100% B.110% C.120% D.130%
②由图可知,当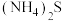 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是________ (用离子方程式解释)。
(4) 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图:___________ 区。
②配位键①和②相比,较稳定的是___________ 。
③键角③___________ 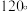 (填“
(填“ ”“
”“ ”或“
”或“ )。
)。
 ,含少量
,含少量 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示:
 和
和 转化为
转化为 进入溶液。
进入溶液。②
 时,
时,
③深度除杂标准:溶液中
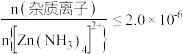 。
。(1)“滤渣1”的主要成分为
 、
、(2)“深度除锰”是将残留的
 转化为
转化为 ,写出该过程的化学方程式
,写出该过程的化学方程式 的加入量远大于其理论值,原因为
的加入量远大于其理论值,原因为(3)“深度除铜”时,锌的最终回收率、除铜效果(用反应后溶液中的铜锌比
 表示)与
表示)与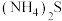 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。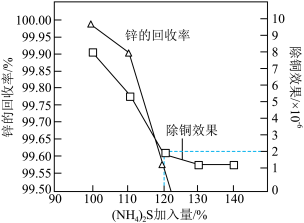
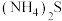 加入量最优选择
加入量最优选择A.100% B.110% C.120% D.130%
②由图可知,当
 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是(4)
 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图: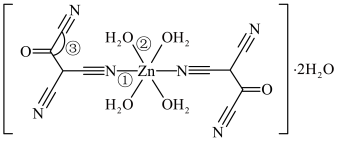
②配位键①和②相比,较稳定的是
③键角③
 (填“
(填“ ”“
”“ ”或“
”或“ )。
)。
您最近一年使用:0次
名校
解题方法
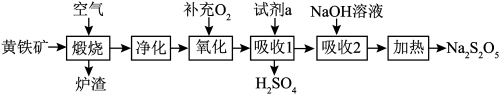
4 . 硫酸的消耗量是衡量一个国家化学工业发展水平的标志。以黄铁矿(主要成分为 )为原料生产
)为原料生产 和
和 。
。
(1) 中铁元素的化合价为
中铁元素的化合价为________ ;试剂a为________ 。
(2) 可和盐酸发生复分解反应生成一种不稳定的液态化合物,该化合物的电子式:
可和盐酸发生复分解反应生成一种不稳定的液态化合物,该化合物的电子式:________ 。
(3)煅烧时主要反应的化学方程式为____________ 。
(4)“氧化”时,反应的化学方程式为____________ 。
(5) 可用于葡萄酒的抗氧化剂,用碘液可以测定葡萄酒中
可用于葡萄酒的抗氧化剂,用碘液可以测定葡萄酒中 的含量,请写出其反应的离子方程式:
的含量,请写出其反应的离子方程式:__________ 。若要检验 是否变质生成了
是否变质生成了 ,设计简单实验进行检验
,设计简单实验进行检验____________ 。
(6)在测定某葡萄酒中 的含量时,取100.00mL葡萄酒样品,消耗
的含量时,取100.00mL葡萄酒样品,消耗 碘液20.00mL,样品中
碘液20.00mL,样品中 的含量为
的含量为________  。
。
 )为原料生产
)为原料生产 和
和 。
。
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)
 可和盐酸发生复分解反应生成一种不稳定的液态化合物,该化合物的电子式:
可和盐酸发生复分解反应生成一种不稳定的液态化合物,该化合物的电子式:(3)煅烧时主要反应的化学方程式为
(4)“氧化”时,反应的化学方程式为
(5)
 可用于葡萄酒的抗氧化剂,用碘液可以测定葡萄酒中
可用于葡萄酒的抗氧化剂,用碘液可以测定葡萄酒中 的含量,请写出其反应的离子方程式:
的含量,请写出其反应的离子方程式: 是否变质生成了
是否变质生成了 ,设计简单实验进行检验
,设计简单实验进行检验(6)在测定某葡萄酒中
 的含量时,取100.00mL葡萄酒样品,消耗
的含量时,取100.00mL葡萄酒样品,消耗 碘液20.00mL,样品中
碘液20.00mL,样品中 的含量为
的含量为 。
。
您最近一年使用:0次
名校
解题方法
5 . 下列做法与调控化学反应速率无关的是
| A.用冰箱冷藏以保鲜食物 | B.酸浸时先将矿石粉碎 |
| C.食盐中添加碘酸钾预防缺碘 | D.食品包装时加入还原铁粉包 |
您最近一年使用:0次
名校
6 . 下列对物质性质的解释错误的是
选项 | 物质性质 | 解释 |
A | 吡咯( | 吡咯中,氮原子的孤对电子参与形成了离域键,使得氮原子上的电子云密度降低 |
B | HF气体的摩尔质量测定值大于实际值 | HF形成了分子间氢键 |
C | 乙酸的酸性大于丙酸 | 烃基越长,推电子效应越大 |
D | 18-冠-6识别钾离子,体现了超分子“分子识别”的特征 | 18-冠-6中,氧原子电负性大,带负电荷,通过离子键与钾离子作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
昨日更新
|
168次组卷
|
2卷引用:2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题
真题
解题方法
7 . 文物见证历史,化学创造文明。东北三省出土的下列文物据其主要成分不能与其他三项归为一类的是
| A.金代六曲葵花婆金银盏 | B.北燕鸭形玻璃注 |
| C.汉代白玉耳杯 | D.新石器时代彩绘几何纹双腹陶罐 |
您最近一年使用:0次
名校
解题方法
8 . 钪是一种重要的稀土元素,其氧化物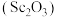 是一种重要的无机化工原料,广泛应用于电子、陶瓷、光学、化工等领域。工业上利用固体废料“赤泥”(含
是一种重要的无机化工原料,广泛应用于电子、陶瓷、光学、化工等领域。工业上利用固体废料“赤泥”(含 、
、 、
、 、
、 、
、 等)生产高纯氧化钪,同时回收
等)生产高纯氧化钪,同时回收 。工艺流程如图:
。工艺流程如图: ;ⅲ.草酸沉淀实验结果
;ⅲ.草酸沉淀实验结果
回答下列问题:
(1)基态 原子的简化电子排布式为
原子的简化电子排布式为___________ 。
(2)为提高“酸浸”速率,可采取的措施是___________ (答出一条即可)。
(3)滤渣1的成分___________ 。
(4)“氧化”后溶液中 浓度为
浓度为 ,常温下“调
,常温下“调 ”时,若控制
”时,若控制 ,则
,则 的去除率为
的去除率为___________ %(忽略掉 前后溶液的体积变化)。
前后溶液的体积变化)。
(5)过程中 生成
生成 的离子方程式为
的离子方程式为___________ 。
(6)研究人员对“沉钪”过程的定量条件进行了对比实验,条件最适合的是已知ⅲ中的第1组,原因是:不仅沉淀率>99.0%、节约草酸用量,且___________ 。
(7)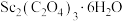 在空气中加热分解时,
在空气中加热分解时, 随温度变化如图所示。已知:
随温度变化如图所示。已知: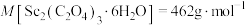 。250℃时固体的主要成分是
。250℃时固体的主要成分是___________ (填化学式)。
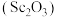 是一种重要的无机化工原料,广泛应用于电子、陶瓷、光学、化工等领域。工业上利用固体废料“赤泥”(含
是一种重要的无机化工原料,广泛应用于电子、陶瓷、光学、化工等领域。工业上利用固体废料“赤泥”(含 、
、 、
、 、
、 、
、 等)生产高纯氧化钪,同时回收
等)生产高纯氧化钪,同时回收 。工艺流程如图:
。工艺流程如图:
 ;ⅲ.草酸沉淀实验结果
;ⅲ.草酸沉淀实验结果| 实验 | 溶液酸度(pH) |  与草酸物质的量之比 与草酸物质的量之比 | 沉淀颗粒 | 草酸钪沉率% |
| 1 | 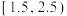 |  | 较粗 | 99.2 |
| 2 | 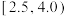 |  | 粗 | 97.2 |
| 3 |  | 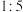 | 细 | 90.1 |
| 4 |  | 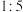 | 很细 | 93.3 |
(1)基态
 原子的简化电子排布式为
原子的简化电子排布式为(2)为提高“酸浸”速率,可采取的措施是
(3)滤渣1的成分
(4)“氧化”后溶液中
 浓度为
浓度为 ,常温下“调
,常温下“调 ”时,若控制
”时,若控制 ,则
,则 的去除率为
的去除率为 前后溶液的体积变化)。
前后溶液的体积变化)。(5)过程中
 生成
生成 的离子方程式为
的离子方程式为(6)研究人员对“沉钪”过程的定量条件进行了对比实验,条件最适合的是已知ⅲ中的第1组,原因是:不仅沉淀率>99.0%、节约草酸用量,且
(7)
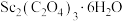 在空气中加热分解时,
在空气中加热分解时, 随温度变化如图所示。已知:
随温度变化如图所示。已知: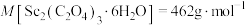 。250℃时固体的主要成分是
。250℃时固体的主要成分是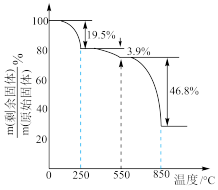
您最近一年使用:0次
名校
9 . 已知 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL
为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL KSCN溶液、
KSCN溶液、 溶液;乙组:向
溶液;乙组:向 的KSCN溶液中滴加酸性
的KSCN溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丙组:向
溶液褪色;丙组:向 的
的 溶液中滴加酸性
溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丁组:分别取50mL
溶液褪色;丁组:分别取50mL KSCN溶液和50mL
KSCN溶液和50mL
 溶液,混合,向混合液中滴加酸性
溶液,混合,向混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法
溶液,溶液先变红后褪色,下列说法错误 的是
 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL
为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL KSCN溶液、
KSCN溶液、 溶液;乙组:向
溶液;乙组:向 的KSCN溶液中滴加酸性
的KSCN溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丙组:向
溶液褪色;丙组:向 的
的 溶液中滴加酸性
溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丁组:分别取50mL
溶液褪色;丁组:分别取50mL KSCN溶液和50mL
KSCN溶液和50mL
 溶液,混合,向混合液中滴加酸性
溶液,混合,向混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法
溶液,溶液先变红后褪色,下列说法| A.甲组同学用到500mL容量瓶、玻璃棒、烧杯、胶头滴管等玻璃仪器 |
B.乙组实验中 将 将 氧化为 氧化为 |
C.丙组实验发生反应的离子方程式: |
D.丁组实验说明还原性: |
您最近一年使用:0次
7日内更新
|
154次组卷
|
4卷引用:2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题
名校
10 . 下列物质对应的化学式错误的是
| A.金刚砂:SiC | B.小苏打: |
C.绿矾: | D.芒硝: |
您最近一年使用:0次

 )和吡啶(
)和吡啶( )均为平面分子,吡啶碱性较强
)均为平面分子,吡啶碱性较强

