名校
解题方法
1 . 短周期主族元素a、b、c、d的原子序数依次增大,同周期主族元素中,b的原子半径最大。原子半径与原子序数、价层电子数关系如图所示。下列叙述正确的是

| A.a和d的简单氢化物的VSEPR模型完全相同 |
| B.工业上可通过电解熔融态的c的氧化物制备c单质 |
C. 和 和 所含化学键类型完全相同 所含化学键类型完全相同 |
| D.a的简单氢化物由液态转化为气态的过程中,断裂了极性键 |
您最近一年使用:0次
2 . 常温下,在 (弱酸)溶液中滴加
(弱酸)溶液中滴加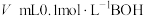 (弱碱)溶液生成强电解质
(弱碱)溶液生成强电解质 ,混合溶液中
,混合溶液中 与
与 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是
 (弱酸)溶液中滴加
(弱酸)溶液中滴加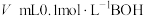 (弱碱)溶液生成强电解质
(弱碱)溶液生成强电解质 ,混合溶液中
,混合溶液中 与
与 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是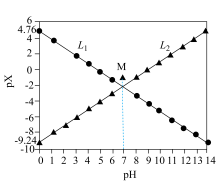
A. 代表 代表 与 与 的关系 的关系 |
B. 时达到 时达到 点, 点, 不水解 不水解 |
C.常温下, |
D.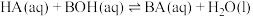 的平衡常数 的平衡常数 小于10000 小于10000 |
您最近一年使用:0次
名校
解题方法
3 .  冠
冠 的结构如图所示,其空腔直径为
的结构如图所示,其空腔直径为 。已知部分粒子直径如下表,该冠醚能识别的粒子是
。已知部分粒子直径如下表,该冠醚能识别的粒子是
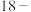 冠
冠 的结构如图所示,其空腔直径为
的结构如图所示,其空腔直径为 。已知部分粒子直径如下表,该冠醚能识别的粒子是
。已知部分粒子直径如下表,该冠醚能识别的粒子是
| 粒子 |  |  |  |  |
| 直径/pm | 152 | 204 | 276 | 334 |
A. | B. | C. | D. |
您最近一年使用:0次
名校
4 . 前四周期元素A、B、C、D、E的原子序数依次增大,基态A原子的核外电子占据3个能级且每个能级上电子数相等,基态C原子价层电子排布式为 ,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态
,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态 的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:
的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:
(1)基态E原子有___________ 种运动状态不同的电子,D位于元素周期表___________ 区。
(2)在A、B、C、D的简单氢化物中,沸点最高的是___________ (填化学式,下同);键角最大的是___________ 。
(3) 分子中D的杂化类型是
分子中D的杂化类型是___________ ;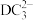 的空间结构为
的空间结构为___________ 。
(4)元素的基态气态原子得到一个电子形成 价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为
价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为 ,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:
,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:___________ 。
(5)B、E组成的一种立方晶胞如图2所示。已知晶胞参数为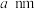 ,设
,设 为阿伏加德罗常数的值,该晶体化学式为
为阿伏加德罗常数的值,该晶体化学式为___________ ,该晶体密度为___________  。
。
 ,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态
,C、D位于同主族,且基态D原子比基态C原子多2个电子能级,基态 的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:
的核外电子占据的最高能层符号为M且其d轨道达到全充满结构,回答下列问题:(1)基态E原子有
(2)在A、B、C、D的简单氢化物中,沸点最高的是
(3)
 分子中D的杂化类型是
分子中D的杂化类型是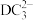 的空间结构为
的空间结构为(4)元素的基态气态原子得到一个电子形成
 价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为
价气态阴离子时所放出的能量称为该元素的第一电子亲和能,单位为 ,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:
,习惯规定,放出能量时电子亲和能为正值,吸收能量时电子亲和能为负值。电子亲和能越大,表明越容易得到电子,A、B、C元素的电子亲和能如图所示:
(5)B、E组成的一种立方晶胞如图2所示。已知晶胞参数为
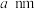 ,设
,设 为阿伏加德罗常数的值,该晶体化学式为
为阿伏加德罗常数的值,该晶体化学式为 。
。
您最近一年使用:0次
名校
解题方法
5 . 实验室制备配合物 的原理是
的原理是
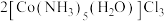 ,下列叙述错误的是
,下列叙述错误的是
 的原理是
的原理是
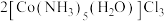 ,下列叙述错误的是
,下列叙述错误的是A. 的电子式为 的电子式为 |
B.基态N原子价层电子排布图为 |
C. 中 中 的配位数为6 的配位数为6 |
D.已知 为正八面体结构,则 为正八面体结构,则 有4种结构 有4种结构 |
您最近一年使用:0次
名校
6 . 有机物D的一种合成路线如下:
(1)A的名称是___________ , 分子的键角为
分子的键角为___________ 。
(2)C的分子式为___________ 。
(3)沸点: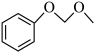
___________ (填“高于”或“低于”)D,其原因是___________ 。
(4)A→B反应类型是___________ ;D中官能团名称是___________ 。
(5)i中 键与
键与 键的个数之比为
键的个数之比为___________ 。乙烯与i互为___________ (选填“同系物”“同分异构体”“同位素”或“同素异形体”)。
(6)B的一溴代物有___________ 种。

(1)A的名称是
 分子的键角为
分子的键角为(2)C的分子式为
(3)沸点:

(4)A→B反应类型是
(5)i中
 键与
键与 键的个数之比为
键的个数之比为(6)B的一溴代物有
您最近一年使用:0次
名校
解题方法
7 . 氮化钛是一种导电材料,也是一种催化剂。氮化钛晶胞如图所示,A的原子坐标为 ,C的原子坐标为
,C的原子坐标为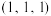 。已知:它的晶胞参数为
。已知:它的晶胞参数为 ,氮原子半径为
,氮原子半径为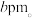 下列叙述错误的是
下列叙述错误的是
 ,C的原子坐标为
,C的原子坐标为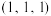 。已知:它的晶胞参数为
。已知:它的晶胞参数为 ,氮原子半径为
,氮原子半径为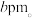 下列叙述错误的是
下列叙述错误的是
| A.基态钛原子有2个未成对电子 | B.B的原子坐标为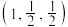 |
C.钛原子半径为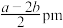 | D.氮原子的配位数为12 |
您最近一年使用:0次
名校
8 . 钠、镁、铝、硅、磷、硫、氯的元素对应的某“物理量”递变规律符合图像的是

| A.原子半径 | B.单质的熔点 | C.第一电离能 | D.电负性 |
您最近一年使用:0次
名校
9 . 氨是国民经济的基础,工业合成氨的反应:
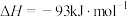 。
。
(1)该反应在下列条件下能自发进行的是___________ (填字母,下同)。
A.较低温度 B.较高温度 C.任何温度
(2)在恒温恒容密闭容器中充入 和
和 ,在铁粉催化下合成
,在铁粉催化下合成 。下列叙述正确的是___________。
。下列叙述正确的是___________。
(3)一定温度下,向恒容密闭容器中充入一定量 和
和 ,平衡体系中
,平衡体系中 体积分数与投料比
体积分数与投料比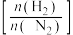 (保持总物质的量相等)关系如图1所示。在a、b、c中,
(保持总物质的量相等)关系如图1所示。在a、b、c中, 平衡转化率最大的是
平衡转化率最大的是___________ 。 和
和 ,在恒温、绝热条件中达到平衡,测得气体压强随时间变化如图2所示。
,在恒温、绝热条件中达到平衡,测得气体压强随时间变化如图2所示。___________ (填“恒温”或“绝热”)条件下进行。
②正反应速率:b___________ c(填“ ”“
”“ ”或“
”或“ ”,下同),气体总物质的量a
”,下同),气体总物质的量a___________ b。
③a点 的转化率为
的转化率为___________ 。

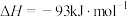 。
。(1)该反应在下列条件下能自发进行的是
A.较低温度 B.较高温度 C.任何温度
(2)在恒温恒容密闭容器中充入
 和
和 ,在铁粉催化下合成
,在铁粉催化下合成 。下列叙述正确的是___________。
。下列叙述正确的是___________。A. 体积分数不变时一定达到平衡状态 体积分数不变时一定达到平衡状态 |
B.平衡后通入 , , 的产率保持不变 的产率保持不变 |
C.增大铁粉质量, 的平衡转化率增大 的平衡转化率增大 |
D.平衡时放出热量为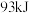 |
(3)一定温度下,向恒容密闭容器中充入一定量
 和
和 ,平衡体系中
,平衡体系中 体积分数与投料比
体积分数与投料比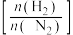 (保持总物质的量相等)关系如图1所示。在a、b、c中,
(保持总物质的量相等)关系如图1所示。在a、b、c中, 平衡转化率最大的是
平衡转化率最大的是
 和
和 ,在恒温、绝热条件中达到平衡,测得气体压强随时间变化如图2所示。
,在恒温、绝热条件中达到平衡,测得气体压强随时间变化如图2所示。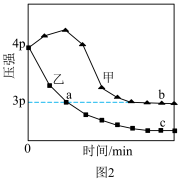
②正反应速率:b
 ”“
”“ ”或“
”或“ ”,下同),气体总物质的量a
”,下同),气体总物质的量a③a点
 的转化率为
的转化率为
您最近一年使用:0次
名校
10 . 我国科学家屠呦呦等人从青蒿中提取青蒿素并测定其分子结构,青蒿素分子结构如图所示,已知连有4个不同的原子或原子团的碳原子叫作手性碳原子。下列叙述错误的是
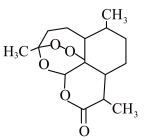
| A.X射线衍射法可用于测定青蒿素的分子结构 |
| B.通过质谱仪可确定青蒿素含酯基和醚键 |
| C.青蒿素含有过氧键,可能具有较强的氧化性 |
| D.1个青蒿素分子含7个手性碳原子 |
您最近一年使用:0次



