解题方法
1 . 下列事实不能用勒夏特列原理解释的是
| A.在合成氨实际生产中,使气态氨变成液氨后及时从平衡混合物中分离出去,以提高原料的利用率 |
B. 、 、 、 、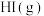 组成的平衡体系,加压后体系颜色变深 组成的平衡体系,加压后体系颜色变深 |
C.向重铬酸钾( )溶液中滴加少量KOH溶液,溶液颜色由橙色变为黄色 )溶液中滴加少量KOH溶液,溶液颜色由橙色变为黄色 |
| D.实验室中常用排饱和食盐水的方法收集氯气 |
您最近一年使用:0次
解题方法
2 . 下列叙述正确的是
A.恒容容器中发生反应N2(g)+O2(g)  2NO(g),若平衡后在容器中充入He,正、逆反应的速率均不变 2NO(g),若平衡后在容器中充入He,正、逆反应的速率均不变 |
B.当一定量的锌粉和过量的6 盐酸反应时,为了减慢反应速率,又不影响产生 盐酸反应时,为了减慢反应速率,又不影响产生 的总量,可向反应器中加入一些水、 的总量,可向反应器中加入一些水、 溶液或 溶液或 溶液 溶液 |
C.已知反应:CaCO3(s)  CaO(s)+CO2(g),在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时CO2(g)的浓度将升高至原来的2倍 CaO(s)+CO2(g),在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时CO2(g)的浓度将升高至原来的2倍 |
D.在一定温度下,容积一定的密闭容器中的反应A(s)+2B(g) C(g)+D(g),当混合气体的总压强不变时,则表明该反应已达平衡状态 C(g)+D(g),当混合气体的总压强不变时,则表明该反应已达平衡状态 |
您最近一年使用:0次
解题方法
3 . 下列叙述错误的是
| A.活化能接近于零的自发反应,当反应物相互接触时,反应瞬间完成 |
| B.我国西周时期发明的“酒曲”酿酒工艺,是利用了催化剂加快反应速率的原理 |
| C.增大反应物浓度,可增大活化分子百分数,从而使单位时间有效碰撞次数增多 |
| D.通过光辐照、超声波、高速研磨等方式都有可能改变化学反应速率 |
您最近一年使用:0次
4 . 某实验小组探究外界条件对化学反应速率的影响,进行了以下实验。
Ⅰ.探究温度、浓度对硫代硫酸钠与稀硫酸反应速率的影响
(1)写出Na2S2O3与H2SO4反应的离子方程式_______ 。
(2)该小组同学设计了如下表所示系列实验:
①实验①和②目的是探究温度对该反应速率的影响,则实验②中,t1=_______ (填“20℃”或“60℃”)、V2= _______ mL。
②若V4=10.0 V5=6.0,则t2=_______ (填“20℃”或“60℃”),实验①和③的实验目的是_______ 。
Ⅱ.探究催化剂对H2O2分解速率的影响_______ ,为此须用到实验器材为_______ 。
Ⅲ.探究催化剂对H2O2分解速率的影响
(4)若仍用上图中的装置,探究MnO2对H2O2分解的催化作用,则此时注射器中应加入的试剂是_______ ,写出该反应的化学方程式_______ 。
Ⅰ.探究温度、浓度对硫代硫酸钠与稀硫酸反应速率的影响
(1)写出Na2S2O3与H2SO4反应的离子方程式
(2)该小组同学设计了如下表所示系列实验:
实验序号 | 反应温度/℃ | Na2S2O3溶液 | H2SO4稀溶液 | H2O | ||
V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
② | t1 | V1 | 0.10 | V2 | 0.50 | V3 |
③ | t2 | V4 | 0.10 | V5 | 0.50 | V6 |
②若V4=10.0 V5=6.0,则t2=
Ⅱ.探究催化剂对H2O2分解速率的影响
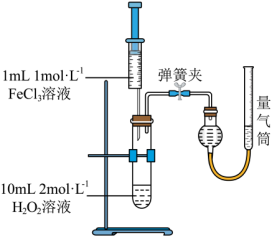
Ⅲ.探究催化剂对H2O2分解速率的影响
(4)若仍用上图中的装置,探究MnO2对H2O2分解的催化作用,则此时注射器中应加入的试剂是
您最近一年使用:0次
5 . N2(g)+3H2(g) 2NH3(g)
2NH3(g) ,下列分析不正确的是
,下列分析不正确的是
 2NH3(g)
2NH3(g) ,下列分析不正确的是
,下列分析不正确的是A.氮分子的 键能大,断开该键需要较多能量 键能大,断开该键需要较多能量 |
| B.增大合成氨的反应速率与提高平衡混合物中氨的含量所采取的措施不完全一致 |
C.平衡混合物中 的沸点最高,液化、分离出 的沸点最高,液化、分离出 能提高其产率及化学反应速率 能提高其产率及化学反应速率 |
D.断裂1  和3 和3  的共价键所需能量小于断裂2 的共价键所需能量小于断裂2  的共价键所需能量 的共价键所需能量 |
您最近一年使用:0次
6 . 已知:CH3OH(g)+H2O(g) 3H2(g)+CO2(g) ΔH>0,则下列有利于提高CO2平衡产率的条件是
3H2(g)+CO2(g) ΔH>0,则下列有利于提高CO2平衡产率的条件是
 3H2(g)+CO2(g) ΔH>0,则下列有利于提高CO2平衡产率的条件是
3H2(g)+CO2(g) ΔH>0,则下列有利于提高CO2平衡产率的条件是| A.高温、高压 | B.低温、高压 | C.高温、低压 | D.低温、低压 |
您最近一年使用:0次
7 . 将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应:H2(g)+Br2(g)  2HBr(g) ΔH <0,平衡时HBr(g)的体积分数为a;若初始条件相同,绝热下进行上述反应,平衡时HBr (g)的体积分数为b,a与b的关系是
2HBr(g) ΔH <0,平衡时HBr(g)的体积分数为a;若初始条件相同,绝热下进行上述反应,平衡时HBr (g)的体积分数为b,a与b的关系是
 2HBr(g) ΔH <0,平衡时HBr(g)的体积分数为a;若初始条件相同,绝热下进行上述反应,平衡时HBr (g)的体积分数为b,a与b的关系是
2HBr(g) ΔH <0,平衡时HBr(g)的体积分数为a;若初始条件相同,绝热下进行上述反应,平衡时HBr (g)的体积分数为b,a与b的关系是| A.a >b | B.a=b | C.a <b | D.无法确定 |
您最近一年使用:0次
真题
解题方法
8 . 文物见证历史,化学创造文明。东北三省出土的下列文物据其主要成分不能与其他三项归为一类的是
| A.金代六曲葵花婆金银盏 | B.北燕鸭形玻璃注 |
| C.汉代白玉耳杯 | D.新石器时代彩绘几何纹双腹陶罐 |
您最近一年使用:0次
9 . 钴广泛应用于电池、合金等领域。以含钴废料(主要含 和
和 ,还含有
,还含有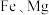 等元素以及
等元素以及 、碳、有机物)为原料制备钴的流程如下:
、碳、有机物)为原料制备钴的流程如下: 难溶于水。
难溶于水。
② (焦亚硫酸钠)常作食品抗氧化剂。
(焦亚硫酸钠)常作食品抗氧化剂。
③常温下,部分氢氧化物沉淀的 如表所示。
如表所示。
④氧化性: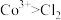 。
。
回答下列问题:
(1)“浸取”时硫酸不宜用浓盐酸代替,其原因是___________ (用离子方程式表示)。
(2)其他条件相同时,“氧化”过程中,氧化率与温度的关系如图1所示,氧化率与 的关系如图2所示(不考虑
的关系如图2所示(不考虑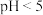 的情况)。
的情况)。___________ 。在此条件下,实际消耗的双氧水远大于理论用量,可能的原因是___________ 。
(3)有人认为“除镁”可以通过调节 代替加入
代替加入 ,请你评价:
,请你评价:___________ (判断是否可行,简述理由)。
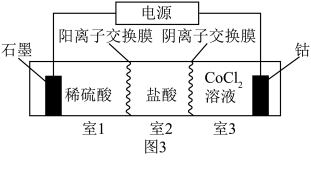
(4)工业上也可利用图3装置实现制备 。
。___________ 。生成 时,室1中溶液理论上减少
时,室1中溶液理论上减少___________ g。
②相较于直接电解 溶液,图3中“三室两膜”装置突出优点是
溶液,图3中“三室两膜”装置突出优点是___________ 。(从绿色化学角度分析)
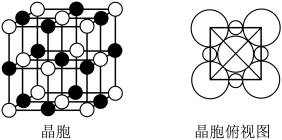
(5)钴的一种氧化物的晶胞如图所示,已知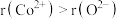 。钴离子的配位数为
。钴离子的配位数为___________ ,晶胞中原子空间利用率为___________ 。[用含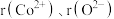 和π的代数式表示,已知:晶胞中原子空间利用率
和π的代数式表示,已知:晶胞中原子空间利用率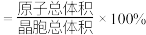 ]
]
 和
和 ,还含有
,还含有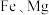 等元素以及
等元素以及 、碳、有机物)为原料制备钴的流程如下:
、碳、有机物)为原料制备钴的流程如下: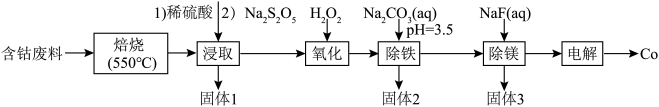
 难溶于水。
难溶于水。②
 (焦亚硫酸钠)常作食品抗氧化剂。
(焦亚硫酸钠)常作食品抗氧化剂。③常温下,部分氢氧化物沉淀的
 如表所示。
如表所示。 |  |  |  |  | |
开始沉淀 | 0.3 | 2.7 | 7.6 | 7.2 | 9.6 |
完全沉淀 | 1.2 | 3.2 | 9.6 | 9.2 | 11.1 |
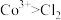 。
。回答下列问题:
(1)“浸取”时硫酸不宜用浓盐酸代替,其原因是
(2)其他条件相同时,“氧化”过程中,氧化率与温度的关系如图1所示,氧化率与
 的关系如图2所示(不考虑
的关系如图2所示(不考虑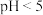 的情况)。
的情况)。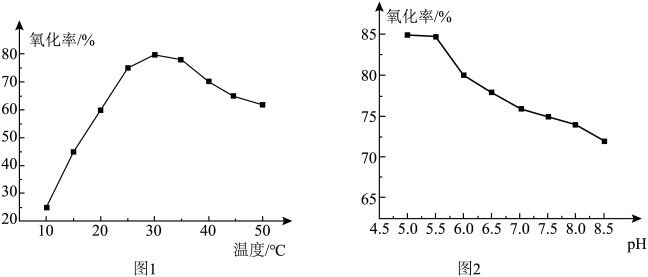
(3)有人认为“除镁”可以通过调节
 代替加入
代替加入 ,请你评价:
,请你评价:(4)工业上也可利用图3装置实现制备
 。
。
 时,室1中溶液理论上减少
时,室1中溶液理论上减少②相较于直接电解
 溶液,图3中“三室两膜”装置突出优点是
溶液,图3中“三室两膜”装置突出优点是(5)钴的一种氧化物的晶胞如图所示,已知
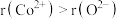 。钴离子的配位数为
。钴离子的配位数为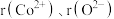 和π的代数式表示,已知:晶胞中原子空间利用率
和π的代数式表示,已知:晶胞中原子空间利用率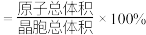 ]
]
您最近一年使用:0次
10 . 向体积均为 的甲、乙两个恒容密闭容器中分别充入
的甲、乙两个恒容密闭容器中分别充入 和
和 ,发生反应:
,发生反应: 。分别在绝热、恒温条件下进行,两反应体系的压强随时间的变化曲线如图所示。下列说法错误的是
。分别在绝热、恒温条件下进行,两反应体系的压强随时间的变化曲线如图所示。下列说法错误的是
 的甲、乙两个恒容密闭容器中分别充入
的甲、乙两个恒容密闭容器中分别充入 和
和 ,发生反应:
,发生反应: 。分别在绝热、恒温条件下进行,两反应体系的压强随时间的变化曲线如图所示。下列说法错误的是
。分别在绝热、恒温条件下进行,两反应体系的压强随时间的变化曲线如图所示。下列说法错误的是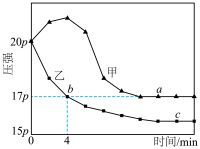
| A.正反应在较低温度下能自发进行 |
B.乙在恒温条件下进行, |
| C.a点的正反应速率大于c点的正反应速率 |
| D.甲条件下平衡常数K小于20.25 |
您最近一年使用:0次



