名校
解题方法
1 . 下列离子方程式正确的是
A.用过量的 溶液吸收 溶液吸收 尾气: 尾气: |
B.铜丝插入浓硫酸中:Cu+H2SO4(浓)=Cu2++SO +H2↑ +H2↑ |
C.向 溶液中加过量的 溶液中加过量的 溶液并加热: 溶液并加热: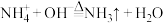 |
D.Fe溶于足量稀 : :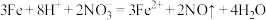 |
您最近一年使用:0次
名校
解题方法
2 . 化学与生产、生活息息相关,下列叙述正确的是
| A.SO2有毒,故不能作食品添加剂 |
| B.医疗上,BaCO3可用作消化系统X射线检查的内服药剂 |
| C.浓硫酸具有很强的吸水性,可用来干燥氨气 |
| D.NH3沸点低,易液化,工业上常用液氨作制冷剂 |
您最近一年使用:0次
3 . PVC是聚氯乙烯的英文简称,可由氯乙烯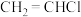 发生加聚反应得到。下列有关说法正确的是
发生加聚反应得到。下列有关说法正确的是
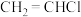 发生加聚反应得到。下列有关说法正确的是
发生加聚反应得到。下列有关说法正确的是A.聚氯乙烯的结构简式为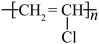 |
| B.聚氯乙烯是纯净物,可作为食品的包装材料 |
C.聚氯乙烯的链节为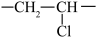 |
| D.聚氯乙烯能使酸性高锰酸钾溶液褪色 |
您最近一年使用:0次
解题方法
4 . 临猗苹果香气浓郁、爽甜多汁,其含有的一种有机物R的结构如图所示,下列有关R的说法正确的是
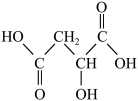
| A.含有三种官能团 |
| B.不能发生取代反应 |
| C.既能与乙醇反应,又能与乙酸反应 |
D.1molR与足量的钠反应生成1mol |
您最近一年使用:0次
5 . 山西被誉为“华夏文明摇篮”,素有“中国古代文化博物馆”之称。下列有关山西博物院镇馆之宝的叙述错误的是
| 选项 | A.庙底沟彩陶罐 | B.晋候鸟尊 |
| 文物 |
|
|
| 叙述 | 以黏土为原料经高温烧结而成 | 可用足量浓硝酸清洗除去表面的铜绿 |
| 选项 | C.虞弘墓石椁 | D.北魏司马金龙墓木板漆画 |
| 选项 |
|
|
| 叙述 | 石椁主要成分为汉白玉,需注意防酸雨腐蚀 | 漆画中使用的天然漆属于有机化合物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 化学与生活、生产和社会发展密切相关。下列说法正确的是
| A.医用口罩所用的熔喷布是一种聚丙烯材料,聚丙烯可以使溴水褪色 |
| B.用二氧化硅可以制成计算机、通信设备和家用电器等的芯片 |
C. 能将某些色素氧化褪色,可用作有色布匹的漂白剂 能将某些色素氧化褪色,可用作有色布匹的漂白剂 |
| D.液氨汽化时吸收大量热,可用作制冷剂 |
您最近一年使用:0次
解题方法
7 . 下列对硅及其化合物的有关叙述正确的是
| A.二氧化硅与烧碱溶液和氢氟酸均能反应,故其是两性氧化物 |
| B.晶体硅的化学性质不活泼,常温下不与任何物质发生反应 |
| C.硅酸钠的水溶液俗称水玻璃,可用作黏合剂和防火剂 |
| D.氮化硅熔点高,硬度大,可导电,化学性质稳定,是优异的非金属材料 |
您最近一年使用:0次
解题方法
8 . 某化学反应中的能量变化如图所示。下列说法正确的是
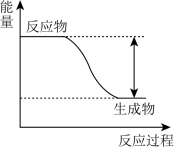
| A.该反应一定可以设计成原电池 |
| B.该反应不需要加热就一定可以发生 |
| C.该图像可以表示中和反应的能量变化 |
| D.反应中断键吸收的能量大于形成化学键放出的能量 |
您最近一年使用:0次
9 . 氮氧化物是主要的大气污染物之一,可用一氧化碳或活性炭还原氮氧化物,减少大气污染。回答下列问题:
(1)一定条件下,CO与NO反应生成两种无污染的气体,反应的化学方程式为2CO(g)+2NO(g)=N2(g)+2CO2(g),生成1mol N2(g),转移电子的物质的量为___________ mol,为提高该反应的化学反应速率,下列措施可行的是 ___________ (填字母)。
A.压缩容器体积 B.降低温度 C.使用合适催化剂 D.恒温恒容充入稀有气体
(2)两个10L的密闭容器中分别都加入活性炭(足量)和1.0mol NO,发生反应:C(s)+2NO(g)=N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见下表:
①T1℃时,0~5min内,反应速率v(CO2)=___________ mol•L-1•min-1。
②T2℃时,按表中数据,反应一定达到化学平衡状态的时间段是___________ min~10min,此时,容器中CO2的物质的量浓度是___________ mol•L-1,NO的平衡转化率为___________ 。
③两容器中温度关系为T1___________ (填“>”“<”或“=”)T2。
(1)一定条件下,CO与NO反应生成两种无污染的气体,反应的化学方程式为2CO(g)+2NO(g)=N2(g)+2CO2(g),生成1mol N2(g),转移电子的物质的量为
A.压缩容器体积 B.降低温度 C.使用合适催化剂 D.恒温恒容充入稀有气体
(2)两个10L的密闭容器中分别都加入活性炭(足量)和1.0mol NO,发生反应:C(s)+2NO(g)=N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见下表:
| 物质的量/mol | 容器1(T1/℃) | 容器2(T2/℃) | |||||||
| 0 | 5min | 9min | 10min | 12min | 0 | 5min | 9min | 10min | |
| NO | 1.0 | 0.58 | 0.42 | 0.40 | 0.40 | 1.0 | 0.50 | 0.34 | 0.34 |
| N2 | 0 | 0.21 | 0.29 | 0.30 | 0.30 | 0 | 0.25 | 0.33 | 0.33 |
②T2℃时,按表中数据,反应一定达到化学平衡状态的时间段是
③两容器中温度关系为T1
您最近一年使用:0次
10 . NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2LSO2含质子数为16NA |
| B.1molN2与3molH2充分反应,生成NH3分子数目为2NA |
| C.64gCu与足量浓硫酸反应,被还原H2SO4数目为2NA |
| D.1molNH4HCO3与足量NaOH溶液充分反应,消耗OH﹣的数目为NA |
您最近一年使用:0次







