名校
1 . 海洋是一个巨大的化学资源宝库,含有80多种元素,其中含有较高的钠和氯元素。化学家常用廉价氯化钠为原料制备纯碱,也可用于电解法获得金属钠、氯气、氢气等,并进一步将其转化为生产、生活和科学实验中用途更为广泛的新物质,如 、
、 、
、 等。下列物质性质与用途正确且具有对应关系的是
等。下列物质性质与用途正确且具有对应关系的是
 、
、 、
、 等。下列物质性质与用途正确且具有对应关系的是
等。下列物质性质与用途正确且具有对应关系的是A. 溶液显碱性,可用作抗酸药物 溶液显碱性,可用作抗酸药物 |
B. 气体呈黄绿色,可用作自来水消毒剂 气体呈黄绿色,可用作自来水消毒剂 |
C. 具有还原性,可置换出 具有还原性,可置换出 溶液中的 溶液中的 单质 单质 |
| D.NaClO具有强氧化性,可用作漂白液 |
您最近一年使用:0次
名校
解题方法
2 . 下列化学用语表达正确的是
A.F原子的核外电子排布式: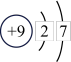 | B. 的轨道表示式: 的轨道表示式: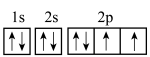 |
C. 分子的结构式: 分子的结构式: | D.Mn的简化电子排布式:[Ar]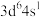 |
您最近一年使用:0次
3 . 下列关于外围电子排布式为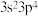 的基态原子的描述正确的是
的基态原子的描述正确的是
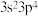 的基态原子的描述正确的是
的基态原子的描述正确的是| A.它的原子核外有三种形状不同的电子云 | B.它的原子核外电子共有16种不同的运动状态 |
C.它可与 反应生成常温时的液态化合物 反应生成常温时的液态化合物 | D.该原子位于d区 |
您最近一年使用:0次
名校
4 . 下列物质的性质与用途相对应的是
| A.浓硫酸具有难挥发性,可用于制备HCl气体 |
B. 具有强氧化性,能与 具有强氧化性,能与 反应制备硝酸铵 反应制备硝酸铵 |
C. 难溶于水,可用作钡餐 难溶于水,可用作钡餐 |
D. 溶液显碱性,可用于制抗酸药物 溶液显碱性,可用于制抗酸药物 |
您最近一年使用:0次
5 .  是绿色氧化剂,可利用反应
是绿色氧化剂,可利用反应 制取
制取 ,下列说法正确的是
,下列说法正确的是
 是绿色氧化剂,可利用反应
是绿色氧化剂,可利用反应 制取
制取 ,下列说法正确的是
,下列说法正确的是A.基态Na原子外围电子排布式为 |
B.基态O原子的轨道表示式: |
C. 的电子式: 的电子式: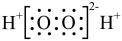 |
D. 是由极性键构成的极性分子 是由极性键构成的极性分子 |
您最近一年使用:0次
解题方法
6 . 下列方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究浓硫酸的特性 | 将浓硫酸滴到蔗糖表面,固体变黑膨胀,有刺激性气体产生 | 浓硫酸有脱水性和强氧化性 |
| B | 检验 和浓盐酸反应后是否有酸剩余 和浓盐酸反应后是否有酸剩余 | 取少量反应后的溶液于试管中,依次加入稀硝酸、 溶液,观察 溶液,观察 | 若产生大量白色沉淀,则说明盐酸有剩余 |
| C | 证明 有氧化性 有氧化性 | 将足量的 溶液滴入酸性高锰酸钾溶液中 溶液滴入酸性高锰酸钾溶液中 | 若溶液中的紫红色褪去,则证明 有氧化性 有氧化性 |
| D | 鉴别两种红棕色气体 和 和 | 向盛有 淀粉溶液的试管中通入气体 淀粉溶液的试管中通入气体 | 溶液变成蓝色,说明该气体是 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 在给定条件下,下列选项中所示的物质间转化均能实现的是
A.饱和NaCl溶液制备纯碱:饱和NaCl溶液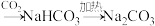 |
B.由S制备 : :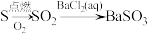 |
C.由 生成 生成 : : |
D. 的生成: 的生成: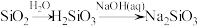 |
您最近一年使用:0次
解题方法
8 . 下列化学反应表示正确的是
A.稀 和氨水的稀溶液反应的热化学方程式为: 和氨水的稀溶液反应的热化学方程式为: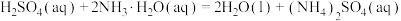 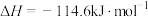 |
B.火箭发射时 和 和 反应: 反应: |
C.锂离子电池放电时的正极反应: |
D.两性氧化物 溶于NaOH溶液的反应: 溶于NaOH溶液的反应: |
您最近一年使用:0次
9 . 化合物G(萘丁美酮)是一种解热、镇痛药,其合成路线如图:___________ 、___________ 和醚键。
(2)可以鉴别B、C两种物质的试剂为___________ 。
(3)C→D过程中依次经历了___________ 和___________ 反应。
(4)C的一种同分异构体同时满足下列条件,该同分异构体的结构简式为___________ 。
①分子中含苯环,能使Br2的CCl4溶液褪色;
②分子中不同化学环境的氢原子数目之比为2∶3。
(5)已知2CH3CHO CH3CH=CHCHO。写出以
CH3CH=CHCHO。写出以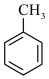 、
、 和CH3CH2OH为原料制备
和CH3CH2OH为原料制备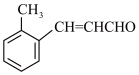 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。___________

(2)可以鉴别B、C两种物质的试剂为
(3)C→D过程中依次经历了
(4)C的一种同分异构体同时满足下列条件,该同分异构体的结构简式为
①分子中含苯环,能使Br2的CCl4溶液褪色;
②分子中不同化学环境的氢原子数目之比为2∶3。
(5)已知2CH3CHO
 CH3CH=CHCHO。写出以
CH3CH=CHCHO。写出以 、
、 和CH3CH2OH为原料制备
和CH3CH2OH为原料制备 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
您最近一年使用:0次
解题方法
10 . 下列说法正确的是
| A.已知H+(aq)+OH-(aq)=H2O(l) ΔH=−57.3kJ∙mol−1,在中和热的测定时实际加入的酸碱的量的多少会影响该反应的ΔH |
| B.1mol H2与0.5mol O2反应放出的热量就是H2的燃烧热 |
| C.加入催化剂可以改变反应的活化能,不能改变焓变 |
D.500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) ∆H=−38.6kJ∙mol−1 2NH3(g) ∆H=−38.6kJ∙mol−1 |
您最近一年使用:0次



