名校
解题方法
1 . 下列化学用语表达正确的是
A.F原子的核外电子排布式: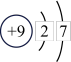 | B. 的轨道表示式: 的轨道表示式: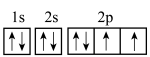 |
C. 分子的结构式: 分子的结构式: | D.Mn的简化电子排布式:[Ar]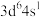 |
您最近一年使用:0次
名校
解题方法
2 . 向含 、
、 、
、 的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
 、
、 、
、 的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
A.原溶液中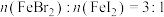 | B.线段II表示 的变化情况 的变化情况 |
C.线段IV表示 的变化情况 的变化情况 | D.根据图像可计算出a=5 |
您最近一年使用:0次
名校
3 . 工厂烟气(主要污染物NO)直接排放会造成空气污染,需处理后才能排放。“纳米零价铁— ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。
。
(1)制备纳米零价铁将 溶液与碱性
溶液与碱性 溶液混合可生成纳米零价铁、
溶液混合可生成纳米零价铁、 和
和 等。
等。
 中
中 电子排布式为
电子排布式为___________ 。
(2)NO的氧化:在一定温度下,将 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①X催化 分解产生HO·,HO·将NO氧化为
分解产生HO·,HO·将NO氧化为 的机理如图所示,则Y的化学式为
的机理如图所示,则Y的化学式为___________ ,纳米零价铁的作用是___________ 。___________ 。
③ 与Y反应可实现X再生,同时产生
与Y反应可实现X再生,同时产生 ,写出
,写出 的电子式
的电子式___________ ,此时 作为
作为___________ 剂。
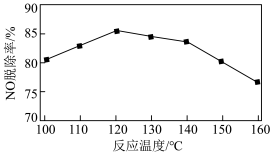
④NO脱除率随温度的变化如下图所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是___________ 。 表示),可大致分为2个过程,反应原理如下图所示。
表示),可大致分为2个过程,反应原理如下图所示。___________ 。
 ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。
。(1)制备纳米零价铁将
 溶液与碱性
溶液与碱性 溶液混合可生成纳米零价铁、
溶液混合可生成纳米零价铁、 和
和 等。
等。 中
中 电子排布式为
电子排布式为(2)NO的氧化:在一定温度下,将
 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。①X催化
 分解产生HO·,HO·将NO氧化为
分解产生HO·,HO·将NO氧化为 的机理如图所示,则Y的化学式为
的机理如图所示,则Y的化学式为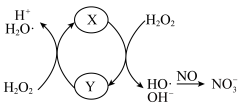
③
 与Y反应可实现X再生,同时产生
与Y反应可实现X再生,同时产生 ,写出
,写出 的电子式
的电子式 作为
作为④NO脱除率随温度的变化如下图所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是
 表示),可大致分为2个过程,反应原理如下图所示。
表示),可大致分为2个过程,反应原理如下图所示。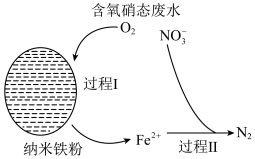
您最近一年使用:0次
名校
4 . 高砷煤中含有砷硫铁(FeAsS)等物质。燃煤产生的烟气中含NO、 、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
(1)燃煤固硫
①燃烧高砷煤时加入生石灰将大部分硫元素转化为___________ (填化学式)留在煤渣中。
②高砷煤燃烧过程中,砷硫铁在高温下被氧化成 释放到烟气中,该反应的化学方程式为
释放到烟气中,该反应的化学方程式为___________ 。
(2)SCR脱硝(脱除烟气中的NO)
在烟气中加入适量氨气,用钒氧化物作催化剂将 、NO、
、NO、 转化为
转化为 。
。
①在SCR脱硝的反应中还原剂为___________ (填化学式)。
②若 与NO的物质的量之比为1∶1,写出SCR脱硝法的反应原理
与NO的物质的量之比为1∶1,写出SCR脱硝法的反应原理___________ (用化学方程式表示)。
(3)粉煤灰成分研究
粉煤灰可用于水泥工业,粉煤灰中的氨含量( 或铵盐)会影响水泥的性能。取50.00g粉煤灰加入NaOH蒸出
或铵盐)会影响水泥的性能。取50.00g粉煤灰加入NaOH蒸出 ,用20mL 0.1000
,用20mL 0.1000 的
的 溶液吸收
溶液吸收 ,用0.200
,用0.200 NaOH溶液滴定过量的
NaOH溶液滴定过量的 至终点,平行滴定3次,平均消耗NaOH溶液10.00mL,计算粉煤灰中的以
至终点,平行滴定3次,平均消耗NaOH溶液10.00mL,计算粉煤灰中的以 计的氨含量
计的氨含量___________ (用 表示,写出计算过程)。
表示,写出计算过程)。
 、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。
、粉尘等,经过SCR脱硝除去NO,粉尘经沉降得到粉煤灰。(1)燃煤固硫
①燃烧高砷煤时加入生石灰将大部分硫元素转化为
②高砷煤燃烧过程中,砷硫铁在高温下被氧化成
 释放到烟气中,该反应的化学方程式为
释放到烟气中,该反应的化学方程式为(2)SCR脱硝(脱除烟气中的NO)
在烟气中加入适量氨气,用钒氧化物作催化剂将
 、NO、
、NO、 转化为
转化为 。
。①在SCR脱硝的反应中还原剂为
②若
 与NO的物质的量之比为1∶1,写出SCR脱硝法的反应原理
与NO的物质的量之比为1∶1,写出SCR脱硝法的反应原理(3)粉煤灰成分研究
粉煤灰可用于水泥工业,粉煤灰中的氨含量(
 或铵盐)会影响水泥的性能。取50.00g粉煤灰加入NaOH蒸出
或铵盐)会影响水泥的性能。取50.00g粉煤灰加入NaOH蒸出 ,用20mL 0.1000
,用20mL 0.1000 的
的 溶液吸收
溶液吸收 ,用0.200
,用0.200 NaOH溶液滴定过量的
NaOH溶液滴定过量的 至终点,平行滴定3次,平均消耗NaOH溶液10.00mL,计算粉煤灰中的以
至终点,平行滴定3次,平均消耗NaOH溶液10.00mL,计算粉煤灰中的以 计的氨含量
计的氨含量 表示,写出计算过程)。
表示,写出计算过程)。
您最近一年使用:0次
名校
5 . 铬是一种具有战略意义的金属,它具有多种价态,单质铬熔点为1857℃。工业上以铬铁矿[主要成分是 ]为原料冶炼铬的流程如图所示:
]为原料冶炼铬的流程如图所示: 中各元素化合价均为整数,则铬的化合价为
中各元素化合价均为整数,则铬的化合价为___________ ,写出基态铬原子的外围电子排布式___________ 。
(2)操作a由两步反应构成,其分别是①___________ 、②与铝粉混合高温下发生铝热反应。
(3) 是两性氢氧化物,写出其与NaOH反应的离子方程式
是两性氢氧化物,写出其与NaOH反应的离子方程式___________ 。
(4)水中的铬元素对水质及环境均有严重的损害作用,必须进行无害化处理。转化为重要产品磁性铁铬氧体(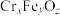 ):先向含
):先向含 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分 )并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
①写出 在酸性条件下被
在酸性条件下被 还原为
还原为 的离子方程式
的离子方程式___________ 。
②若处理含1mol (不考虑其他含铬微粒)的污水时恰好消耗10mol
(不考虑其他含铬微粒)的污水时恰好消耗10mol  ,则当铁铬氧体中
,则当铁铬氧体中 时,则铁铬氧体的化学式为
时,则铁铬氧体的化学式为___________ 。
 ]为原料冶炼铬的流程如图所示:
]为原料冶炼铬的流程如图所示: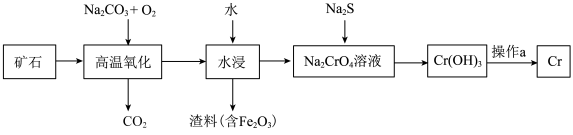
 中各元素化合价均为整数,则铬的化合价为
中各元素化合价均为整数,则铬的化合价为(2)操作a由两步反应构成,其分别是①
(3)
 是两性氢氧化物,写出其与NaOH反应的离子方程式
是两性氢氧化物,写出其与NaOH反应的离子方程式(4)水中的铬元素对水质及环境均有严重的损害作用,必须进行无害化处理。转化为重要产品磁性铁铬氧体(
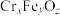 ):先向含
):先向含 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分 )并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。①写出
 在酸性条件下被
在酸性条件下被 还原为
还原为 的离子方程式
的离子方程式②若处理含1mol
 (不考虑其他含铬微粒)的污水时恰好消耗10mol
(不考虑其他含铬微粒)的污水时恰好消耗10mol  ,则当铁铬氧体中
,则当铁铬氧体中 时,则铁铬氧体的化学式为
时,则铁铬氧体的化学式为
您最近一年使用:0次
名校
6 . 按要求填空。
(1)已知钴元素在周期表中的信息如下,回答下列问题:___________ ,基态原子核外有___________ 种不同运动状态的电子,画出该原子的原子结构示意图___________ 。
(2)已知高温下 比CuO更稳定,试从核外电子排布角度解释原因
比CuO更稳定,试从核外电子排布角度解释原因___________ 。
(3)氰化钾是一种剧毒物质,贮存和使用时必须注意安全。已知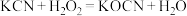 ,则
,则 中所含三种元素的电负性由大到小的顺序为
中所含三种元素的电负性由大到小的顺序为___________ (用元素符号表示,下同),第一电离能从大到小顺序为___________ ,基态氮原子的电子排布式为___________ ,其能量最高的电子所在原子轨道的电子云轮廓图为___________ 形。
(1)已知钴元素在周期表中的信息如下,回答下列问题:

(2)已知高温下
 比CuO更稳定,试从核外电子排布角度解释原因
比CuO更稳定,试从核外电子排布角度解释原因(3)氰化钾是一种剧毒物质,贮存和使用时必须注意安全。已知
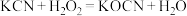 ,则
,则 中所含三种元素的电负性由大到小的顺序为
中所含三种元素的电负性由大到小的顺序为
您最近一年使用:0次
名校
7 .  可用于制铁盐、兽药,与砂糖混用为补血剂,其工艺生产流程如下:
可用于制铁盐、兽药,与砂糖混用为补血剂,其工艺生产流程如下:
 可用于制铁盐、兽药,与砂糖混用为补血剂,其工艺生产流程如下:
可用于制铁盐、兽药,与砂糖混用为补血剂,其工艺生产流程如下: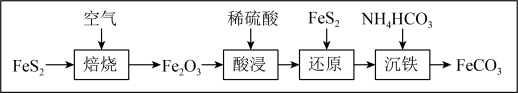
A.“焙烧”时,将 粉碎可提高焙烧效率 粉碎可提高焙烧效率 |
| B.“焙烧”过程中氧化剂和还原剂的物质的量之比为11∶4 |
C.“还原”工序中,反应的离子方程式为: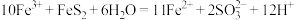 |
D.“沉铁”时,有 生成 生成 |
您最近一年使用:0次
名校
8 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作 | 结论 |
| A | 将铁锈溶于浓盐酸,再滴入 溶液,紫红色褪去 溶液,紫红色褪去 | 铁锈与浓盐酸反应生成亚铁离子 |
| B | 用洁净的铂丝蘸取溶液在火焰上灼烧,火焰呈黄色 | 溶液中一定有钠元素,可能有钾元素 |
| C | 向 和KSCN的混合溶液中滴入酸化的 和KSCN的混合溶液中滴入酸化的 溶液,观察溶液颜色的变化 溶液,观察溶液颜色的变化 |  的氧化性强于 的氧化性强于 |
| D | 将 通入 通入 溶液后,将混合气体依次通入酸性 溶液后,将混合气体依次通入酸性 溶液、品红溶液、澄清石灰水 溶液、品红溶液、澄清石灰水 | 验证非金属性:S>C |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 某钒催化剂在一定条件下形成相邻的氧化还原位和酸性吸附位,该催化剂催化 脱除电厂烟气中NO的反应机理如图所示。
脱除电厂烟气中NO的反应机理如图所示。
 脱除电厂烟气中NO的反应机理如图所示。
脱除电厂烟气中NO的反应机理如图所示。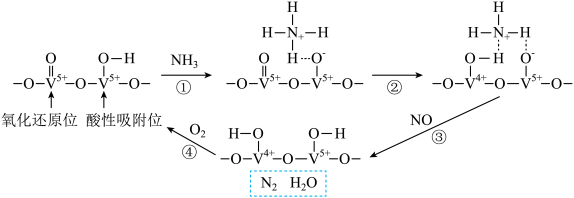
| A.反应①~④均为氧化还原反应 |
B.消耗1mol  ,理论上可处理2mol NO ,理论上可处理2mol NO |
C.反应②为 |
D.总反应方程式 |
您最近一年使用:0次
名校
10 . X、Y、Z、W、Q、R均为元素周期表前四周期元素,原子序数依次增大。X的基态原子中,电子排布在三个不同的能级,且每个能级的电子总数相等。Y的2p轨道有3个未成对电子。Z的族序数是其周期序数的3倍。W原子的第一至第六电离能分别为 ,
,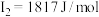 ,
, ,
, ,
, ,
,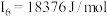 。Q在前四周期中电负性最小。R位于元素周期表第11列。下列说法正确的是
。Q在前四周期中电负性最小。R位于元素周期表第11列。下列说法正确的是
 ,
,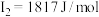 ,
, ,
, ,
, ,
,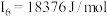 。Q在前四周期中电负性最小。R位于元素周期表第11列。下列说法正确的是
。Q在前四周期中电负性最小。R位于元素周期表第11列。下列说法正确的是| A.原子半径:X<Y<Z | B.W的氢化物为 |
| C.Q的最高价氧化物的水化物为强碱 | D.R为主族元素 |
您最近一年使用:0次



