名校
解题方法
1 . 室温下,向 溶液中加入足量氨水
溶液中加入足量氨水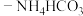 混合溶液,生成
混合溶液,生成 沉淀。已知:
沉淀。已知: ,
,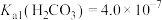 ,
,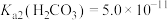 。下列说法正确的是
。下列说法正确的是
 溶液中加入足量氨水
溶液中加入足量氨水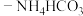 混合溶液,生成
混合溶液,生成 沉淀。已知:
沉淀。已知: ,
,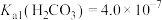 ,
,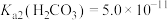 。下列说法正确的是
。下列说法正确的是A.生成 的离子方程式: 的离子方程式: |
B.0.1   溶液中:( 溶液中:( ): ):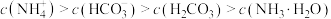 |
C.0.2  氨水和0.2 氨水和0.2   溶液等体积混合: 溶液等体积混合: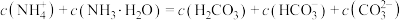 |
D.生成 沉淀后的滤液中: 沉淀后的滤液中: |
您最近一年使用:0次
昨日更新
|
279次组卷
|
3卷引用:江苏省南通市海安高级中学2024届高三下学期第二次模拟考试化学试题
名校
2 . PtNiFe—LDHGO催化甲醛氧化的反应机理如图:
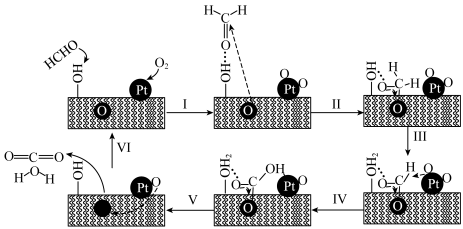
A.步骤Ⅰ中甲醛通过氢键吸附在催化剂表面的 上 上 |
| B.上述反应机理涉及极性键和非极性键的形成 |
C.该反应每生成1 mol ,转移电子的数目约为 ,转移电子的数目约为 |
| D.PtNiFe—LDHGO降低了该反应的活化能 |
您最近一年使用:0次
昨日更新
|
272次组卷
|
2卷引用:江苏省南通市海安高级中学2024届高三下学期第二次模拟考试化学试题
解题方法
3 . 元素N、O、P、S位于周期表中p区。下列说法正确的是
A.电离能:  | B.原子半径:  |
C.酸性:  | D.热稳定性: 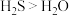 |
您最近一年使用:0次
昨日更新
|
45次组卷
|
2卷引用:江苏省南通市2024届高三下学期模拟预测化学试题
名校
解题方法
4 . 肼( )是一种含氢量高的燃料。向恒容密闭容器内加入3 mol
)是一种含氢量高的燃料。向恒容密闭容器内加入3 mol ,一定条件下体系中
,一定条件下体系中 催化分解存在以下平衡:
催化分解存在以下平衡:
 .
.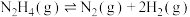 ;
;
 .
.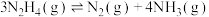 。
。
不同温度下达到平衡时, 均几乎完全分解,分解产物的物质的量如图。
均几乎完全分解,分解产物的物质的量如图。
 )是一种含氢量高的燃料。向恒容密闭容器内加入3 mol
)是一种含氢量高的燃料。向恒容密闭容器内加入3 mol ,一定条件下体系中
,一定条件下体系中 催化分解存在以下平衡:
催化分解存在以下平衡: .
.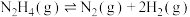 ;
; .
.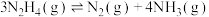 。
。不同温度下达到平衡时,
 均几乎完全分解,分解产物的物质的量如图。
均几乎完全分解,分解产物的物质的量如图。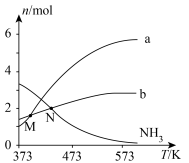
A.曲线a对应的物质是 |
| B.低于M点对应温度时,以反应Ⅰ为主 |
C.体系中一定不存在反应: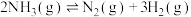 |
D.N点时,体系内: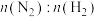 为2∶3 为2∶3 |
您最近一年使用:0次
名校
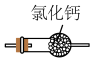
5 . 实验室制备NH3的实验原理及装置均正确的是
|
|
| A.制取氨气 | B.干燥氨气 |
|
|
| C.收集氨气 | D.吸收氨气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
488次组卷
|
2卷引用:江苏省南通市海安高级中学2024届高三下学期第二次模拟考试化学试题
名校
解题方法
6 . 乙烯年产量是衡量国家石油化工发展水平的重要指标,乙烷制乙烯具有极高的经济效益。
已知:i.乙烷裂解为乙烯为自由基反应,其可能的引发反应及对应化学键的解离能如下:
ii.乙烷裂解中主要发生的反应及其在不同温度下的平衡常数如下表:
(1)乙烷直接裂解制乙烯。
①引发乙烷直接裂解的反应主要为___________ 。
②不采用乙烷直接裂解制乙烯裂解原因是___________ 。
(2)乙烷催化氧化脱氢制乙烯。
已知:i.
 kJ·mol
kJ·mol ;
;
ii.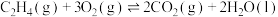
 kJ·mol
kJ·mol ;
;
①则
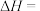
___________ 。
800℃时,当 和
和 的混合气以一定流速通过反应器时,混合气中
的混合气以一定流速通过反应器时,混合气中 的比值对乙烷氧化裂解制乙烯的反应中乙烷转化率、乙烯选择性、乙烯收率的影响如图所示:
的比值对乙烷氧化裂解制乙烯的反应中乙烷转化率、乙烯选择性、乙烯收率的影响如图所示: 时,
时,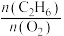 越小,乙烷转化率越大,但乙烯的选择性越小的原因是
越小,乙烷转化率越大,但乙烯的选择性越小的原因是___________ 。
(3) 耦合乙烷催化脱氢制乙烯。
耦合乙烷催化脱氢制乙烯。
①用Cr/SSZ-13为催化剂、 作为温和的氧化剂用于乙烷脱氢制备乙烯有诸多优势。催化条件下,乙烷裂解主要引发反应为反应
作为温和的氧化剂用于乙烷脱氢制备乙烯有诸多优势。催化条件下,乙烷裂解主要引发反应为反应 ,同时Cr的价态由+3升高+4.推测配位不饱和
,同时Cr的价态由+3升高+4.推测配位不饱和 催化
催化 耦合
耦合 脱氢反应过程如图所示,补全图中画框部分。
脱氢反应过程如图所示,补全图中画框部分。___________  代替
代替 的优势为
的优势为___________ 。
(4)电催化乙烷催化脱氢制乙烯。
利用质子传导型固体氧化物电解池也可实现乙烷制乙烯。乙烷在电极上直接电催化裂解为乙烯,同时质子在外加电势下经电解质“抽取”至另一极与 反应生成CO,阳极的电极方程式为
反应生成CO,阳极的电极方程式为___________ 。
已知:i.乙烷裂解为乙烯为自由基反应,其可能的引发反应及对应化学键的解离能如下:
| 可能的引发反应 | 有关键的解离能(kJ/mol) |
 . .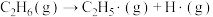 | 410 |
 . .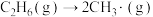 | 368 |
| 反应 | 1100K | 1300K | 1500K |
 . .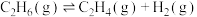 | 1.6 | 18.9 | 72.0 |
 . .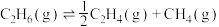 | 60.9 | 108.7 | 165.8 |
 . .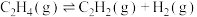 | 0.015 | 0.33 | 3.2 |
 . .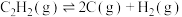 |  |  | 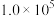 |
(1)乙烷直接裂解制乙烯。
①引发乙烷直接裂解的反应主要为
②不采用乙烷直接裂解制乙烯裂解原因是
(2)乙烷催化氧化脱氢制乙烯。
已知:i.

 kJ·mol
kJ·mol ;
;ii.
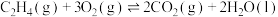
 kJ·mol
kJ·mol ;
;①则

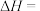
800℃时,当
 和
和 的混合气以一定流速通过反应器时,混合气中
的混合气以一定流速通过反应器时,混合气中 的比值对乙烷氧化裂解制乙烯的反应中乙烷转化率、乙烯选择性、乙烯收率的影响如图所示:
的比值对乙烷氧化裂解制乙烯的反应中乙烷转化率、乙烯选择性、乙烯收率的影响如图所示: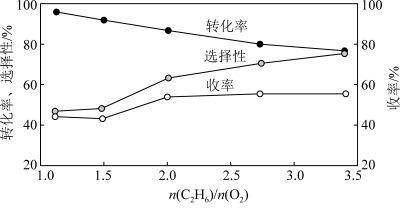
 时,
时,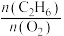 越小,乙烷转化率越大,但乙烯的选择性越小的原因是
越小,乙烷转化率越大,但乙烯的选择性越小的原因是(3)
 耦合乙烷催化脱氢制乙烯。
耦合乙烷催化脱氢制乙烯。①用Cr/SSZ-13为催化剂、
 作为温和的氧化剂用于乙烷脱氢制备乙烯有诸多优势。催化条件下,乙烷裂解主要引发反应为反应
作为温和的氧化剂用于乙烷脱氢制备乙烯有诸多优势。催化条件下,乙烷裂解主要引发反应为反应 ,同时Cr的价态由+3升高+4.推测配位不饱和
,同时Cr的价态由+3升高+4.推测配位不饱和 催化
催化 耦合
耦合 脱氢反应过程如图所示,补全图中画框部分。
脱氢反应过程如图所示,补全图中画框部分。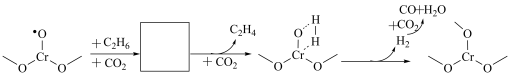
 代替
代替 的优势为
的优势为(4)电催化乙烷催化脱氢制乙烯。
利用质子传导型固体氧化物电解池也可实现乙烷制乙烯。乙烷在电极上直接电催化裂解为乙烯,同时质子在外加电势下经电解质“抽取”至另一极与
 反应生成CO,阳极的电极方程式为
反应生成CO,阳极的电极方程式为
您最近一年使用:0次
名校
7 .  是重要漂白剂和消毒剂,主要用于水、砂糖、油脂的漂白杀菌。实验室制备
是重要漂白剂和消毒剂,主要用于水、砂糖、油脂的漂白杀菌。实验室制备 装置如图1所示。
装置如图1所示。 的溶解度曲线如图2所示;若溶液温度高于60℃,
的溶解度曲线如图2所示;若溶液温度高于60℃, 发生分解。
发生分解。
ii. 气体浓度超过10%时,易发生爆炸性分解。
气体浓度超过10%时,易发生爆炸性分解。 (浓)
(浓)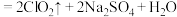 。
。
(1)下列实验操作一定能提高 吸收效率的有___________。(填序号)
吸收效率的有___________。(填序号)
(2)试管C中获得的产品往往混有 杂质,其原因是
杂质,其原因是___________ 。
(3)反应过程中,打开 ,并缓慢鼓入
,并缓慢鼓入 的目的是
的目的是___________ 。
(4)反应结束后,补充完整制取 晶体的实验方案:取试管C中的溶液,
晶体的实验方案:取试管C中的溶液,___________ ,低温干燥,得到 晶体。(实验中须使用稀盐酸、
晶体。(实验中须使用稀盐酸、 溶液、蒸馏水)
溶液、蒸馏水)
(5)产品中 质量分数的测定:称取5.000g产品配成250mL溶液;取25.00mL所配溶液,加入足量KI溶液和稀硫酸,发生反应:
质量分数的测定:称取5.000g产品配成250mL溶液;取25.00mL所配溶液,加入足量KI溶液和稀硫酸,发生反应: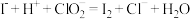 ;向充分反应后的混合物中逐滴加入0.8400
;向充分反应后的混合物中逐滴加入0.8400 
 溶液至恰好完全反应:
溶液至恰好完全反应: (方程式均未配平),消耗
(方程式均未配平),消耗 溶液20.00 mL。
溶液20.00 mL。
①若加入KI溶液后在空气中放置时间过长,会导致测得的 质量分数
质量分数___________ (填“偏高”“偏低”或“无影响”)。
②已知产品中的杂质不与KI、 发生反应。产品中
发生反应。产品中 的质量分数为
的质量分数为___________ 。
 是重要漂白剂和消毒剂,主要用于水、砂糖、油脂的漂白杀菌。实验室制备
是重要漂白剂和消毒剂,主要用于水、砂糖、油脂的漂白杀菌。实验室制备 装置如图1所示。
装置如图1所示。
 的溶解度曲线如图2所示;若溶液温度高于60℃,
的溶解度曲线如图2所示;若溶液温度高于60℃, 发生分解。
发生分解。ii.
 气体浓度超过10%时,易发生爆炸性分解。
气体浓度超过10%时,易发生爆炸性分解。
 (浓)
(浓)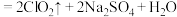 。
。(1)下列实验操作一定能提高
 吸收效率的有___________。(填序号)
吸收效率的有___________。(填序号)| A.装置C采用热水浴 | B.加快滴加浓硫酸的速率 |
C.适当提高 的浓度 的浓度 | D.通过多孔球泡向C的混合溶液中通 |
(2)试管C中获得的产品往往混有
 杂质,其原因是
杂质,其原因是(3)反应过程中,打开
 ,并缓慢鼓入
,并缓慢鼓入 的目的是
的目的是(4)反应结束后,补充完整制取
 晶体的实验方案:取试管C中的溶液,
晶体的实验方案:取试管C中的溶液, 晶体。(实验中须使用稀盐酸、
晶体。(实验中须使用稀盐酸、 溶液、蒸馏水)
溶液、蒸馏水)(5)产品中
 质量分数的测定:称取5.000g产品配成250mL溶液;取25.00mL所配溶液,加入足量KI溶液和稀硫酸,发生反应:
质量分数的测定:称取5.000g产品配成250mL溶液;取25.00mL所配溶液,加入足量KI溶液和稀硫酸,发生反应: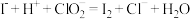 ;向充分反应后的混合物中逐滴加入0.8400
;向充分反应后的混合物中逐滴加入0.8400 
 溶液至恰好完全反应:
溶液至恰好完全反应: (方程式均未配平),消耗
(方程式均未配平),消耗 溶液20.00 mL。
溶液20.00 mL。①若加入KI溶液后在空气中放置时间过长,会导致测得的
 质量分数
质量分数②已知产品中的杂质不与KI、
 发生反应。产品中
发生反应。产品中 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
8 . 氯霉素(H)的一种合成路线如下:
(1)A→B反应中,碳原子的杂化轨道类型的变化为___________ 。
(2)B→C的反应类型为___________ 。
(3)D的分子式为C10H11BrO2,其结构简式为___________ 。
(4)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式___________ 。
能与FeCl3溶液发生显色反应;
核磁共振氢谱有5个峰;
能发生水解反应;苯环上的一溴代物只有一种。
(5)物质E在水中的溶解度比F___________ (填“大”、“小”或“无差别”)。
(6)写出以乙烯为主要原料制备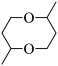 的合成路线流程图
的合成路线流程图___________ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。

(1)A→B反应中,碳原子的杂化轨道类型的变化为
(2)B→C的反应类型为
(3)D的分子式为C10H11BrO2,其结构简式为
(4)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式
能与FeCl3溶液发生显色反应;
核磁共振氢谱有5个峰;
能发生水解反应;苯环上的一溴代物只有一种。
(5)物质E在水中的溶解度比F
(6)写出以乙烯为主要原料制备
 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
9 . 用过二硫酸铵 溶液作浸取剂可以提取黄铜矿(主要成分为
溶液作浸取剂可以提取黄铜矿(主要成分为 )中的铜。
)中的铜。
已知:i. 、
、 均能导电;
均能导电;
ii. ;
;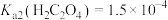 ;
;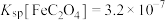
(1) 的晶胞如图1所示。
的晶胞如图1所示。 晶胞,则每个
晶胞,则每个 晶胞中含有的Fe原子个数为
晶胞中含有的Fe原子个数为___________ 。
②图2所示结构单元不能作为 晶胞的原因是
晶胞的原因是___________ 。
(2)用 溶液作浸取剂浸取
溶液作浸取剂浸取 的原理示意如图3所示。
的原理示意如图3所示。
①一段时间后, 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
②浸取初期,随着浸取时间延长, 的浸出速率迅速提高,其可能的原因是
的浸出速率迅速提高,其可能的原因是___________ 。
(3)在足量 溶液中添加少量
溶液中添加少量 溶液作为浸取剂与
溶液作为浸取剂与 作用,一段时间结果如下:
作用,一段时间结果如下:
①添加Ag⁺可以显著提高Cu元素的浸出率的原因:___________ 。
②进一步研究发现添加的少量 可以循环参与反应。
可以循环参与反应。 “再生”的离子方程式为:
“再生”的离子方程式为:___________ 。
(4)进一步从浸出液中提取铜并使 再生的流程示意图如图4所示。
再生的流程示意图如图4所示。
①滤液A中加草酸的反应为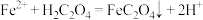 ,该反应化学平衡常数为
,该反应化学平衡常数为___________ 。
②电解滤液B而不电解滤液A的原因是___________ 。
 溶液作浸取剂可以提取黄铜矿(主要成分为
溶液作浸取剂可以提取黄铜矿(主要成分为 )中的铜。
)中的铜。已知:i.
 、
、 均能导电;
均能导电;ii.
 ;
;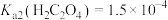 ;
;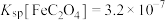
(1)
 的晶胞如图1所示。
的晶胞如图1所示。
 晶胞,则每个
晶胞,则每个 晶胞中含有的Fe原子个数为
晶胞中含有的Fe原子个数为②图2所示结构单元不能作为
 晶胞的原因是
晶胞的原因是(2)用
 溶液作浸取剂浸取
溶液作浸取剂浸取 的原理示意如图3所示。
的原理示意如图3所示。
①一段时间后,
 与
与 反应的离子方程式为
反应的离子方程式为②浸取初期,随着浸取时间延长,
 的浸出速率迅速提高,其可能的原因是
的浸出速率迅速提高,其可能的原因是(3)在足量
 溶液中添加少量
溶液中添加少量 溶液作为浸取剂与
溶液作为浸取剂与 作用,一段时间结果如下:
作用,一段时间结果如下:添加 | 未加 | |
| Cu元素的浸出率 | 98.02% | 30.90% |
| 过程中产物形态 |
|
|
②进一步研究发现添加的少量
 可以循环参与反应。
可以循环参与反应。 “再生”的离子方程式为:
“再生”的离子方程式为:(4)进一步从浸出液中提取铜并使
 再生的流程示意图如图4所示。
再生的流程示意图如图4所示。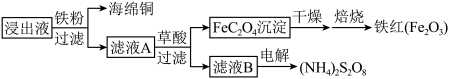
①滤液A中加草酸的反应为
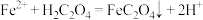 ,该反应化学平衡常数为
,该反应化学平衡常数为②电解滤液B而不电解滤液A的原因是
您最近一年使用:0次
名校
解题方法
10 . 在元素周期表中,某些主族元素与右下方的主族元素的某些性质是相似的。如: 和
和 均为两性氢氧化物,
均为两性氢氧化物, 溶于强碱形成
溶于强碱形成 ;BeO和
;BeO和 都具有难溶于水、高熔点等性质。
都具有难溶于水、高熔点等性质。 和
和 在气态时通常以二聚体的形式存在。B和Si均能溶于NaOH溶液生成盐和
在气态时通常以二聚体的形式存在。B和Si均能溶于NaOH溶液生成盐和 。工业上用焦炭和
。工业上用焦炭和 在高温下反应制粗硅。硼酸(
在高温下反应制粗硅。硼酸( )和硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构,常用作润滑剂。下列说法正确的是
)和硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构,常用作润滑剂。下列说法正确的是
 和
和 均为两性氢氧化物,
均为两性氢氧化物, 溶于强碱形成
溶于强碱形成 ;BeO和
;BeO和 都具有难溶于水、高熔点等性质。
都具有难溶于水、高熔点等性质。 和
和 在气态时通常以二聚体的形式存在。B和Si均能溶于NaOH溶液生成盐和
在气态时通常以二聚体的形式存在。B和Si均能溶于NaOH溶液生成盐和 。工业上用焦炭和
。工业上用焦炭和 在高温下反应制粗硅。硼酸(
在高温下反应制粗硅。硼酸( )和硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构,常用作润滑剂。下列说法正确的是
)和硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构,常用作润滑剂。下列说法正确的是A. 二聚体中含有配位键 二聚体中含有配位键 | B. 的空间结构为平面正方形 的空间结构为平面正方形 |
C. 中的 中的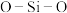 键角为180° 键角为180° | D. 晶体在常温下能导电 晶体在常温下能导电 |
您最近一年使用:0次