名校
1 . 春季早晚温差大,空气中花粉多,是湿疹的高发季节,本维莫德(G)是治疗湿疹的非激素类外用药,其合成路线如下:______ 。
(2)下列有关说法正确的是______ 。
Ⅰ.B物质核磁共振氢谱有3组吸收峰,其峰面积之比为1∶1∶2;
Ⅱ.1mol A最多可以与1mol的 反应,最多可以消耗3mol的
反应,最多可以消耗3mol的 反应;
反应;
Ⅲ.1mol A中含有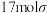 键,室温下,在水中的溶解度A比B大;
键,室温下,在水中的溶解度A比B大;
Ⅳ.G物质与足量 加成产物中有4个手性碳原子,G物质中C原子的杂化类型:
加成产物中有4个手性碳原子,G物质中C原子的杂化类型: 。
。
(3)合成路线中设置A到B,将A中酚羟基变为醚键的目的是____________ 。
(4)Y的分子式为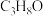 ,其结构简式为
,其结构简式为____________ ,欲确定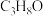 中存在C—O和O—H化学键,可采取的仪器分析方法为
中存在C—O和O—H化学键,可采取的仪器分析方法为______ (填选项)。
A.核磁共振氢谱 B.质谱 C.红外光谱 D.原子发射光谱
(5)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式____________ 。
Ⅰ.碱性条件下水解后酸化生成两种产物。
Ⅱ.一种产物含有苯环,其核磁共振氢谱只有3组峰,且峰面积之比为1∶2∶1,不能与 溶液显色;
溶液显色;
Ⅲ.另一种产物能与银氨溶液反应,被氧化为碳酸后分解生成二氧化碳和水。
(6)写出以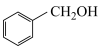 为原料制备
为原料制备 的合成路线流程图
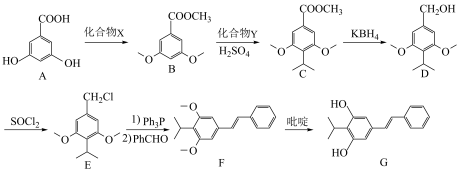
的合成路线流程图______________ (须用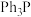 ,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
其中:—Ph为苯基(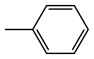 )。
)。
(2)下列有关说法正确的是
Ⅰ.B物质核磁共振氢谱有3组吸收峰,其峰面积之比为1∶1∶2;
Ⅱ.1mol A最多可以与1mol的
 反应,最多可以消耗3mol的
反应,最多可以消耗3mol的 反应;
反应;Ⅲ.1mol A中含有
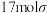 键,室温下,在水中的溶解度A比B大;
键,室温下,在水中的溶解度A比B大;Ⅳ.G物质与足量
 加成产物中有4个手性碳原子,G物质中C原子的杂化类型:
加成产物中有4个手性碳原子,G物质中C原子的杂化类型: 。
。(3)合成路线中设置A到B,将A中酚羟基变为醚键的目的是
(4)Y的分子式为
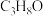 ,其结构简式为
,其结构简式为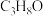 中存在C—O和O—H化学键,可采取的仪器分析方法为
中存在C—O和O—H化学键,可采取的仪器分析方法为A.核磁共振氢谱 B.质谱 C.红外光谱 D.原子发射光谱
(5)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式
Ⅰ.碱性条件下水解后酸化生成两种产物。
Ⅱ.一种产物含有苯环,其核磁共振氢谱只有3组峰,且峰面积之比为1∶2∶1,不能与
 溶液显色;
溶液显色;Ⅲ.另一种产物能与银氨溶液反应,被氧化为碳酸后分解生成二氧化碳和水。
(6)写出以
 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图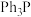 ,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
您最近一年使用:0次
名校
2 . 下列有关说法正确的是
A. 是由非极性共价键形成的极性分子 是由非极性共价键形成的极性分子 |
B.二氯化二硫 分子结构和 分子结构和 类似 类似 |
C. 和 和 的中心原子杂化轨道类型分别为 的中心原子杂化轨道类型分别为 和 和 |
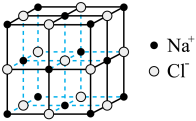
D. 晶胞中氯离子周围最近且等距离的氯离子数为6 晶胞中氯离子周围最近且等距离的氯离子数为6 |
您最近一年使用:0次
名校
3 . 研究 、
、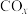 的消除和再利用对改善生态环境、促进低碳社会的构建和环境保护,构建生态文明具有重要的意义。
的消除和再利用对改善生态环境、促进低碳社会的构建和环境保护,构建生态文明具有重要的意义。
(1)采用 作还原剂催化还原
作还原剂催化还原 可以消除氮氧化物的污染。烟气以一定的流速通过催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物的转化率),反应原理为:
可以消除氮氧化物的污染。烟气以一定的流速通过催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物的转化率),反应原理为: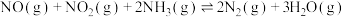 。以下说法正确的是______。
。以下说法正确的是______。
(2)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应用Rh做催化剂时该反应的过程示意图如图所示:__________ 。(填“极性键”、“非极性键”或“极性键和非极性键”)。过程Ⅱ为__________ 过程(填“吸热”或“放热”)。
②已知过程Ⅰ的焓变为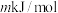 ,过程Ⅱ的焓变为
,过程Ⅱ的焓变为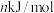 ,则该反应的热化学方程式为:
,则该反应的热化学方程式为:__________ 。
(3) 催化还原NO的物质转化如图所示。若参与反应的
催化还原NO的物质转化如图所示。若参与反应的 和
和 的物质的量之比为4∶1,则转化时
的物质的量之比为4∶1,则转化时 和NO物质的量之比为:
和NO物质的量之比为:__________ 。其中__________ 是催化剂(填化学符号)。______ (填选项)。(A.化学能转化为电能 B.电能转化为化学能),石墨Ⅰ是该电化学装置的______ (填选项)(A.正极 B.负极)石墨Ⅰ电极上发生的电极反应为__________ (提醒:介质为熔融 )。相同条件下,放电过程中消耗的
)。相同条件下,放电过程中消耗的 和
和 的体积比为
的体积比为__________ 。
 、
、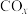 的消除和再利用对改善生态环境、促进低碳社会的构建和环境保护,构建生态文明具有重要的意义。
的消除和再利用对改善生态环境、促进低碳社会的构建和环境保护,构建生态文明具有重要的意义。(1)采用
 作还原剂催化还原
作还原剂催化还原 可以消除氮氧化物的污染。烟气以一定的流速通过催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物的转化率),反应原理为:
可以消除氮氧化物的污染。烟气以一定的流速通过催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物的转化率),反应原理为: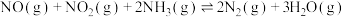 。以下说法正确的是______。
。以下说法正确的是______。A.使用催化剂更有利于提高 的平衡转化率 的平衡转化率 |
| B.及时吹脱水蒸气,可以提高脱氮率 |
| C.其他条件不变的条件下,改变压强对脱氮率没有影响 |
| D.烟气通过催化剂的流速越快,脱氮效果会越好 |
(2)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应用Rh做催化剂时该反应的过程示意图如图所示:

②已知过程Ⅰ的焓变为
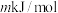 ,过程Ⅱ的焓变为
,过程Ⅱ的焓变为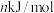 ,则该反应的热化学方程式为:
,则该反应的热化学方程式为:(3)
 催化还原NO的物质转化如图所示。若参与反应的
催化还原NO的物质转化如图所示。若参与反应的 和
和 的物质的量之比为4∶1,则转化时
的物质的量之比为4∶1,则转化时 和NO物质的量之比为:
和NO物质的量之比为: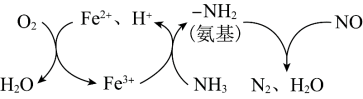
 )。相同条件下,放电过程中消耗的
)。相同条件下,放电过程中消耗的 和
和 的体积比为
的体积比为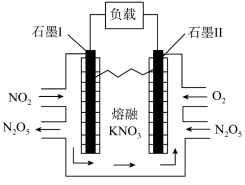
您最近一年使用:0次
名校
4 . 根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 实验结论 |
A | 将 溶液与 溶液与 溶液混合,生成白色 溶液混合,生成白色 沉淀 沉淀 | 结合质子能力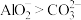 |
B | 将溴乙烷和氢氧化钠的乙醇溶液共热后产生的气体通入酸性 溶液,溶液褪色 溶液,溶液褪色 | 溴乙烷发生消去反应 |
C | 向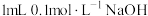 溶液中加入 溶液中加入 溶液,振荡后滴加 溶液,振荡后滴加 葡萄糖溶液,加热,无砖红色沉淀 葡萄糖溶液,加热,无砖红色沉淀 | 葡萄糖中不含有醛基 |
D | 向淀粉溶液中加适量20%的 溶液,加热,冷却后加 溶液,加热,冷却后加 溶液至中性,再滴加碘水,溶液变蓝 溶液至中性,再滴加碘水,溶液变蓝 | 淀粉未水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 通过以下反应可分别获取 和
和 :①通过电解获得
:①通过电解获得 和
和 (装置示意如题图);②在90℃将
(装置示意如题图);②在90℃将 与
与 反应生成
反应生成 并获得
并获得 。下列说法错误的是
。下列说法错误的是
 和
和 :①通过电解获得
:①通过电解获得 和
和 (装置示意如题图);②在90℃将
(装置示意如题图);②在90℃将 与
与 反应生成
反应生成 并获得
并获得 。下列说法错误的是
。下列说法错误的是
A.电解过程中转移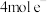 ,理论上可获得标准状况下 ,理论上可获得标准状况下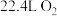 |
B.电解后 溶液的物质的量浓度不变 溶液的物质的量浓度不变 |
C.电解时阳极的电极反应式: |
D.电解的总反应式: |
您最近一年使用:0次
名校
6 . 化合物Z是一种抗骨质疏松药的一种重要中间体,可由下列反应制得。下列有关X、Y、Z的说法错误的是

A.X的分子式为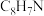 |
B.可用浓溴水溶液鉴别Z和 |
| C.Z可发生取代、加成、还原、氧化、缩聚反应 |
| D.Z与足量的氢气加成后产物中有4个手性碳原子 |
您最近一年使用:0次
名校
7 . 下列对于反应 的有关说法正确的是
的有关说法正确的是
 的有关说法正确的是
的有关说法正确的是A.加入催化剂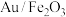 ,反应的焓变 ,反应的焓变 变小 变小 |
B.该反应的 , , |
| C.向固定容积的反应体系中充入氦气,压强增大,因此反应速率加快 |
D.其他条件相同,增大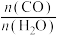 ,反应的平衡常数K不变 ,反应的平衡常数K不变 |
您最近一年使用:0次
名校
解题方法
8 . 下列物质结构与性质或物质性质与用途不具有对应关系的是
A. 溶液有碱性,可除去废铁屑表面的油污 溶液有碱性,可除去废铁屑表面的油污 |
B. 溶液具有氧化性,可用于腐蚀印刷电路板上的Cu 溶液具有氧化性,可用于腐蚀印刷电路板上的Cu |
C. 和 和 中Br所带的电性相同, 中Br所带的电性相同, 和 和 与水反应的产物相同 与水反应的产物相同 |
D.淀粉遇 变蓝, 变蓝, 可用于检验淀粉的存在 可用于检验淀粉的存在 |
您最近一年使用:0次
名校
9 . 氯、溴、碘及其化合物在自然界广泛存在且具有重要应用。氯、溴主要存在于海水中,工业常通过电解 饱和溶液制备
饱和溶液制备 ,
, 可用于制取漂白粉、氯化氢(H—H、Cl—Cl、H—Cl的键能分别为
可用于制取漂白粉、氯化氢(H—H、Cl—Cl、H—Cl的键能分别为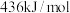 、
、 、
、 )。卤水中
)。卤水中 可通过
可通过 氧化、
氧化、 溶液吸收,
溶液吸收, 能发生水解反应。锂碘电池可供电心脏起搏器,一种
能发生水解反应。锂碘电池可供电心脏起搏器,一种 二次电池正极界面反应机理如图所示。下列化学反应表示错误的是
二次电池正极界面反应机理如图所示。下列化学反应表示错误的是
 饱和溶液制备
饱和溶液制备 ,
, 可用于制取漂白粉、氯化氢(H—H、Cl—Cl、H—Cl的键能分别为
可用于制取漂白粉、氯化氢(H—H、Cl—Cl、H—Cl的键能分别为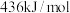 、
、 、
、 )。卤水中
)。卤水中 可通过
可通过 氧化、
氧化、 溶液吸收,
溶液吸收, 能发生水解反应。锂碘电池可供电心脏起搏器,一种
能发生水解反应。锂碘电池可供电心脏起搏器,一种 二次电池正极界面反应机理如图所示。下列化学反应表示错误的是
二次电池正极界面反应机理如图所示。下列化学反应表示错误的是
A. 用 用 溶液吸收: 溶液吸收: |
B. 电池正极放电时的电极反应有: 电池正极放电时的电极反应有: |
C. 与 与 反应: 反应: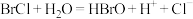 |
D.氯气制氯化氢: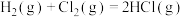  |
您最近一年使用:0次
10 . 水合肼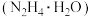 是无色、有强还原性的液体,实验室制备水合肼溶液的反应原理为
是无色、有强还原性的液体,实验室制备水合肼溶液的反应原理为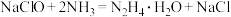 ,
, 能与
能与 剧烈反应。下面是某学生设计的实验中所涉及的装置图(部分夹持装置已省略),下列说法错误的是
剧烈反应。下面是某学生设计的实验中所涉及的装置图(部分夹持装置已省略),下列说法错误的是
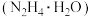 是无色、有强还原性的液体,实验室制备水合肼溶液的反应原理为
是无色、有强还原性的液体,实验室制备水合肼溶液的反应原理为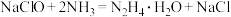 ,
, 能与
能与 剧烈反应。下面是某学生设计的实验中所涉及的装置图(部分夹持装置已省略),下列说法错误的是
剧烈反应。下面是某学生设计的实验中所涉及的装置图(部分夹持装置已省略),下列说法错误的是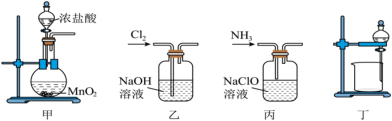
A.制取 装置甲必须加热,或将 装置甲必须加热,或将 替换成 替换成 |
B.用装置乙制备 溶液, 溶液, 是漂白液的有效成分 是漂白液的有效成分 |
| C.用装置丙制备水合肼溶液,应该将导管插入液面以下 |
D.用装置丁无法分离水合肼和 混合溶液 混合溶液 |
您最近一年使用:0次



