名校
解题方法
1 . 有机物A( )具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。部分相关物质的转化如下图:
)具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。部分相关物质的转化如下图:
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被氯取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
回答下列问题:
(1)A的结构简式为_______________ ,B可以发生的反应有__________ (填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称分别是_______________ 、_______________ 。
(3)写出与D、E具有相同官能团的同分异构体的可能结构简式:_______________ 、_______________ 。
(4)E可用于生产氨苄青霉素等。已知E的制备方法不同于其常见的同系物,据报道,可由2-甲基-1-丙醇和甲酸在一定条件下制取E。该反应的化学方程式是________________ 。
 )具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。部分相关物质的转化如下图:
)具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。部分相关物质的转化如下图: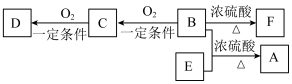
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被氯取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
回答下列问题:
(1)A的结构简式为
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称分别是
(3)写出与D、E具有相同官能团的同分异构体的可能结构简式:
(4)E可用于生产氨苄青霉素等。已知E的制备方法不同于其常见的同系物,据报道,可由2-甲基-1-丙醇和甲酸在一定条件下制取E。该反应的化学方程式是
您最近一年使用:0次
2 . 纳米铁在废水处理、材料研发等领域有重要应用。以某钛白粉厂副产品(主要含 ,还含有
,还含有 、
、 、
、 等杂质)为原料制备纳米铁的流程如下:
等杂质)为原料制备纳米铁的流程如下: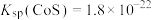 ,
, ,
,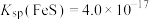 ,
,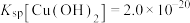 。当溶液中离子浓度小于
。当溶液中离子浓度小于 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。
(1)结合离子方程式解释“除钛”时加入铁粉的作用:________________ 。
(2)“除钴镍”完全后,溶液中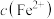 的最大值为
的最大值为___________ mol/L。
(3)用纳米铁去除废水中的 。常温下,选择
。常温下,选择 初始浓度为
初始浓度为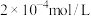 的废水,控制纳米铁的用量相同,测得
的废水,控制纳米铁的用量相同,测得 去除率随初始pH的变化如图-1所示。初始
去除率随初始pH的变化如图-1所示。初始 时
时 去除率明显大于
去除率明显大于 时的原因是
时的原因是________________ 。 是一种优良的磁性材料,该
是一种优良的磁性材料,该 晶胞的
晶胞的 的结构如图-2所示,研究发现结构中的
的结构如图-2所示,研究发现结构中的 只可能出现在图中某一“▲”所示位置上,
只可能出现在图中某一“▲”所示位置上, 所在晶胞的位置在
所在晶胞的位置在_________ 处(填a或b或c)
 ,还含有
,还含有 、
、 、
、 等杂质)为原料制备纳米铁的流程如下:
等杂质)为原料制备纳米铁的流程如下: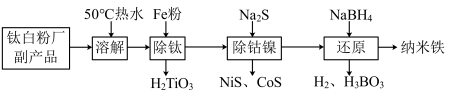
 ,
, ,
,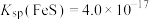 ,
,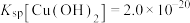 。当溶液中离子浓度小于
。当溶液中离子浓度小于 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。(1)结合离子方程式解释“除钛”时加入铁粉的作用:
(2)“除钴镍”完全后,溶液中
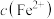 的最大值为
的最大值为(3)用纳米铁去除废水中的
 。常温下,选择
。常温下,选择 初始浓度为
初始浓度为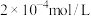 的废水,控制纳米铁的用量相同,测得
的废水,控制纳米铁的用量相同,测得 去除率随初始pH的变化如图-1所示。初始
去除率随初始pH的变化如图-1所示。初始 时
时 去除率明显大于
去除率明显大于 时的原因是
时的原因是
 是一种优良的磁性材料,该
是一种优良的磁性材料,该 晶胞的
晶胞的 的结构如图-2所示,研究发现结构中的
的结构如图-2所示,研究发现结构中的 只可能出现在图中某一“▲”所示位置上,
只可能出现在图中某一“▲”所示位置上, 所在晶胞的位置在
所在晶胞的位置在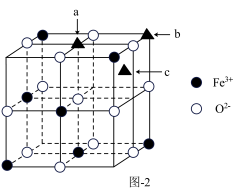
您最近一年使用:0次
名校
3 . 化合物F是一种天然药物合成中的重要中间体,其合成路线如图: 杂化的碳原子数目为
杂化的碳原子数目为___________ 。
(2)A的熔点比对羟基苯甲醛熔点低的原因是___________ 。
(3)D→E的反应过程中会产生一种与E互为同分异构体的副产物,写出该副产物的结构简式:___________ 。
(4)C的一种同分异构体同时满足下列条件,写出其结构简式:___________ 。
①分子中含有苯环,能发生银镜反应,且能使 溶液发生显色反应;
溶液发生显色反应;
②分子中不同化学环境的氢原子个数之比为1∶1∶2∶6。
(5)设计以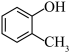 和
和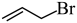 为原料制备
为原料制备 的合成路线(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
的合成路线(无机试剂和有机溶剂任用,合成路线示例见本题题干)。___________ 。

 杂化的碳原子数目为
杂化的碳原子数目为(2)A的熔点比对羟基苯甲醛熔点低的原因是
(3)D→E的反应过程中会产生一种与E互为同分异构体的副产物,写出该副产物的结构简式:
(4)C的一种同分异构体同时满足下列条件,写出其结构简式:
①分子中含有苯环,能发生银镜反应,且能使
 溶液发生显色反应;
溶液发生显色反应;②分子中不同化学环境的氢原子个数之比为1∶1∶2∶6。
(5)设计以
 和
和 为原料制备
为原料制备 的合成路线(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
的合成路线(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
您最近一年使用:0次
名校
4 . 粗铜精炼的副产品铜阳极泥中含有Au、Ag、 、
、 等物质,其含量远高于常规开采的矿石,是提取稀贵金属和硒的重要原料,其中一种分离提取的工艺流程如下:
等物质,其含量远高于常规开采的矿石,是提取稀贵金属和硒的重要原料,其中一种分离提取的工艺流程如下: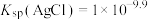
②常温下, 的平衡常数
的平衡常数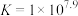
(1)Se与O同族,其基态原子价层电子的运动状态有___________ 种。
(2)“蒸硒”时将铜阳极泥与浓硫酸混合于450~500℃下焙烧,浓硫酸将硒元素氧化为 并蒸出,写出
并蒸出,写出 与浓硫酸反应的化学方程式
与浓硫酸反应的化学方程式___________ 。
(3)“分金”时应控制 的用量,原因是为了减少
的用量,原因是为了减少___________ (填化学式)的产生。
(4)“分银”原理为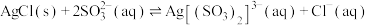 ,常温下该反应的平衡常数为
,常温下该反应的平衡常数为___________ ,若加入1L 溶液充分溶解0.1mol AgCl,理论上
溶液充分溶解0.1mol AgCl,理论上 溶液的浓度须达到
溶液的浓度须达到___________ mol/L(忽略溶解前后溶液的体积变化)。
(5)将滤液2返回“分银”工序循环使用,发现循环多次后银浸出率降低,可能的原因是___________ 。
(6)①粗银电解精炼时需控制电解液的pH为1.5~2,其原因是___________ 。
②银的晶胞结构如图所示,则银原子的配位数是___________ 。
 、
、 等物质,其含量远高于常规开采的矿石,是提取稀贵金属和硒的重要原料,其中一种分离提取的工艺流程如下:
等物质,其含量远高于常规开采的矿石,是提取稀贵金属和硒的重要原料,其中一种分离提取的工艺流程如下:
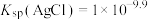
②常温下,
 的平衡常数
的平衡常数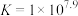
(1)Se与O同族,其基态原子价层电子的运动状态有
(2)“蒸硒”时将铜阳极泥与浓硫酸混合于450~500℃下焙烧,浓硫酸将硒元素氧化为
 并蒸出,写出
并蒸出,写出 与浓硫酸反应的化学方程式
与浓硫酸反应的化学方程式(3)“分金”时应控制
 的用量,原因是为了减少
的用量,原因是为了减少(4)“分银”原理为
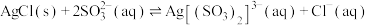 ,常温下该反应的平衡常数为
,常温下该反应的平衡常数为 溶液充分溶解0.1mol AgCl,理论上
溶液充分溶解0.1mol AgCl,理论上 溶液的浓度须达到
溶液的浓度须达到(5)将滤液2返回“分银”工序循环使用,发现循环多次后银浸出率降低,可能的原因是
(6)①粗银电解精炼时需控制电解液的pH为1.5~2,其原因是
②银的晶胞结构如图所示,则银原子的配位数是

您最近一年使用:0次
名校
解题方法
5 . 某研究小组通过下列路线合成镇静药物氯硝西泮。
(1)化合物E的含氧官能团的名称是___________ 。
(2)化合物C的结构简式是___________ 。
(3)合成过程中,设计A→B的目的是___________ 。
(4)E→F合成过程中,碱性条件可能更有利于提高F的产率,原因是___________ 。
(5)写出F→G的化学方程式___________ 。
(6)G→氯硝西泮过程分两步进行,第一步和第二步的反应类型分别为___________ 、___________ 。

已知:①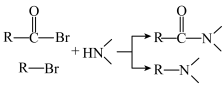 ;②
;②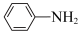 有较强还原性
有较强还原性
(1)化合物E的含氧官能团的名称是
(2)化合物C的结构简式是
(3)合成过程中,设计A→B的目的是
(4)E→F合成过程中,碱性条件可能更有利于提高F的产率,原因是
(5)写出F→G的化学方程式
(6)G→氯硝西泮过程分两步进行,第一步和第二步的反应类型分别为
您最近一年使用:0次
名校
解题方法
6 . 我国科学家成功利用 人工合成淀粉,使淀粉生产方式从农耕种植转变为工业制造成为可能,其部分转化过程如下:
人工合成淀粉,使淀粉生产方式从农耕种植转变为工业制造成为可能,其部分转化过程如下: 水解可制得
水解可制得 。
。
下列有关反应的说法正确的是
 人工合成淀粉,使淀粉生产方式从农耕种植转变为工业制造成为可能,其部分转化过程如下:
人工合成淀粉,使淀粉生产方式从农耕种植转变为工业制造成为可能,其部分转化过程如下:
 水解可制得
水解可制得 。
。下列有关反应的说法正确的是
A.反应①中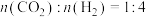 | B.反应②中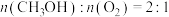 |
| C.反应③中发生了加成反应 | D.反应①~③在高温下速率一定更快 |
您最近一年使用:0次
名校
7 . 二氧化碳加氢制甲烷过程中的主要反应为
反应1: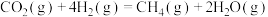
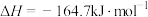
反应2:
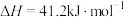
在密闭容器中, 、
、 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如题图所示。下列说法正确的是
实际转化率随温度的变化如题图所示。下列说法正确的是
反应1:
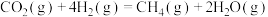
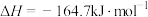
反应2:

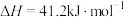
在密闭容器中,
 、
、 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如题图所示。下列说法正确的是
实际转化率随温度的变化如题图所示。下列说法正确的是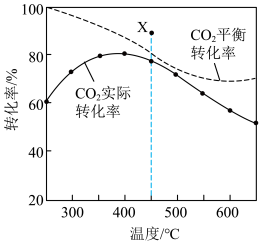
A.反应 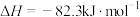 |
| B.增大压强,能使反应1正向移动且K增大 |
| C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃ |
D.450℃时,增大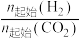 ,能使 ,能使 平衡转化率达到X点的值 平衡转化率达到X点的值 |
您最近一年使用:0次
名校
解题方法
8 . 我国科学家成功利用 人工合成淀粉,使淀粉生产方式从农耕种植转变为工业制造成为可能,其部分转化过程如下:
人工合成淀粉,使淀粉生产方式从农耕种植转变为工业制造成为可能,其部分转化过程如下: 水解可制得
水解可制得 。
。
下列有关物质关系的说法正确的是
 人工合成淀粉,使淀粉生产方式从农耕种植转变为工业制造成为可能,其部分转化过程如下:
人工合成淀粉,使淀粉生产方式从农耕种植转变为工业制造成为可能,其部分转化过程如下: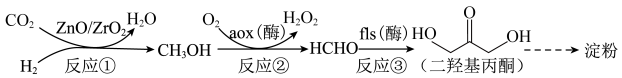
 水解可制得
水解可制得 。
。下列有关物质关系的说法正确的是
A. 通过新制氢氧化铜加热转化为HCHO 通过新制氢氧化铜加热转化为HCHO | B.HCHO和苯酚通过缩聚反应形成酚醛树脂 |
| C.淀粉和纤维素互为同分异构体 | D. 和 和 互为同系物 互为同系物 |
您最近一年使用:0次
名校
解题方法
9 . 某高聚物可表示成如图,下列说法正确的是

| A.该高聚物由二氯乙炔、二氯乙烯和1,3-丁二烯加聚而成 |
B.若该高聚物与足量的 发生加成反应,最多可以消耗2n mol 发生加成反应,最多可以消耗2n mol |
C.该高聚物能被酸性 溶液氧化,也能使溴水褪色 溶液氧化,也能使溴水褪色 |
| D.可以用焚烧或者填埋的方式处理该高聚物的废料 |
您最近一年使用:0次
名校
10 . 下列方案设计、现象和结论正确的是
| 编号 | 目的 | 方案设计 | 现象和结论 |
| A | 判断淀粉是否完全水解 | 在试管中加入0.5g淀粉和4mL2mol/L 溶液,加热,冷却后,加入碘水 溶液,加热,冷却后,加入碘水 | 溶液显蓝色,则说明淀粉未水解 |
| B | 探究苯酚的性质 | 向苯酚浓溶液中加入少量稀溴水 | 未产生白色沉淀,则证明苯酚和稀溴水未发生反应 |
| C | 验证酸性 >苯酚 >苯酚 | 向 固体中滴加乙酸溶液,将生成的气体导入苯酚钠溶液中 固体中滴加乙酸溶液,将生成的气体导入苯酚钠溶液中 | 苯酚钠溶液变浑浊 酸性  >苯酚 >苯酚 |
| D | 检验乙醇的消去产物 | 将乙醇和浓硫酸在170℃共热后的产物,先通过足量氢氧化钠溶液,再通入 |  褪色,证明有乙烯生成 褪色,证明有乙烯生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



