名校
解题方法
1 . 下列反应的化学或离子方程式错误的是
A. 制 制 的离子方程式: 的离子方程式: |
B.白磷与 溶液反应: 溶液反应: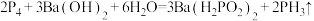 |
C. 与足量的 与足量的 溶液反应的离子方程式: 溶液反应的离子方程式: |
D.雌黄制备雄黄的方程式: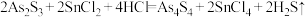 |
您最近一年使用:0次
名校
解题方法
2 . 氨是工业生产硝酸的重要原料,请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:

(1)氨气在“氧化炉”中所发生反应的化学方程式为________ 。
(2)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①氨转化法。已知7 mol氨恰好能将含NO和NO2共6 mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为________ 。
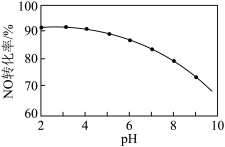
②NaClO溶液氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
Ⅰ.在酸性NaClO溶液中,HClO氧化NO生成Cl-和 ,其离子方程式:
,其离子方程式:________ 。
Ⅱ.NaClO溶液的初始pH越小,NO转化率越高。其原因是________ 。
(3)用硝酸可以回收粗银中的银。取样品0.3000 g溶于足量的硝酸,以NH4Fe(SO4)2·12H2O为指示剂,用0.1 mol/LKSCN标准溶液滴定,当锥形瓶中溶液变为红色,且半分钟内不褪色达滴定终点,平行滴定三次,平均消耗22.00 mLKSCN标准溶液。已知:AgSCN为难溶于水的白色固体,FeSCN2+为红色。通过计算确定粗银中银的回收率________ (假设产品中的杂质不参与反应,写出计算过程)。

(1)氨气在“氧化炉”中所发生反应的化学方程式为
(2)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①氨转化法。已知7 mol氨恰好能将含NO和NO2共6 mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
②NaClO溶液氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
Ⅰ.在酸性NaClO溶液中,HClO氧化NO生成Cl-和
 ,其离子方程式:
,其离子方程式:Ⅱ.NaClO溶液的初始pH越小,NO转化率越高。其原因是
(3)用硝酸可以回收粗银中的银。取样品0.3000 g溶于足量的硝酸,以NH4Fe(SO4)2·12H2O为指示剂,用0.1 mol/LKSCN标准溶液滴定,当锥形瓶中溶液变为红色,且半分钟内不褪色达滴定终点,平行滴定三次,平均消耗22.00 mLKSCN标准溶液。已知:AgSCN为难溶于水的白色固体,FeSCN2+为红色。通过计算确定粗银中银的回收率
您最近一年使用:0次
3 . 工业上由含铜废料(含有 、
、 、
、 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
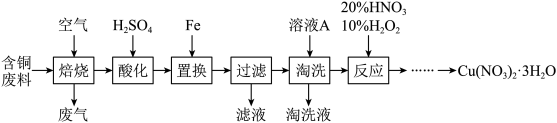
(1)“焙烧”在600℃时进行,写出 转化为
转化为 和
和 的化学方程式:
的化学方程式:________ 。
(2)“淘洗”所用的溶液A可以是________(填字母)。
(3)“反应”这一步所用 试剂是 和
和 ,反应过程中无气体生成,该反应的化学方程式:
,反应过程中无气体生成,该反应的化学方程式:________ 。
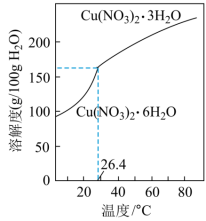
(4)根据题图分析从“反应”所得溶液中析出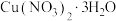 的方法是
的方法是________ 。
 、
、 、
、 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
(1)“焙烧”在600℃时进行,写出
 转化为
转化为 和
和 的化学方程式:
的化学方程式:(2)“淘洗”所用的溶液A可以是________(填字母)。
| A.稀硫酸 | B.浓硫酸 | C.稀硝酸 | D.浓硝酸 |
(3)“反应”这一步所用 试剂是
 和
和 ,反应过程中无气体生成,该反应的化学方程式:
,反应过程中无气体生成,该反应的化学方程式:(4)根据题图分析从“反应”所得溶液中析出
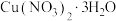 的方法是
的方法是
您最近一年使用:0次
4 . 工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Ni、Si等元素)制备MnSO4,工艺流程如图:

下列说法正确的是

下列说法正确的是
| A.已知“滤渣1”中含有S,则“溶浸”中涉及生成S的反应中氧化剂与还原剂的物质的量之比为1:2 |
| B.“氧化”中添加适量的MnO2的作用是将Fe2+氧化Fe3+为以保证铁元素全部进入“滤渣2” |
| C.为提高生产效率,“调pH”工序应该在较高温度下进行 |
D.沉锰的离子反应为: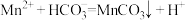 |
您最近一年使用:0次
名校
5 . 水体中氨氮含量超标会造成水体富营养化,用次氯酸钙除去氨氮的原理如图所示。下列说法错误的是
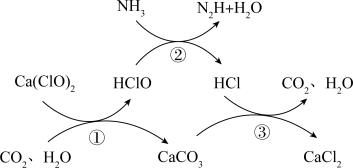

| A.反应①为非氧化还原反应 |
| B.反应②每生成1 mol N2,转移6 mol电子 |
| C.22.4 L二氧化碳所含的共用电子对数目为4NA |
| D.CO2在该反应中能够循环利用 |
您最近一年使用:0次
名校
解题方法
6 . X、Y、Z、M、Q是五种原子序数依次增大的短周期主族元素,X的核外电子数等于其周期数,元素Y的简单气态氢化物的水溶液呈碱性,Z的核外电子数等于X、Y核外电子数之和,M与X同主族,Q是同周期中非金属性最强的元素,下列说法正确的是
| A.氧化物对应水化物的酸性:Q>Y | B.简单离子半径:M>Z |
C. 与MQ的晶体类型不同 与MQ的晶体类型不同 | D.简单氢化物的沸点:Z>Y |
您最近一年使用:0次
名校
解题方法
7 . 下列氮及其化合物的性质与用途具有对应关系的是
| A.N2难溶于水,可用作瓜果保护气 | B.浓硝酸具有强氧化性,可用于钝化铁、铝 |
| C.NH3具有还原性,可用作制冷剂 | D.HNO3具有强氧化性,可用于制硝酸铵 |
您最近一年使用:0次
名校
解题方法
8 . 在题给条件下,下列物质间的转化可以实现的是
A. | B. |
C. | D. |
您最近一年使用:0次
名校
解题方法
9 . 下列相关微粒的化学用语错误的是
A.中子数为9氮原子: | B. 的电子式: 的电子式: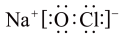 |
C. 的结构式: 的结构式: | D. 的结构示意图: 的结构示意图: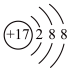 |
您最近一年使用:0次
10 . 电化学在生产中有广泛的应用。下列说法正确的是
| A.工业冶炼金属铝,常采用电解熔融的氯化铝的方法 |
| B.电解精炼铜时,用粗铜作阴极 |
| C.在镀件上镀银时可用纯银作阳极 |
| D.铜的电解精炼时,粗铜中含有的杂质锌、金、银等金属在阳极沉降下来形成阳极泥 |
您最近一年使用:0次
2024-03-29更新
|
93次组卷
|
2卷引用:江苏省镇江市六校联考2023-2024学年高二下学期3月月考化学试题



