名校
解题方法
1 . “微生物法”处理含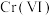 废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含
废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含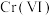 废水。
废水。
(1)硫酸盐还原菌能将水中的 转化为
转化为 ,
, 与
与 可反应生成
可反应生成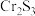 和
和 两种沉淀。写出
两种沉淀。写出 与
与 反应的离子方程式:
反应的离子方程式:___________ 。
(2)用硫酸盐还原菌(SRB)处理含铬废水时,温度常控制在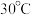 左右,温度过高,
左右,温度过高,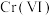 的去除率低的原因是
的去除率低的原因是___________ 。
(3)硫酸盐还原菌(SRB)常存在于水体中,会腐蚀许多金属及合金。一种Fe合金在硫酸盐还原菌存在条件下腐蚀的机理如图所示。已知溶液中的 会完全转化为
会完全转化为 ,则
,则 腐蚀后生成
腐蚀后生成 和
和 的物质的量之比为
的物质的量之比为___________ 。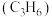 为原料脱硝除去NO,将NO转化为对环境友好的物质。研究表明催化剂添加助剂后催化活性提高的原因是形成活性
为原料脱硝除去NO,将NO转化为对环境友好的物质。研究表明催化剂添加助剂后催化活性提高的原因是形成活性 参与反应,图2为丙烯脱硝机理。
参与反应,图2为丙烯脱硝机理。___________ ,乙为___________ 。(用化学式表示)
②若参加反应的丙烯与 物质的量之比为
物质的量之比为 ,则反应的化学方程式为
,则反应的化学方程式为___________ 。
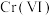 废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含
废水具有效率高、选择性强、吸附容量大等优点。一种微生物法是用硫酸盐还原菌(SRB)处理含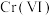 废水。
废水。(1)硫酸盐还原菌能将水中的
 转化为
转化为 ,
, 与
与 可反应生成
可反应生成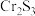 和
和 两种沉淀。写出
两种沉淀。写出 与
与 反应的离子方程式:
反应的离子方程式:(2)用硫酸盐还原菌(SRB)处理含铬废水时,温度常控制在
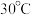 左右,温度过高,
左右,温度过高,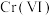 的去除率低的原因是
的去除率低的原因是(3)硫酸盐还原菌(SRB)常存在于水体中,会腐蚀许多金属及合金。一种Fe合金在硫酸盐还原菌存在条件下腐蚀的机理如图所示。已知溶液中的
 会完全转化为
会完全转化为 ,则
,则 腐蚀后生成
腐蚀后生成 和
和 的物质的量之比为
的物质的量之比为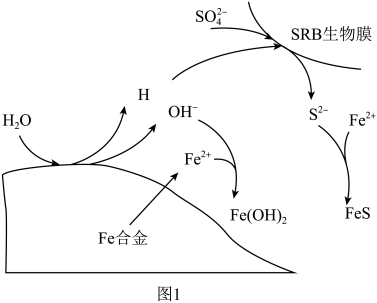
 为原料脱硝除去NO,将NO转化为对环境友好的物质。研究表明催化剂添加助剂后催化活性提高的原因是形成活性
为原料脱硝除去NO,将NO转化为对环境友好的物质。研究表明催化剂添加助剂后催化活性提高的原因是形成活性 参与反应,图2为丙烯脱硝机理。
参与反应,图2为丙烯脱硝机理。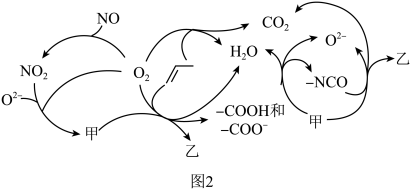
②若参加反应的丙烯与
 物质的量之比为
物质的量之比为 ,则反应的化学方程式为
,则反应的化学方程式为
您最近一年使用:0次
名校
2 . 海洋是一个巨大的化学资源宝库,含有80多种元素,其中含有较高的钠和氯元素。化学家常用廉价氯化钠为原料制备纯碱,也可用于电解法获得金属钠、氯气、氢气等,并进一步将其转化为生产、生活和科学实验中用途更为广泛的新物质,如 、
、 、
、 等。下列物质性质与用途正确且具有对应关系的是
等。下列物质性质与用途正确且具有对应关系的是
 、
、 、
、 等。下列物质性质与用途正确且具有对应关系的是
等。下列物质性质与用途正确且具有对应关系的是A. 溶液显碱性,可用作抗酸药物 溶液显碱性,可用作抗酸药物 |
B. 气体呈黄绿色,可用作自来水消毒剂 气体呈黄绿色,可用作自来水消毒剂 |
C. 具有还原性,可置换出 具有还原性,可置换出 溶液中的 溶液中的 单质 单质 |
| D.NaClO具有强氧化性,可用作漂白液 |
您最近一年使用:0次
解题方法
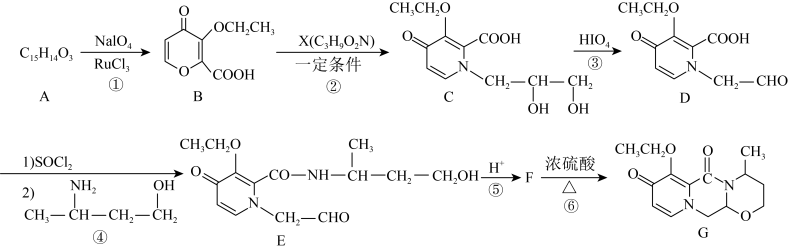
3 . 一种药物中间体G的合成路线如下:________ 。
(2)X的结构简式为________ 。
(3)已知F与E互为同分异构体,则E→F的反应类型为________ 反应。
(4)写出满足下列条件的D的一种同分异构体的的结构简式:________ 。
①能与 溶液发生显色反应;
溶液发生显色反应;
②水解后可得到三种有机产物,其中一种是最简单的α-氨基酸,另两种产物酸化后均只含两种化学环境不同的氢。
(5)写出以 、
、 、2-丁烯为原料制备
、2-丁烯为原料制备
已知:Ⅰ. 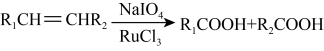
Ⅱ. 
(2)X的结构简式为
(3)已知F与E互为同分异构体,则E→F的反应类型为
(4)写出满足下列条件的D的一种同分异构体的的结构简式:
①能与
 溶液发生显色反应;
溶液发生显色反应;②水解后可得到三种有机产物,其中一种是最简单的α-氨基酸,另两种产物酸化后均只含两种化学环境不同的氢。
(5)写出以
 、
、 、2-丁烯为原料制备
、2-丁烯为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
名校
4 . 一种抗病毒药物盐酸阿比朵尔(Arbidol)合成路线如下:
(1)化合物F中含氧官能团的名称为_______ ;
(2)F→G的反应分为两步,第ⅰ步反应产物的结构简式为_______ 。
(3) 的水溶液显碱性的原因是
的水溶液显碱性的原因是_______ (用化学方程式表示)。
(4)写出同时满足下列条件的E的一种同分异构体的结构简式_______ 。
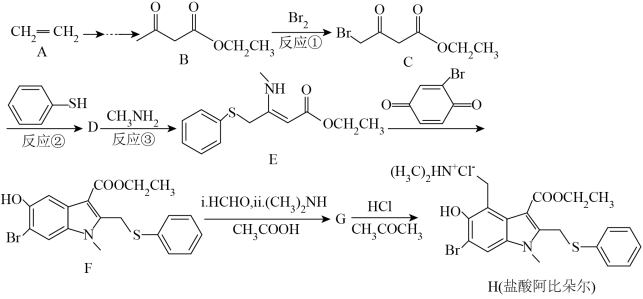
①含有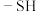 ,同时有手性碳原子:②分子中有6种化学环境的氢原子。
,同时有手性碳原子:②分子中有6种化学环境的氢原子。
(5)结合题干和已知信息,写出由试剂A合成B的路线(无机试剂任选,合成路线流程图示例见本题题干)_______ 。
已知:R1COOR2+R3CH2COOR4
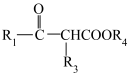 +R2OH
+R2OH
(1)化合物F中含氧官能团的名称为
(2)F→G的反应分为两步,第ⅰ步反应产物的结构简式为
(3)
 的水溶液显碱性的原因是
的水溶液显碱性的原因是(4)写出同时满足下列条件的E的一种同分异构体的结构简式
①含有
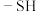 ,同时有手性碳原子:②分子中有6种化学环境的氢原子。
,同时有手性碳原子:②分子中有6种化学环境的氢原子。(5)结合题干和已知信息,写出由试剂A合成B的路线(无机试剂任选,合成路线流程图示例见本题题干)
您最近一年使用:0次
名校
5 . 周期表中ⅡA族元素及其化合物应用广泛。铍的化合物性质与铝相似, 的熔点为
的熔点为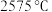 ,熔融时
,熔融时 能导电,而
能导电,而 不能导电;下列有关说法正确的是
不能导电;下列有关说法正确的是
 的熔点为
的熔点为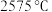 ,熔融时
,熔融时 能导电,而
能导电,而 不能导电;下列有关说法正确的是
不能导电;下列有关说法正确的是
A. 和 和 均为离子化合物 均为离子化合物 |
B. 的晶胞如图所示,晶胞中 的晶胞如图所示,晶胞中 的配位数为4 的配位数为4 |
| C.ⅡA族元素形成的氧化物均能与冷水直接化合成强碱 |
D.在空气中加热蒸发 和 和 溶液都能得到 溶液都能得到 和 和 固体 固体 |
您最近一年使用:0次
2024-01-28更新
|
763次组卷
|
3卷引用:江苏省镇江中学2023-2024学年高一下学期期中检测化学试题
江苏省镇江中学2023-2024学年高一下学期期中检测化学试题2024届江苏省连云港市高三第一次调研考试(一模)化学试题(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
名校
6 . 亚氯酸钠(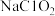 )是一种杀菌漂白剂,可用于棉纺漂白,食品消毒,水处理等,消毒时本身被还原成
)是一种杀菌漂白剂,可用于棉纺漂白,食品消毒,水处理等,消毒时本身被还原成 。亚氯酸钠晶体的一种生产工艺如下:
。亚氯酸钠晶体的一种生产工艺如下:

已知:① 浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。
浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。
② 在温度高于60℃时易分解生成
在温度高于60℃时易分解生成 和NaCl。
和NaCl。
(1)“ 发生器”中:
发生器”中: 与
与 发生反应,该反应的离子方程式为
发生反应,该反应的离子方程式为___________ 。 发生器中鼓入空气的目的是
发生器中鼓入空气的目的是___________ 。
(2)“吸收塔”中: 作
作___________ (填“氧化剂”或“还原剂”或“既不做氧化剂也不做还原剂”)。吸收过程需要控制温度不超过20℃,其原因___________ (填两点)。
(3)结晶: 溶解度曲线如图所示。
溶解度曲线如图所示。

从 溶液中获得无水
溶液中获得无水 晶体的过程对温度的控制要求较高。具体操作:先减压,将
晶体的过程对温度的控制要求较高。具体操作:先减压,将 溶液加热到
溶液加热到___________ (填字母序号)浓缩至有晶膜出现,再在常压下冷却至___________ (填字母序号),过滤,洗涤,干燥。
a.略低于38℃ b.略高于38℃ c.略低于60℃ d.略高于60℃
(4)为测定所得 产品的纯度,进行如下实验:
产品的纯度,进行如下实验:
步骤①:取1.000g样品于烧杯中,用适量蒸馏水溶解后,加入略过量的KI晶体,再滴加适量的稀硫酸,充分反应(反应方程式为: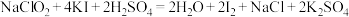 )
)
步骤②:将所得溶液转移至250mL容量瓶中,稀释定容得溶液A;
步骤③:准确移取25.00mL溶液A于锥形瓶中,向锥形瓶中滴加两滴淀粉溶液作指示剂,用 的
的 标准溶液与之反应,至恰好完全反应时消耗
标准溶液与之反应,至恰好完全反应时消耗 溶液22.00mL(反应方程式为:
溶液22.00mL(反应方程式为: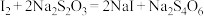 )。
)。
计算该 产品的纯度(写出计算过程)
产品的纯度(写出计算过程)___________ 。
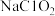 )是一种杀菌漂白剂,可用于棉纺漂白,食品消毒,水处理等,消毒时本身被还原成
)是一种杀菌漂白剂,可用于棉纺漂白,食品消毒,水处理等,消毒时本身被还原成 。亚氯酸钠晶体的一种生产工艺如下:
。亚氯酸钠晶体的一种生产工艺如下:
已知:①
 浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。
浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。②
 在温度高于60℃时易分解生成
在温度高于60℃时易分解生成 和NaCl。
和NaCl。(1)“
 发生器”中:
发生器”中: 与
与 发生反应,该反应的离子方程式为
发生反应,该反应的离子方程式为 发生器中鼓入空气的目的是
发生器中鼓入空气的目的是(2)“吸收塔”中:
 作
作(3)结晶:
 溶解度曲线如图所示。
溶解度曲线如图所示。
从
 溶液中获得无水
溶液中获得无水 晶体的过程对温度的控制要求较高。具体操作:先减压,将
晶体的过程对温度的控制要求较高。具体操作:先减压,将 溶液加热到
溶液加热到a.略低于38℃ b.略高于38℃ c.略低于60℃ d.略高于60℃
(4)为测定所得
 产品的纯度,进行如下实验:
产品的纯度,进行如下实验:步骤①:取1.000g样品于烧杯中,用适量蒸馏水溶解后,加入略过量的KI晶体,再滴加适量的稀硫酸,充分反应(反应方程式为:
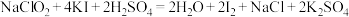 )
)步骤②:将所得溶液转移至250mL容量瓶中,稀释定容得溶液A;
步骤③:准确移取25.00mL溶液A于锥形瓶中,向锥形瓶中滴加两滴淀粉溶液作指示剂,用
 的
的 标准溶液与之反应,至恰好完全反应时消耗
标准溶液与之反应,至恰好完全反应时消耗 溶液22.00mL(反应方程式为:
溶液22.00mL(反应方程式为: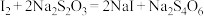 )。
)。计算该
 产品的纯度(写出计算过程)
产品的纯度(写出计算过程)
您最近一年使用:0次
解题方法
7 . 已知: ,氢氧化铜悬浊液受热易分解生成
,氢氧化铜悬浊液受热易分解生成 。蚀刻含铜电路板有多种方法,用蚀刻废液可制备
。蚀刻含铜电路板有多种方法,用蚀刻废液可制备 。
。
(1)酸性蚀刻液法(过氧化氢-盐酸法)。
①用过氧化氢和盐酸蚀刻含铜电路板时发生的离子反应方程式为_______ 。
②反应后有气泡产生,且反应一段时间后,随着溶液变蓝,产生气泡的速率加快,可能的原因是_______ 。
(2)碱性蚀刻液法。碱性含铜蚀刻液主要成分为 、氨水、氯化铵等。蚀刻过程中,
、氨水、氯化铵等。蚀刻过程中, 与电路板上的铜发生反应生成
与电路板上的铜发生反应生成 ,失去蚀刻能力,通入空气可恢复蚀刻能力。
,失去蚀刻能力,通入空气可恢复蚀刻能力。
①
 中
中 键的数目为
键的数目为_______ 。
②蚀刻能力恢复的化学方程式为_______ 。
(3)酸性蚀刻废液与碱性蚀刻废液混和可析出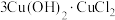 沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
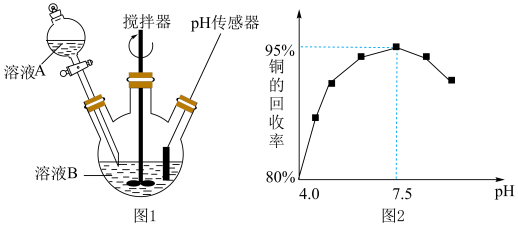
①为减少 胶体形成而影响后续操作,溶液A为
胶体形成而影响后续操作,溶液A为_______ (选填“酸性”或“碱性”)蚀刻废液。
② 时,铜元素回收率下降的原因为
时,铜元素回收率下降的原因为_______ 。
(4)设计从酸性蚀刻废液中制备氧化铜的实验方案。向一定质量的酸性蚀刻废液中_______ 。(实验中必须 使用的试剂:20% 溶液、硝酸银溶液、稀硝酸、蒸馏水)
溶液、硝酸银溶液、稀硝酸、蒸馏水)
 ,氢氧化铜悬浊液受热易分解生成
,氢氧化铜悬浊液受热易分解生成 。蚀刻含铜电路板有多种方法,用蚀刻废液可制备
。蚀刻含铜电路板有多种方法,用蚀刻废液可制备 。
。(1)酸性蚀刻液法(过氧化氢-盐酸法)。
①用过氧化氢和盐酸蚀刻含铜电路板时发生的离子反应方程式为
②反应后有气泡产生,且反应一段时间后,随着溶液变蓝,产生气泡的速率加快,可能的原因是
(2)碱性蚀刻液法。碱性含铜蚀刻液主要成分为
 、氨水、氯化铵等。蚀刻过程中,
、氨水、氯化铵等。蚀刻过程中, 与电路板上的铜发生反应生成
与电路板上的铜发生反应生成 ,失去蚀刻能力,通入空气可恢复蚀刻能力。
,失去蚀刻能力,通入空气可恢复蚀刻能力。①

 中
中 键的数目为
键的数目为②蚀刻能力恢复的化学方程式为
(3)酸性蚀刻废液与碱性蚀刻废液混和可析出
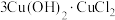 沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
①为减少
 胶体形成而影响后续操作,溶液A为
胶体形成而影响后续操作,溶液A为②
 时,铜元素回收率下降的原因为
时,铜元素回收率下降的原因为(4)设计从酸性蚀刻废液中制备氧化铜的实验方案。向一定质量的酸性蚀刻废液中
 溶液、硝酸银溶液、稀硝酸、蒸馏水)
溶液、硝酸银溶液、稀硝酸、蒸馏水)
您最近一年使用:0次
名校
解题方法
8 . 有机物G是一种治疗帕金森病的药物,其一种合成路线如下:

(1)有机物G中发生 杂化与
杂化与 杂化的碳原子的比例为
杂化的碳原子的比例为_____ 。
(2)已知A→B的反应为加成反应,则B的结构简式为_____ 。
(3)E的一种同分异构体符合下列条件,写出该同分异构体的结构简式:_____ 。
①能与 溶液发生显色反应,能与
溶液发生显色反应,能与 溶液反应生成
溶液反应生成 。
。
②分子中含有4种化学环境不同的氢原子。
(4)已知

写出以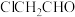 、
、 为原料,制取
为原料,制取 的合成路线图
的合成路线图_____ ,无机试剂及有机溶剂任用,合成示例见本题题干。

(1)有机物G中发生
 杂化与
杂化与 杂化的碳原子的比例为
杂化的碳原子的比例为(2)已知A→B的反应为加成反应,则B的结构简式为
(3)E的一种同分异构体符合下列条件,写出该同分异构体的结构简式:
①能与
 溶液发生显色反应,能与
溶液发生显色反应,能与 溶液反应生成
溶液反应生成 。
。②分子中含有4种化学环境不同的氢原子。
(4)已知

写出以
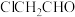 、
、 为原料,制取
为原料,制取 的合成路线图
的合成路线图
您最近一年使用:0次
9 . 硫及其化合物的转化具有重要应用。下列说法不 正确的是
A.实验室检验 既具有氧化性也具有还原性: 既具有氧化性也具有还原性: |
B.工业制硫酸过程中的物质转化: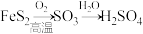 |
C.用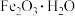 脱除天然气中的 脱除天然气中的 : : |
D.实验室制备少量 的原理: 的原理: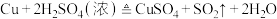 |
您最近一年使用:0次
10 . 将 转化为
转化为 能存效减少
能存效减少 排放。
排放。
(1)已知:Ⅰ.
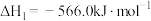
Ⅱ.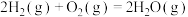
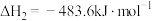
Ⅲ.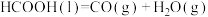
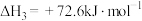
则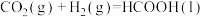

_______ 。
(2)325℃时,水在 粉表面产生
粉表面产生 和
和 ,
, 再与
再与 反应生产甲酸。
反应生产甲酸。
①由 、
、 、
、 制备甲酸的化学方程式为
制备甲酸的化学方程式为_______ 。
②直接加热 与
与 难以生成甲酸,该条件下能较快生成甲酸的原因是
难以生成甲酸,该条件下能较快生成甲酸的原因是_______ 。
(3)科学家利用 在
在 (与
(与 同族)基催化剂上加氢成功制得甲酸,其过程如下图所示。
同族)基催化剂上加氢成功制得甲酸,其过程如下图所示。
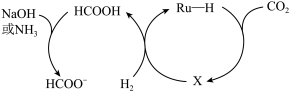
① 与
与 通过加成形成中间体X,画出中间体X的
通过加成形成中间体X,画出中间体X的结构式 :_______ 。
②反应过程中加入 或
或 的目的是
的目的是_______ 。
(4) 通过电解法转化为
通过电解法转化为 的反应机理如图所示,Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的
的反应机理如图所示,Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的 有较好的阻拦作用,可让
有较好的阻拦作用,可让 自由通过。
自由通过。
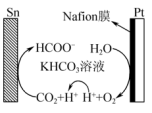
① 电极上生成
电极上生成 的电极反应式为
的电极反应式为_______ 。
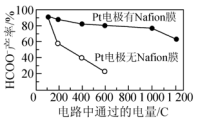
②电路中通过的电量与 产率的关系如图所示,相同条件下,Pt电极有Nafion膜
产率的关系如图所示,相同条件下,Pt电极有Nafion膜 产率明显提高,但电量
产率明显提高,但电量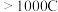 后又显著下降,可能原因是
后又显著下降,可能原因是_______ 。
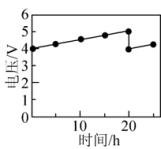
③若电解时将Nafon膜置于两个电极中间,保持电流恒定,20h时向阳极区补充 ,电压与时间关系如图所示,0~20h,电压增大的原因是
,电压与时间关系如图所示,0~20h,电压增大的原因是_______ 。
 转化为
转化为 能存效减少
能存效减少 排放。
排放。(1)已知:Ⅰ.

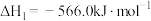
Ⅱ.
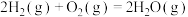
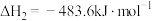
Ⅲ.
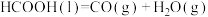
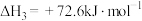
则
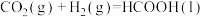

(2)325℃时,水在
 粉表面产生
粉表面产生 和
和 ,
, 再与
再与 反应生产甲酸。
反应生产甲酸。①由
 、
、 、
、 制备甲酸的化学方程式为
制备甲酸的化学方程式为②直接加热
 与
与 难以生成甲酸,该条件下能较快生成甲酸的原因是
难以生成甲酸,该条件下能较快生成甲酸的原因是(3)科学家利用
 在
在 (与
(与 同族)基催化剂上加氢成功制得甲酸,其过程如下图所示。
同族)基催化剂上加氢成功制得甲酸,其过程如下图所示。
①
 与
与 通过加成形成中间体X,画出中间体X的
通过加成形成中间体X,画出中间体X的②反应过程中加入
 或
或 的目的是
的目的是(4)
 通过电解法转化为
通过电解法转化为 的反应机理如图所示,Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的
的反应机理如图所示,Pt电极上覆盖的Nafion膜是一种阳离子交换膜,对浓度不高的 有较好的阻拦作用,可让
有较好的阻拦作用,可让 自由通过。
自由通过。
①
 电极上生成
电极上生成 的电极反应式为
的电极反应式为②电路中通过的电量与
 产率的关系如图所示,相同条件下,Pt电极有Nafion膜
产率的关系如图所示,相同条件下,Pt电极有Nafion膜 产率明显提高,但电量
产率明显提高,但电量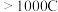 后又显著下降,可能原因是
后又显著下降,可能原因是
③若电解时将Nafon膜置于两个电极中间,保持电流恒定,20h时向阳极区补充
 ,电压与时间关系如图所示,0~20h,电压增大的原因是
,电压与时间关系如图所示,0~20h,电压增大的原因是
您最近一年使用:0次
2023-09-02更新
|
296次组卷
|
2卷引用:江苏省镇江市丹阳市2023-2024学年高三上学期开学考试化学试题



