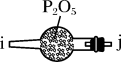
解题方法
1 . 利用反应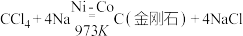 可实现人工合成金刚石。已知
可实现人工合成金刚石。已知 、钠的晶胞如图所示:
、钠的晶胞如图所示:
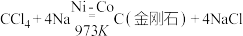 可实现人工合成金刚石。已知
可实现人工合成金刚石。已知 、钠的晶胞如图所示:
、钠的晶胞如图所示: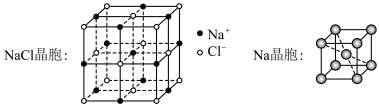
| A.C(金刚石)属于共价晶体 |
B. 晶胞中有2个钠原子 晶胞中有2个钠原子 |
C. 的杂化方式是 的杂化方式是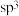 杂化 杂化 |
D. 晶体中每个 晶体中每个 周围有8个 周围有8个 |
您最近一年使用:0次
解题方法
2 . 下列分子的中心原子杂化轨道的类型不相同的是
A. 与 与 | B. 与 与 | C. 与 与 | D. 与 与 |
您最近一年使用:0次
解题方法
3 . 下列叙述正确的是
| A.干冰中存在分子间作用力和共价键,汽化时破坏了共价键 |
B. 的相对分子质量比 的相对分子质量比 的大,其沸点比水的高 的大,其沸点比水的高 |
C. 单质的熔点依次升高,与原子半径大小有关 单质的熔点依次升高,与原子半径大小有关 |
| D.硫酸能形成分子间氢键 |
您最近一年使用:0次
解题方法
4 . 下列说法中,正确的是
| A.分子晶体中,分子间作用力越大,则分子越稳定 |
| B.键长越短,键能越大,所以晶体硅的熔点低于金刚石 |
C.键能: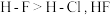 的沸点比 的沸点比 的高 的高 |
| D.氨气极易溶于水是因为氨分子间存在氢键 |
您最近一年使用:0次
5 . 某元素基态原子有4个电子层,它的 原子轨道上只有1个电子,这样的元素有
原子轨道上只有1个电子,这样的元素有
 原子轨道上只有1个电子,这样的元素有
原子轨道上只有1个电子,这样的元素有| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
6 . 工业上可利用硫酸亚铁制备铁盐、亚铁盐、纳米 等。下列说法不正确的是
等。下列说法不正确的是
 等。下列说法不正确的是
等。下列说法不正确的是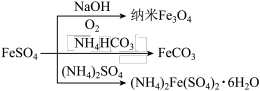
A.纳米 溶于水可以形成胶体 溶于水可以形成胶体 |
B.制备纳米 的反应中,每消耗3mol 的反应中,每消耗3mol ,转移2mol电子 ,转移2mol电子 |
C.制备碳酸亚铁的反应为 |
D.从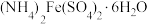 溶液中获取晶体的操作是:蒸发浓缩、降温结晶、过滤、洗涤、干燥 溶液中获取晶体的操作是:蒸发浓缩、降温结晶、过滤、洗涤、干燥 |
您最近一年使用:0次
7 . 高品质 可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质
可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质 的某工艺流程如图:
的某工艺流程如图: 、
、 ,还均含少量Fe、Ca、Mg、Al、Si等元素的氧化物。
,还均含少量Fe、Ca、Mg、Al、Si等元素的氧化物。
②该工艺条件下,相关金属离子完全形成氢氧化物沉淀的pH如表:
回答下列问题:
(1)“配矿”过程中,将软锰矿与黄铁矿粉碎混匀的目的是___________ 。
(2)“酸浸”操作中需先后分批加入 、
、 。加入
。加入 后酸浸过程中主要反应的离子方程式为:
后酸浸过程中主要反应的离子方程式为: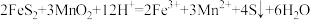 、
、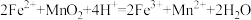 。
。
①已知滤渣1的主要成分为S、 、
、___________ (填化学式)等,其附着在矿粉颗粒表面使上述反应受阻,此时加入 ,利用其迅速分解产生的大量气泡可破除该不利影响。分析导致
,利用其迅速分解产生的大量气泡可破除该不利影响。分析导致 迅速分解的因素是
迅速分解的因素是___________ 。
②矿粉颗粒表面附着物被破除后, 还可以继续与
还可以继续与 反应,从而提高锰元素的浸出率,该反应的离子方程式是
反应,从而提高锰元素的浸出率,该反应的离子方程式是___________ 。
(3)“调pH”操作中需调节溶液pH范围为4.7~6.0,此时“滤渣2”的主要成分为 、
、___________ (填化学式)。
 可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质
可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质 的某工艺流程如图:
的某工艺流程如图: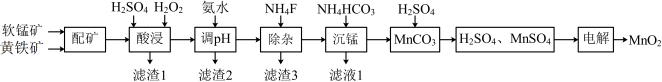
 、
、 ,还均含少量Fe、Ca、Mg、Al、Si等元素的氧化物。
,还均含少量Fe、Ca、Mg、Al、Si等元素的氧化物。②该工艺条件下,相关金属离子完全形成氢氧化物沉淀的pH如表:
| 金属离子 |  |  |  |  |  |
| 开始沉淀pH | 6.9 | 1.9 | 6.6 | 9.1 | 3.4 |
沉淀完全(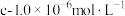 )的pH )的pH | 8.3 | 3.2 | 10.1 | 10.9 | 4.7 |
(1)“配矿”过程中,将软锰矿与黄铁矿粉碎混匀的目的是
(2)“酸浸”操作中需先后分批加入
 、
、 。加入
。加入 后酸浸过程中主要反应的离子方程式为:
后酸浸过程中主要反应的离子方程式为: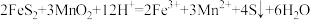 、
、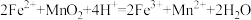 。
。①已知滤渣1的主要成分为S、
 、
、 ,利用其迅速分解产生的大量气泡可破除该不利影响。分析导致
,利用其迅速分解产生的大量气泡可破除该不利影响。分析导致 迅速分解的因素是
迅速分解的因素是②矿粉颗粒表面附着物被破除后,
 还可以继续与
还可以继续与 反应,从而提高锰元素的浸出率,该反应的离子方程式是
反应,从而提高锰元素的浸出率,该反应的离子方程式是(3)“调pH”操作中需调节溶液pH范围为4.7~6.0,此时“滤渣2”的主要成分为
 、
、
您最近一年使用:0次
解题方法
8 . 研究人员对 和Fe粉去除废水中的硝态氮进行研究。已知:
和Fe粉去除废水中的硝态氮进行研究。已知:
i.某工厂排放的含氮废水中总氮=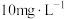 ,含有硝态氮
,含有硝态氮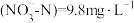 、氨氮
、氨氮 。
。
ii.本实验中 在pH=1~3时,脱除硝态氮转化为
在pH=1~3时,脱除硝态氮转化为 效果较强。
效果较强。
iii. 和Fe粉均可以脱除硝态氮,本实验中二者均为过量。
和Fe粉均可以脱除硝态氮,本实验中二者均为过量。
(1) 和Fe粉在去除废水中硝态氮的过程中表现
和Fe粉在去除废水中硝态氮的过程中表现___________ 性(填“氧化”或“还原”)。
(2)研究 在含氮废水中发生反应时发现,降低溶液pH更有利于
在含氮废水中发生反应时发现,降低溶液pH更有利于 的去除,可能的原因是
的去除,可能的原因是___________ 。
(3)脱除pH=1的含氮废水中硝态氮,单独加入 或同时加入
或同时加入 与Fe粉的实验结果如图1和图2。
与Fe粉的实验结果如图1和图2。 ,脱除NO;主要反应的离子方程式为
,脱除NO;主要反应的离子方程式为___________ 。
②根据图1和图2,图2中20~60min内体系中生成 主要反应的离子方程式为
主要反应的离子方程式为___________ 。
③检验处理后的废水中存在 ,取一定量废水蒸发浓缩,
,取一定量废水蒸发浓缩,___________ (补充操作和现象)。
 和Fe粉去除废水中的硝态氮进行研究。已知:
和Fe粉去除废水中的硝态氮进行研究。已知:i.某工厂排放的含氮废水中总氮=
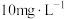 ,含有硝态氮
,含有硝态氮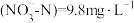 、氨氮
、氨氮 。
。ii.本实验中
 在pH=1~3时,脱除硝态氮转化为
在pH=1~3时,脱除硝态氮转化为 效果较强。
效果较强。iii.
 和Fe粉均可以脱除硝态氮,本实验中二者均为过量。
和Fe粉均可以脱除硝态氮,本实验中二者均为过量。(1)
 和Fe粉在去除废水中硝态氮的过程中表现
和Fe粉在去除废水中硝态氮的过程中表现(2)研究
 在含氮废水中发生反应时发现,降低溶液pH更有利于
在含氮废水中发生反应时发现,降低溶液pH更有利于 的去除,可能的原因是
的去除,可能的原因是(3)脱除pH=1的含氮废水中硝态氮,单独加入
 或同时加入
或同时加入 与Fe粉的实验结果如图1和图2。
与Fe粉的实验结果如图1和图2。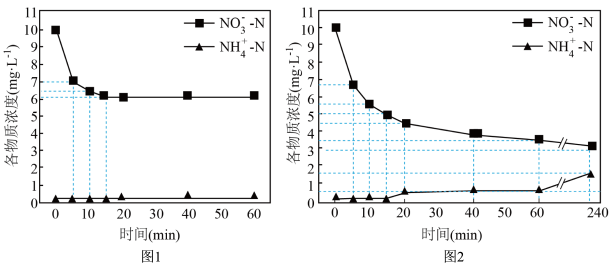
 ,脱除NO;主要反应的离子方程式为
,脱除NO;主要反应的离子方程式为②根据图1和图2,图2中20~60min内体系中生成
 主要反应的离子方程式为
主要反应的离子方程式为③检验处理后的废水中存在
 ,取一定量废水蒸发浓缩,
,取一定量废水蒸发浓缩,
您最近一年使用:0次
9 . 某兴趣小组设计用铁粉将NO还原为 (同时生成FeO)。
(同时生成FeO)。
已知:①浓硝酸可氧化NO。
②NaOH溶液能吸收 ,不吸收NO。
,不吸收NO。
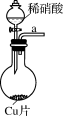
(1)装置甲中的空气含有氧气,所以甲中产生的NO有部分被氧化为 。装置丁的作用是除去挥发来的硝酸和产生的
。装置丁的作用是除去挥发来的硝酸和产生的___________ 。(写化学式)
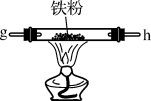
(2)装置戊中发生的化学方程式:___________ 。
(3)装置己的作用是___________ 。
(4)装置的连接顺序为a→___________ 。
(5)装置丙中发生氧化还原反应,生成两种盐,写出反应的离子方程式___________ 。
 (同时生成FeO)。
(同时生成FeO)。
|
|
|
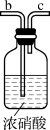
| 甲 | 乙 | 丙 |
|
|
|
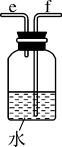
| 丁 | 戊 | 己 |
②NaOH溶液能吸收
 ,不吸收NO。
,不吸收NO。(1)装置甲中的空气含有氧气,所以甲中产生的NO有部分被氧化为
 。装置丁的作用是除去挥发来的硝酸和产生的
。装置丁的作用是除去挥发来的硝酸和产生的(2)装置戊中发生的化学方程式:
(3)装置己的作用是
(4)装置的连接顺序为a→
(5)装置丙中发生氧化还原反应,生成两种盐,写出反应的离子方程式
您最近一年使用:0次
解题方法
10 . 下列指定反应的离子方程式正确的是
A.足量的铁与稀硝酸反应: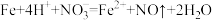 |
B. 溶液中加入过量的NaOH溶液并加热: 溶液中加入过量的NaOH溶液并加热: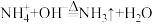 |
C.氢氧化钡溶液中加入足量硫酸氢钠: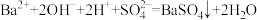 |
D.向偏铝酸钠溶液中通足量二氧化碳: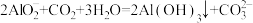 |
您最近一年使用:0次