1 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4。
回答下列问题:
(1)用电子式表示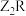 的形成过程:
的形成过程:__________ 。
(2)W在周期表中的位置是__________ 。
(3)ZYX的电子式为__________ , 中含有的化学键类型为
中含有的化学键类型为__________ 。
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是__________ (用元素的离子符号表示)。
(5)下列说法能证明非金属性Q强于R的是__________ (填字母)。
a.简单阴离子的还原性: b.简单氢化物热稳定性:
b.简单氢化物热稳定性:
c.氧化物对应的水化物的酸性: d.Q的单质能从
d.Q的单质能从 溶液中置换出R单质
溶液中置换出R单质
(6)35号元素溴 和Q位于同一主族,被称为“海洋元素”,高溴酸
和Q位于同一主族,被称为“海洋元素”,高溴酸 的酸性比
的酸性比
__________ (填“强”或“弱”),请从位—构—性角度 分析原因_____________ 。
回答下列问题:
(1)用电子式表示
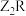 的形成过程:
的形成过程:(2)W在周期表中的位置是
(3)ZYX的电子式为
 中含有的化学键类型为
中含有的化学键类型为(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(5)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:
 b.简单氢化物热稳定性:
b.简单氢化物热稳定性:
c.氧化物对应的水化物的酸性:
 d.Q的单质能从
d.Q的单质能从 溶液中置换出R单质
溶液中置换出R单质(6)35号元素溴
 和Q位于同一主族,被称为“海洋元素”,高溴酸
和Q位于同一主族,被称为“海洋元素”,高溴酸 的酸性比
的酸性比
您最近一年使用:0次
名校
2 . 下表是元素周期表的一部分,a~k分别代表10种元素,请回答:
(1)元素a~k中,其简单氢化物最稳定的是_____ (填元素符号)。
(2)b的简单氢化物的结构式_____ 。
(3)c、d、e、f中形成的简单离子半径由大到小的顺序是_____ (填离子符号)。
(4)写出两种由c原子和e原子构成的化合物的电子式_____ 。
(5)元素h、i的最高价氧化物对应水化物中酸性较强的是_____ (填化学式)。
(6)写出84号元素在元素周期表中的位置_____ 。
(7)g的单质与e的最高价氧化物对应的水化物反应的化学方程式是_____ 。
(8)下列说法能证明金属性k强于f的是_____ (填序号)。
A.k的简单阳离子的氧化性更弱
B.k的氢氧化物水溶液的导电性更强
C.k的单质与水反应更剧烈
| a | ||||||||
| b | c | d | ||||||
| e | f | g | h | i | ||||
| k | …… | |||||||
(2)b的简单氢化物的结构式
(3)c、d、e、f中形成的简单离子半径由大到小的顺序是
(4)写出两种由c原子和e原子构成的化合物的电子式
(5)元素h、i的最高价氧化物对应水化物中酸性较强的是
(6)写出84号元素在元素周期表中的位置
(7)g的单质与e的最高价氧化物对应的水化物反应的化学方程式是
(8)下列说法能证明金属性k强于f的是
A.k的简单阳离子的氧化性更弱
B.k的氢氧化物水溶液的导电性更强
C.k的单质与水反应更剧烈
您最近一年使用:0次
名校
解题方法
3 . 1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中①~⑧代表8种元素。
回答下列问题:
(1)②的元素名称是______ 。
(2)画出⑥的原子结构示意图______ ,写出③与⑦形成的离子化合物的电子式______ 。
(3)③④⑧对应的简单离子半径最小的是______ (用离子符号表示)。
(4)写出⑤的单质与③的最高价氧化物对应水化物反应的离子方程式______ 。
(5)下列说法能证明非金属性⑧强于⑦的是______ (填字母)。
a.简单阴离子的还原性:⑧>⑦ b.简单氢化物的稳定性:⑧>⑦
c.氧化物对应的水化物的酸性:⑧>⑦
(6)由①⑧组成的化合物是______ (填“离子化合物”或“共价化合物”),该化合物的某浓溶液的密度为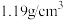 ,溶质质量分数为36.5%,其物质的量浓度为
,溶质质量分数为36.5%,其物质的量浓度为______ mol/L。
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
(1)②的元素名称是
(2)画出⑥的原子结构示意图
(3)③④⑧对应的简单离子半径最小的是
(4)写出⑤的单质与③的最高价氧化物对应水化物反应的离子方程式
(5)下列说法能证明非金属性⑧强于⑦的是
a.简单阴离子的还原性:⑧>⑦ b.简单氢化物的稳定性:⑧>⑦
c.氧化物对应的水化物的酸性:⑧>⑦
(6)由①⑧组成的化合物是
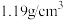 ,溶质质量分数为36.5%,其物质的量浓度为
,溶质质量分数为36.5%,其物质的量浓度为
您最近一年使用:0次
2024-01-22更新
|
107次组卷
|
2卷引用:河南省信阳高级中学2023-2024学年高一下学期开学化学试题
名校
解题方法
4 . 某实验小组对 溶液与
溶液与 溶液的反应进行探究。
溶液的反应进行探究。
已知:① 极易水解,在
极易水解,在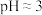 时已经完全沉淀为
时已经完全沉淀为 。
。
②铁氰化钾的化学式为 ,用于检验
,用于检验 ,遇
,遇 离子产生蓝色沉淀。
离子产生蓝色沉淀。
【实验1】
(1)用方程式解释 溶液显碱性的原因
溶液显碱性的原因________ 。配制FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度。从化学平衡角度说明浓盐酸的作用________ 。
(2)探究现象ⅰ产生的原因:
①甲同学认为发生反应: ;他取少量红褐色溶液于试管中,继续滴加
;他取少量红褐色溶液于试管中,继续滴加 溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是______ (填化学式)。
②乙同学认为 与
与 之间仅发生氧化还原反应,其离子方程式为
之间仅发生氧化还原反应,其离子方程式为________ ;该说法是否合理,为什么?_______ 。
③丙同学认为前两位同学所说反应均有发生,他取少许红褐色溶液于试管中,加入______ ,有白色沉淀产生,证明产物中含有 ,说明
,说明 与
与 之间发生了氧化还原反应。
之间发生了氧化还原反应。
④丁同学认为丙同学的实验不严谨,因为_______ 。为了进一步确认 被氧化的原因,丁同学设计了实验2。
被氧化的原因,丁同学设计了实验2。
【实验2】
用下图装置(a、b均为石墨电极)进行实验。闭合开关后灵敏电流计指针偏转。
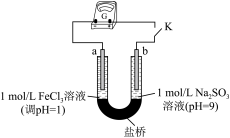
(3)实验2中正极的电极反应式为________ 。丁同学又用铁氰化钾溶液检验正极的产物,观察到有蓝色沉淀产生。他得出的结论是________ 。
(4)综合上述结果,请从平衡移动角度解释现象ⅱ产生的原因:_________ 。
 溶液与
溶液与 溶液的反应进行探究。
溶液的反应进行探究。已知:①
 极易水解,在
极易水解,在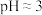 时已经完全沉淀为
时已经完全沉淀为 。
。②铁氰化钾的化学式为
 ,用于检验
,用于检验 ,遇
,遇 离子产生蓝色沉淀。
离子产生蓝色沉淀。【实验1】
| 装置 | 实验现象 |
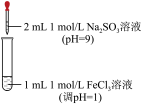 | 现象ⅰ:一开始溶液颜色加深,由棕黄色变为红褐色。 现象ⅱ:一段时间后溶液颜色变浅,变为浅黄色。 |
(1)用方程式解释
 溶液显碱性的原因
溶液显碱性的原因(2)探究现象ⅰ产生的原因:
①甲同学认为发生反应:
 ;他取少量红褐色溶液于试管中,继续滴加
;他取少量红褐色溶液于试管中,继续滴加 溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是②乙同学认为
 与
与 之间仅发生氧化还原反应,其离子方程式为
之间仅发生氧化还原反应,其离子方程式为③丙同学认为前两位同学所说反应均有发生,他取少许红褐色溶液于试管中,加入
 ,说明
,说明 与
与 之间发生了氧化还原反应。
之间发生了氧化还原反应。④丁同学认为丙同学的实验不严谨,因为
 被氧化的原因,丁同学设计了实验2。
被氧化的原因,丁同学设计了实验2。【实验2】
用下图装置(a、b均为石墨电极)进行实验。闭合开关后灵敏电流计指针偏转。

(3)实验2中正极的电极反应式为
(4)综合上述结果,请从平衡移动角度解释现象ⅱ产生的原因:
您最近一年使用:0次
2024-01-15更新
|
80次组卷
|
2卷引用:湖南省常德市汉寿县第一中学2023-2024学年高二下学期开学化学试题
解题方法
5 . 下列关于铁及其化合物的说法正确的是
| A.检验 FeCl2溶液中的Fe2+,可将酸性KMnO4溶液滴加到该溶液中,若酸性KMnO4溶液褪色,证明含有Fe2+ |
| B.Fe3O4中铁的化合价有+2和+3价,是一种混合物 |
| C.为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,应取少量样品溶于盐酸,滴加KSCN溶液,若溶液未变红,说明铁粉未变质 |
| D. FeCl3溶液腐蚀铜板的离子方程式为2Fe3++Cu=2Fe2++Cu2+ |
您最近一年使用:0次
解题方法
6 . 下列离子的检验说法正确的是
| A.用洁净的铂丝蘸取某溶液于酒精灯外焰上灼烧,火焰呈黄色则证明溶液中含有K+ |
| B.某溶液先加氯水,再加KSCN溶液,出现红色则证明一定含有Fe2+ |
C.某溶液加入稀盐酸,产生的气体通入澄清石灰水,溶液变浑浊则证明一定有 |
| D.某溶液先加足量稀HNO3,再加少量AgNO3溶液,生成白色沉淀则证明一定有Cl﹣ |
您最近一年使用:0次
名校
7 .  和
和 在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是

 和
和 在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
A.①中品红褪色证明 有氧化性 有氧化性 |
| B.②中的试剂X应该是浓硫酸 |
| C.③中的试剂Y应该是NaOH溶液 |
D.②中颜色变浅,但不消失,且③中出现浑浊,即可证明气体中有 |
您最近一年使用:0次
2023-07-17更新
|
285次组卷
|
5卷引用:福建省福清第一中学2023-2024学年高一下学期开学适应性练习化学试题
福建省福清第一中学2023-2024学年高一下学期开学适应性练习化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期期末考试化学试题新疆石河子第一中学2023-2024学年高二上学期9月月考化学试题(已下线)第01讲 硫及其化合物-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)(已下线)5.1.2 硫酸
名校
8 . 某同学进行如下实验:
已知:i.H2O2 H++HO
H++HO HO
HO
 H++O
H++O
ii.BaO2是一种白色难溶于水的固体
下列说法不合理的是
| 序号 | 实验① | 实验② | 实验③ | 实验④ | 实验⑤ |
| 方案 | 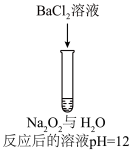 | 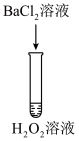 | 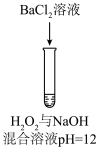 | 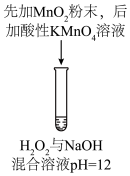 | 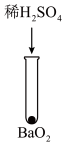 |
| 现象 | 出现白色沉淀 | 无明显现象 | 出现白色沉淀 | 产生大量气泡,高锰酸钾溶液不褪色 | 出现白色沉淀 |
 H++HO
H++HO HO
HO
 H++O
H++O
ii.BaO2是一种白色难溶于水的固体
下列说法不合理的是
| A.实验①和③生成白色沉淀的反应属于复分解反应 |
| B.实验③可证明H2O2溶液中存在电离平衡 |
| C.实验⑤的白色沉淀经检验为BaSO4,但不能证明溶解度BaO2>BaSO4 |
| D.可用BaCl2、MnO2、H2O检验长期放置的Na2O2中是否含有Na2CO3 |
您最近一年使用:0次
9 . 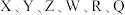 为原子序数依次增大的六种短周期主族元素。
为原子序数依次增大的六种短周期主族元素。 是原子半径最小的元素;
是原子半径最小的元素; 原子最外层电子数是核外电子层数的3倍;
原子最外层电子数是核外电子层数的3倍; 是短周期中金属性最强的元素;
是短周期中金属性最强的元素; 是地壳中含量最多的金属元素;
是地壳中含量最多的金属元素; 的最高正价与最低负价代数和为4。回答下列问题:
的最高正价与最低负价代数和为4。回答下列问题:
(1)用电子式表示
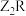 的形成过程:
的形成过程:(2)W在周期表中的位置是
(3)ZYX的电子式为
 中含有的化学键类型为
中含有的化学键类型为(4)
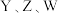 三种元素对应的简单离子半径由大到小的顺序是
三种元素对应的简单离子半径由大到小的顺序是(5)下列说法能证明非金属性
 强于
强于 的是
的是a.简单阴离子的还原性: b.简单氢化物热稳定性:
b.简单氢化物热稳定性:
c.氧化物对应的水化物的酸性: d.
d.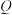 的单质能从
的单质能从 溶液中置换出
溶液中置换出 单质
单质
(6)
 的单质与
的单质与 的最高价氧化物对应的水化物反应的化学方程式为
的最高价氧化物对应的水化物反应的化学方程式为
您最近一年使用:0次
2024-03-29更新
|
163次组卷
|
2卷引用:江西省部分学校2023-2024学年高一下学期开学考化学试题
名校
10 . 宇航服的材料中含有聚酰胺-1010,其结构简式为: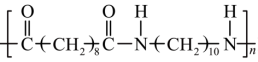 。其中部分制备流程可表示如图:
。其中部分制备流程可表示如图:

最后通过G与J合成聚酰胺-1010。
已知:①RCN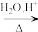 RCOOH
RCOOH
②2 R1OOCR2COOH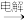 R1OOCR2-R2COOR1+2CO2↑+H2↑
R1OOCR2-R2COOR1+2CO2↑+H2↑
回答下列问题:
(1)实验室用电石(主要成分为CaC2)和水反应制取A.如图是制备装置。下列有关说法正确的是___________。

(2)A→B的反应类型为___________ 。
(3)D的结构简式为___________ 。
(4)E中的含氧官能团名称是___________ 。
(5)F→G的第一步的化学方程式为___________ 。
(6)写出一种符合下列条件的D的同分异构体的结构简式___________ 。
①分子内含有2个-CH3; ②能与NaHCO3溶液反应放出CO2;
③能发生水解反应; ④能发生银镜反应; ⑤核磁共振氢谱有5组峰。
(7)芳纶—1414(结构简式如图所示)也可用作舱外航天服材料。
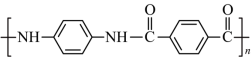
写出以对二甲苯( )为原料合成芳纶—1414的合成路线流程图。(无机试剂和有机溶剂任用)。
)为原料合成芳纶—1414的合成路线流程图。(无机试剂和有机溶剂任用)。___________
已知:羧酸铵可部分脱水生成酰胺,酰胺在碱性次卤酸盐条件下可发生Hofmann降级反应:R-COONH4 R-CONH2
R-CONH2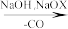 RNH2
RNH2
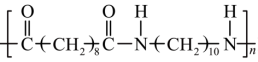 。其中部分制备流程可表示如图:
。其中部分制备流程可表示如图:
最后通过G与J合成聚酰胺-1010。
已知:①RCN
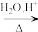 RCOOH
RCOOH②2 R1OOCR2COOH
 R1OOCR2-R2COOR1+2CO2↑+H2↑
R1OOCR2-R2COOR1+2CO2↑+H2↑回答下列问题:
(1)实验室用电石(主要成分为CaC2)和水反应制取A.如图是制备装置。下列有关说法正确的是___________。

| A.可以用启普发生器代替图中的气体发生装置 |
| B.将收集好的气体通入酸性高锰酸钾溶液中,若酸性高锰酸钾溶液褪色,则证明该气体是A |
| C.可用饱和食盐水代替水,减缓反应速率 |
| D.若要制取较纯净的乙炔,可用CuSO4溶液除去杂质气体 |
(2)A→B的反应类型为
(3)D的结构简式为
(4)E中的含氧官能团名称是
(5)F→G的第一步的化学方程式为
(6)写出一种符合下列条件的D的同分异构体的结构简式
①分子内含有2个-CH3; ②能与NaHCO3溶液反应放出CO2;
③能发生水解反应; ④能发生银镜反应; ⑤核磁共振氢谱有5组峰。
(7)芳纶—1414(结构简式如图所示)也可用作舱外航天服材料。
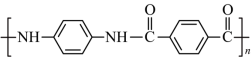
写出以对二甲苯(
 )为原料合成芳纶—1414的合成路线流程图。(无机试剂和有机溶剂任用)。
)为原料合成芳纶—1414的合成路线流程图。(无机试剂和有机溶剂任用)。已知:羧酸铵可部分脱水生成酰胺,酰胺在碱性次卤酸盐条件下可发生Hofmann降级反应:R-COONH4
 R-CONH2
R-CONH2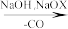 RNH2
RNH2
您最近一年使用:0次



