名校
解题方法
1 . 联氨( )溶于水可以发生与氨类似的电离。常温下,向20 mL 0.1 mol⋅L
)溶于水可以发生与氨类似的电离。常温下,向20 mL 0.1 mol⋅L 联氨盐酸盐溶液(
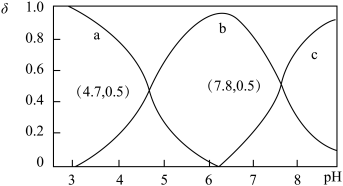
联氨盐酸盐溶液(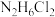 )中加入NaOH固体(假设溶液体积变化忽略不计)。体系中各含氮粒子的分布系数(δ)随pH的变化如图所示。下列说法正确的是
)中加入NaOH固体(假设溶液体积变化忽略不计)。体系中各含氮粒子的分布系数(δ)随pH的变化如图所示。下列说法正确的是
 )溶于水可以发生与氨类似的电离。常温下,向20 mL 0.1 mol⋅L
)溶于水可以发生与氨类似的电离。常温下,向20 mL 0.1 mol⋅L 联氨盐酸盐溶液(
联氨盐酸盐溶液(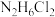 )中加入NaOH固体(假设溶液体积变化忽略不计)。体系中各含氮粒子的分布系数(δ)随pH的变化如图所示。下列说法正确的是
)中加入NaOH固体(假设溶液体积变化忽略不计)。体系中各含氮粒子的分布系数(δ)随pH的变化如图所示。下列说法正确的是
A.曲线a可表示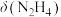 随pH的变化关系 随pH的变化关系 |
B. 时, 时, |
C.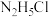 溶液中: 溶液中: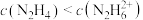 |
D.常温下,反应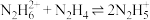 的平衡常数为 的平衡常数为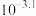 |
您最近一年使用:0次
2023-08-31更新
|
501次组卷
|
2卷引用:山西省大同市2023-2024学年高三上学期开学质量检测化学试题
名校
解题方法
2 . 在 的晶体空隙中插入金属离子可获得超导体。一种超导体的面心立方晶胞如图1所示,已知:晶胞参数为
的晶体空隙中插入金属离子可获得超导体。一种超导体的面心立方晶胞如图1所示,已知:晶胞参数为 ,各点的原子分数坐标分别为
,各点的原子分数坐标分别为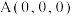 ,
,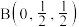 。下列说法错误的是
。下列说法错误的是
 的晶体空隙中插入金属离子可获得超导体。一种超导体的面心立方晶胞如图1所示,已知:晶胞参数为
的晶体空隙中插入金属离子可获得超导体。一种超导体的面心立方晶胞如图1所示,已知:晶胞参数为 ,各点的原子分数坐标分别为
,各点的原子分数坐标分别为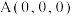 ,
,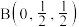 。下列说法错误的是
。下列说法错误的是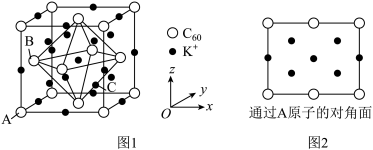
| A.通过A原子的对角面结构如图2所示 | B.相邻两个 的最短距离为 的最短距离为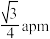 |
C.晶胞中C点原子分数坐标为 | D.该晶体的密度表达式为 |
您最近一年使用:0次
2023-02-09更新
|
1684次组卷
|
8卷引用:山西省运城市康杰中学2023-2024学年高二下学期开学考试化学试题
山西省运城市康杰中学2023-2024学年高二下学期开学考试化学试题广东省清远市清新区部分学校2022-2023学年高三下学期2月联考化学试题广东省清远市清新区部分学校2022-2023学年高三2月联考化学试题湖北省武汉市洪山高级中学2022-2023学年高二下学期2月考试化学试题山东省曹县第一中学2022-2023学年高二下学期2月月考化学试题(已下线)专题卷20 《物质结构与性质》选择题分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)2023年湖南卷高考真题变式题(选择题11-14)浙江省宁波市镇海中2023-2024学年高二下学期期中考试化学试题
3 . 无机化合物A主要用于药物制造。在一定条件下,2.30g固体A与5.35gNH4Cl固体恰好完全反应,生成固体B和4.48L气体C(标准状况)。气体C极易溶于水得到碱性溶液,电解无水B可生成一种短周期元素的金属单质D和氯气。由文献资料知道:工业上物质A可用金属D与液态的C在硝酸铁催化下反应来制备,纯净的A物质为白色固体,但制得的粗品往往是灰色的;物质A的熔点390℃,沸点430℃,密度大于苯或甲苯,遇水反应剧烈,也要避免接触酸、酒精。在空气中A缓慢分解,对其加强热则猛烈分解,在750~800℃分解为化合物E和气体C。
回答下列问题:
(1)A的化学式____________ 。
(2)A与盐酸反应的化学方程式为____________ 。
(3)A在750~800℃分解的方程式为____________ ,制得的粗品往往是灰色的,其可能的原因是_________ 。
(4)久置的A可能大部分变质而不能使用,需要将其销毁。遇到这种情况,可用苯或甲苯将其覆盖,然后缓慢加入用苯或甲苯稀释过的无水乙醇,试解释其化学原理:__________ 。
(5)工业制备单质D的流程图如下:

①步骤①中操作名称是__________ 。
②试用平衡移动原理解释步骤②中减压的目的是_______________ 。
(6)写出D的重氢化合物与水反应的化学方程式为____________ 。
回答下列问题:
(1)A的化学式
(2)A与盐酸反应的化学方程式为
(3)A在750~800℃分解的方程式为
(4)久置的A可能大部分变质而不能使用,需要将其销毁。遇到这种情况,可用苯或甲苯将其覆盖,然后缓慢加入用苯或甲苯稀释过的无水乙醇,试解释其化学原理:
(5)工业制备单质D的流程图如下:

①步骤①中操作名称是
②试用平衡移动原理解释步骤②中减压的目的是
(6)写出D的重氢化合物与水反应的化学方程式为
您最近一年使用:0次
2016-12-09更新
|
372次组卷
|
2卷引用:2017届山西省重点中学协作体高三上学期开学考试化学试卷
4 . 废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧电池的铜帽(Cu、Zn 总含量约为99%)回收Cu并制备ZnO 的部分实验过程如下:
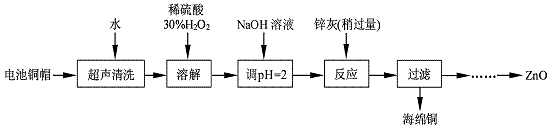
(1)写出铜帽溶解时铜与加入的稀硫酸、30%H2O2反应的离子反应方程式:_________________ ;铜帽溶解完全后,需加热(至沸)将溶液中过量的H2O2除去。
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2 后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中反应的离子方程式如下:
2Cu2++4I-=2CuI(白色)↓+I2 2S2O32-+I2=2I-+S4O62-
①滴定选用的指示剂为___________ ,滴定终点观察到的现象为_______________ ;
②某同学称取1.0g电池铜帽进行实验,得到100.00mL含有Cu2+的溶液,量取20.00mL上述含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用0.1000mol/L Na2S2O3标准溶液滴定至终点。再重复操作实验3次,记录数据如下:
计算电池铜帽中Cu的质量分数为__________ ,(结果保留四位有效数字)若滴定前溶液中的H2O2没有除尽,则所测定c (Cu2+)将会___________ (填“偏高”、“偏低”或“无影响”);
(3)常温下,若向50mL 0.0001mol/L CuSO4溶液中加入50mL0.00022mol/LNaOH溶液,生成了沉淀。已知KSP[Cu (OH)2] =2.0×10-20(mol/L)3,计算沉淀生成后溶液中c(Cu2+)=_____ mol/L;
(4)已知pH>11 时Zn(OH)2 能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0 mol·L-1计算)。
实验中可选用的试剂:30%H2O2、1.0 mol·L-1HNO3、1.0 mol·L-1NaOH。由除去铜的滤液制备ZnO的实验步骤依次为:①向滤液中加入适量30% H2O2,使其充分反应;
②_______________________ ;③过滤;
④______________________ ;⑤过滤、洗涤、干燥;⑥900℃煅烧。

(1)写出铜帽溶解时铜与加入的稀硫酸、30%H2O2反应的离子反应方程式:
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2 后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中反应的离子方程式如下:
2Cu2++4I-=2CuI(白色)↓+I2 2S2O32-+I2=2I-+S4O62-
①滴定选用的指示剂为
②某同学称取1.0g电池铜帽进行实验,得到100.00mL含有Cu2+的溶液,量取20.00mL上述含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用0.1000mol/L Na2S2O3标准溶液滴定至终点。再重复操作实验3次,记录数据如下:
| 实验编号 | 1 | 2 | 3 | 4 |
| V(Na2S2O3)(mL) | 28.32 | 25.31 | 25.30 | 25.32 |
计算电池铜帽中Cu的质量分数为
(3)常温下,若向50mL 0.0001mol/L CuSO4溶液中加入50mL0.00022mol/LNaOH溶液,生成了沉淀。已知KSP[Cu (OH)2] =2.0×10-20(mol/L)3,计算沉淀生成后溶液中c(Cu2+)=
(4)已知pH>11 时Zn(OH)2 能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0 mol·L-1计算)。
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
实验中可选用的试剂:30%H2O2、1.0 mol·L-1HNO3、1.0 mol·L-1NaOH。由除去铜的滤液制备ZnO的实验步骤依次为:①向滤液中加入适量30% H2O2,使其充分反应;
②
④
您最近一年使用:0次
2016-01-25更新
|
258次组卷
|
3卷引用:2017届山西省重点中学协作体高三上学期开学考试化学试卷



